O que há de novo em
Progeria Research
Adicionamos esta seção para que você possa acessar facilmente as informações sobre as publicações científicas mais recentes e significativas sobre a pesquisa da Progéria.
Além dos artigos destacados abaixo, agora existem centenas de artigos sobre Progeria e assuntos relacionados à Progeria. Sugerimos que você pesquise no PubMed para encontrar os tópicos específicos que está procurando.
Março de 2023: Marcos emocionantes de pesquisa na avaliação do tratamento e extensão da vida!
Temos o prazer de compartilhar com você duas emocionantes atualizações de pesquisas, publicadas on-line hoje no principal jornal cardiovascular do mundo, Circulação (1):
Biomarcador na Progéria
Uma nova maneira de medir a progerina, a proteína tóxica que causa a Progéria, foi desenvolvida por uma equipe liderada pelo cofundador e diretor médico da PRF, Dr. Leslie Gordon. Com a descoberta desse biomarcador, que usa o plasma sanguíneo para medir os níveis de progerina, os pesquisadores podem entender como os tratamentos estão afetando os participantes de ensaios clínicos após um período de tempo mais curto e em vários pontos ao longo de cada ensaio clínico.
Este teste pode otimizar o processo de ensaio clínico ao fornecer informações antecipadas sobre a eficácia dos tratamentos que estão sendo testados, como uma introdução a outros testes clínicos, como ganho de peso, alterações dermatológicas, contratura e função articular, etc., todos os quais requerem muito mais tempo para se manifestar. Essas características clínicas da Progéria são importantes medidas de longo prazo dos efeitos do tratamento que agora são complementadas pelos níveis de progerina medidos anteriormente na terapia. Agora podemos entender os benefícios do tratamento quatro meses após o início do tratamento ou interromper um tratamento que pode não beneficiar o participante do estudo, para evitar efeitos colaterais desnecessários.
Vidas ainda mais longas com lonafarnib
Além de acelerar o tratamento futuro e as descobertas de cura, esta nova e inovadora forma de medir a progerina indica que o benefício a longo prazo de lonafarnib para crianças com Progéria é maior do que previamente determinado.
Os dados do estudo indicam que níveis mais baixos de progerina no sangue refletem o benefício de sobrevivência: quanto mais tempo alguém com Progéria permanece no lonafarnib, maior o benefício de sobrevivência de estar em terapia. Os níveis de progerina diminuíram em cerca de 30-60% enquanto o medicamento foi tomado, e a expectativa de vida para pacientes em tratamento por mais de 10 anos foi estimada em quase 5 anos. Isso é um aumento de mais de 35% na expectativa de vida média, de 14.5 anos para quase 20 anos de idade!
Para saber mais, veja nosso comunicado de imprensa aqui
“Uma das histórias mais marcantes já compartilhadas neste podcast”
– Dra. Carolyn Lam, especialista em coração de renome mundial e apresentadora do podcast Circulação na corrida, na jornada que levou a essas descobertas empolgantes. Ouça a entrevista completa sobre o profundo impacto deste estudo diretamente do Dr. Gordon. Ouvir SUA PARTICIPAÇÃO FAZ A DIFERENÇA (começando às 6:41).
Ouça a Dra. Leslie Gordon no podcast Circulation on the Run
E em junho, dois artigos editoriais (2) e (3) foram publicados em Circulação destacando a importância crítica desse biomarcador para o avanço dos tratamentos e a cura de crianças com Progéria e para uma melhor compreensão do envelhecimento.

(1) Gordon, LB, Norris, W., Hamren, S., et al. Progerina plasmática em pacientes com síndrome de Hutchinson-Gilford Progeria: desenvolvimento de imunoensaio e avaliação clínica. Circulação, 2023
(2) Progressão de anormalidades cardíacas na síndrome de Hutchinson-Gilford Progeria: um estudo longitudinal prospectivo.
Olsen FJ, Gordon LB, Smoot L, Kleinman ME, Gerhard-Herman M, Hegde SM, Mukundan S, Mahoney T, Massaro J, Ha S, Prakash A. Circulação. 2023 de junho de 6;147(23):1782-1784. doi: 10.1161/CIRCULATIONAHA.123.064370. Epub 2023 5 de junho.
(3) Ferramentas prontamente disponíveis para detectar progerina e progressão da doença cardíaca na síndrome de Hutchinson-Gilford Progeria.
Eriksson M, Haugaa K, Revêchon G. Circulação. 2023 de junho de 6;147(23):1745-1747. doi: 10.1161/CIRCULATIONAHA.123.064765. Epub 2023 5 de junho.
Março de 2021: Revelações emocionantes em RNA Therapeutics for Progeria!
Estamos entusiasmados em compartilhar os resultados de dois estudos revolucionários muito empolgantes sobre o uso de RNA terapêutico em pesquisa Progeria. Ambos os estudos foram co-financiados pela The Progeria Research Foundation (PRF) e co-criados pelo Diretor Médico da PRF, Dra. Leslie Gordon.
A progerina é a proteína causadora da doença na Progéria. As terapias de RNA interferem na capacidade do corpo de produzir progerina, bloqueando sua produção no nível de RNA. Isso significa que o tratamento é mais específico do que a maioria das terapias que têm como alvo a progerina no nível da proteína.
Embora cada estudo tenha usado um sistema de entrega de drogas diferente, ambos os estudos direcionaram a mesma estratégia básica de tratamento, inibindo a produção de codificação de RNA para a proteína anormal, progerina. Ambos foram liderados por pesquisadores do National Institutes of Health (NIH), e foram publicados hoje na revista Nature Medicine.
Um estudo, liderado por Francis Collins, MD, PhD, Diretor do NIH, mostrou que o tratamento de camundongos Progéria com uma droga chamada SRP2001 reducou o mRNA da progerina prejudicial e a expressão da proteína na aorta, a principal artéria do corpo, bem como em outros tecidos. No final do estudo, a parede aórtica permaneceu mais forte e os ratos demonstraram um aumento da sobrevivência de mais de 60%.
"Ter uma terapia de RNA direcionada que mostre resultados tão significativos em um modelo animal me dá esperança de que isso possa levar a um grande avanço no tratamento da progéria", disse Collins.
A outro estudo, liderado por Tom Misteli, PhD, Diretor do Center for Cancer Research, National Cancer Institute, NIH, mostrou um 90 - 95% de redução do RNA tóxico produtor de progerina em diferentes tecidos após o tratamento com um medicamento denominado LB143. O laboratório de Misteli descobriu que a redução da proteína progerina foi mais eficaz no fígado, com melhorias adicionais no coração e na aorta.
Agora sabemos que existem várias maneiras de diminuir a produção da proteína progerina prejudicial usando a terapêutica de RNA. Cada estudo encontrou diferentes trechos de RNA nos modelos de camundongos que, quando direcionados, entregaram um caminho eficaz para o tratamento, resultando em Camundongos Progeria que viveram muito mais do que aqueles tratados em estudos anteriores com Zokinvy (lonafarnibe), o único medicamento aprovado pela FDA para crianças com Progéria. Além disso, os pesquisadores descobriram que um tratamento combinado com RNA terapêutico e Zokinvy (lonafarnibe) reduziu os níveis de proteína progerina no fígado e no coração de forma mais eficaz do que qualquer um dos tratamentos isolados.
“Esses dois estudos altamente importantes demonstram o grandes avanços que estão agora sobre nós no campo da terapêutica de Progeria direcionada ”, disse o Diretor Médico da PRF, Dra. Leslie Gordon. “Fiquei entusiasmado em trabalhar com esses grupos de pesquisa brilhantes para promover a terapia de RNA para crianças com Progéria. Ambos são estudos empolgantes de prova de princípio e PRF está animado para avançar em direção aos ensaios clínicos que aplicam essas estratégias de tratamento.
-
Erdos, MR, Cabral, WA, Tavarez, UL et ai. Uma abordagem terapêutica antisense direcionada para a síndrome de Hutchinson-Gilford progeria. Nat Med (2021). https://doi.org/10.1038/s41591-021-01274-0
Puttaraju, M., Jackson, M., Klein, S. et ai. A triagem sistemática identifica oligonucleotídeos anti-sentido terapêuticos para a síndrome de progéria de Hutchinson-Gilford. Nat Med (2021). https://doi.org/10.1038/s41591-021-01262-4
Janeiro de 2021: notável progresso na edição genética em modelos de camundongos Progeria
A revista científica Natureza resultados de descoberta publicados demonstrar que a edição genética em um modelo de camundongo da Progéria corrigiu a mutação que causa a Progéria em muitas células, melhorou vários sintomas-chave da doença e aumentou drasticamente a expectativa de vida dos camundongos.
Co-financiado pela PRF e coautor do Diretor Médico da PRF, Dra. Leslie Gordon, o estudo descobriu que, com uma única injeção de um editor básico programado para corrigir a mutação causadora da doença, os ratos sobreviveram 2.5 vezes mais do que os ratos Progeria não tratados de controle. a uma idade correspondente ao início da velhice em camundongos saudáveis. É importante ressaltar que os camundongos tratados também retiveram tecido vascular saudável - um achado significativo, pois a perda de integridade vascular é um preditor de mortalidade em crianças com Progéria.
O estudo foi co-liderado por especialista mundial em edição genética, David Liu, PhD, do Broad Institute, MIT, Jonathan Brown, Professor Assistente de Medicina na Divisão de Medicina Cardiovascular da Universidade de Vanderbilt, e Francis Collins, MD, PhD, Diretor do National Institutes of Health.
“Ver essa resposta dramática em nosso modelo de camundongo Progeria é um dos desenvolvimentos terapêuticos mais interessantes de que participei em 40 anos como médico-cientista”, disse o Dr. Collins.
“Cinco anos atrás, ainda estávamos terminando o desenvolvimento do primeiro editor de base”, disse o Dr. Liu. “Se você tivesse me dito que dentro de cinco anos, uma única dose de um editor básico poderia tratar a Progéria em um animal nos níveis de DNA, RNA, proteína, patologia vascular e tempo de vida, eu teria dito 'não tem como'. É uma verdadeira prova da dedicação da equipa que tornou este trabalho possível. ”
Estudos pré-clínicos adicionais são necessários para investigar esses resultados, que esperamos um dia levem a um ensaio clínico. Leia mais sobre esta notícia emocionante neste Wall Street Journal artigo.
Novembro de 2020: Aprovação do FDA para lonafarnibe (Zokinvy)
Em 20 de novembro de 2020, a PRF cumpriu uma parte importante de nossa missão: lonafarnibe, o primeiro tratamento para Progéria, recebeu a aprovação da FDA.
A Progéria agora se junta a menos de 5% das doenças raras com um tratamento aprovado pela FDA. * Crianças e jovens adultos com Progéria nos EUA agora podem ter acesso ao lonafarnibe (agora chamado de 'Zokinvy') por receita, em vez de por meio de um ensaio clínico.
Este marco importante foi alcançado graças a 13 anos inabaláveis de pesquisa envolvendo quatro ensaios clínicos, todos co-coordenados pela PRF, tornados possíveis pelas crianças corajosas e suas famílias, e financiados por você, a maravilhosa comunidade de doadores da PRF.
Clique aqui para obter mais informações.
* 300 doenças raras com tratamento aprovado pela FDA (https://www.rarediseases.info.nih.gov/diseases/FDS-orphan-drugs)/7,000 doenças raras para as quais a base molecular é conhecida (www.OMIM. org) = 4.2%
Abril 2018: Estudo global publicado no JAMA encontra tratamento com Lonafarnib prolonga a sobrevivência em crianças com Progéria
Clique aqui para mais detalhes.
Associação de tratamento com Lonafarnib vs nenhum tratamento com taxa de mortalidade em pacientes com síndrome de Hutchinson-Gilford Progeria, Leslie B. Gordon, MD, PhD; Heather Shappell, PhD; Joe Massaro, PhD; Ralph B. D'Agostino Sr., PhD; Joan Brazier, MS; Susan E. Campbell, MA; Monica E. Kleinman, MD; Mark W. Kieran, MD, PhD; JAMA, Abril 24, 2018.
Julho 2016: resultados de testes triplos
Outubro 2014: a notável jornada da PRF publicada na Expert Opinion
 Em um artigo publicado no Opinião de um 'expert e da autoria da diretora executiva Audrey Gordon e da diretora médica Leslie Gordon, os dois líderes da PRF discutem a história, as metas e as realizações da PRF, e como os programas da PRF têm sido fundamentais na jornada da obscuridade ao tratamento.
Em um artigo publicado no Opinião de um 'expert e da autoria da diretora executiva Audrey Gordon e da diretora médica Leslie Gordon, os dois líderes da PRF discutem a história, as metas e as realizações da PRF, e como os programas da PRF têm sido fundamentais na jornada da obscuridade ao tratamento.
Os autores escrevem: “É nossa esperança que a descrição dos programas e serviços da PRF a seguir, juntamente com um relato de como eles estão ajudando a PRF a cumprir sua missão de salvar crianças com Progéria, ajude e inspire outras pessoas a tomarem medidas semelhantes para as muitas populações de doenças raras que precisam de atenção imediata. ”
Maio 2014: Estudo constata que medicações experimentais aumentam a vida útil estimada em crianças com progéria
Este estudo demonstra que há evidências de que um inibidor da farnesiltransferase (FTI) pode prolongar a vida de crianças com Progéria por pelo menos um ano e meio. O estudo mostrou uma extensão da sobrevida média dos anos 1.6 durante os seis anos após o início do tratamento. Dois medicamentos adicionais adicionados posteriormente nos ensaios, pravastatina e zoledronato, também podem contribuir para esse achado. Esta é a primeira evidência de tratamentos que influenciam a sobrevivência desta doença fatal.
Clique aqui para mais detalhes.
Impacto dos inibidores da farnesilação na sobrevivência na síndrome de Progeria de Hutchinson-Gilford, Leslie B. Gordon, MD, PhD, Joe Massaro, PhD, Ralph B. D'Agostino Sr., PhD, Susan E. Campbell, MA, Joan Brazier, MS, W. Ted Brown, MD, PhD, Monica E Kleinman, MD, Mark W. Kieran MD, PhD e Progeria Clinical Trials Collaborative; Circulação, Maio 2, 2014 (on-line).
Setembro 2012: Descoberto o primeiro tratamento de Progéria para Progéria
Os resultados o primeiro teste clínico de medicamentos para crianças com Progéria revelam que Lonafarnib, um tipo de inibidor da farnesiltransferase (FTI) originalmente desenvolvido para tratar o câncer, provou ser eficaz para Progéria. Cada criança apresenta melhora em uma ou mais das quatro maneiras: ganhando peso adicional, melhor audição, melhor estrutura óssea e / ou, mais importante, maior flexibilidade dos vasos sanguíneos. O estudo * foi financiado e coordenado pela The Progeria Research Foundation.
Clique aqui para mais detalhes.
* Gordon LBO objetivo deste estudo foi avaliar a eficácia do uso de antimicrobianos em pacientes com câncer de próstata, bem como sobre o uso de antidepressivos em pacientes com câncer de próstata. Os pacientes com síndrome de Hutchinson-Gilford Progeria são mais propensos a desenvolver um câncer de colo uterino, que é mais comum em crianças com síndrome de prognóstico de Hutchinson-Gilford. Proceedings, da Academia Nacional de Ciências, 9 de outubro de 2012 vol. 109 não. 41 16666-16671
Outubro 2011: Uma nova abordagem para a terapia com progeria
Esse splicing aberrante em células cutâneas cultivadas de Progéria pode ser evitado dessa maneira, foi demonstrado em 2005 (2). No entanto, para o tratamento de pacientes, o reagente inibidor deve ser administrado intacto a todos os tecidos do paciente. levou mais seis anos, e trabalho em vários laboratórios, para desenvolver esses métodos de “entrega”.
Na nova pesquisa (1), o bloqueio do splicing aberrante no mouse modelo resultou em resultados impressionantes. Houve nítidas reduções nas concentrações de progerina em todos os tecidos analisados, exceto no músculo esquelético, que pode ter uma captação reduzida do agente bloqueador. O modelo de camundongo recapitulou muitos dos fenótipos de pacientes com Progéria, incluindo
- Vida útil severamente reduzida (dias 103 em comparação com os anos 2 para ratos do tipo selvagem).
- Redução da taxa de crescimento.
- Postura anormal com curvatura da coluna vertebral.
- Aberrações nucleares profundas como resultado do acúmulo de progerina.
- Perda geral da camada de gordura sob a pele.
- Alterações ósseas profundas.
- Alterações cardiovasculares, incluindo perda significativa de células do músculo liso vascular.
- Alterações nas concentrações de vários hormônios no plasma sanguíneo circulante, incluindo insulina e hormônio do crescimento.
A in vivo A demonstração da eficácia da redução da produção de progerina, bloqueando o splicing aberrante, é um forte candidato a uma nova e valiosa abordagem da terapia com Progeria.
(1) Osório FG, Navarro CL, Cadiñanos J, López-Mejia IC, Quirós PM, et al., Science Translational Medicine, 3: Edição 106, publicação on-line antecipada, 26 de outubro (2011).
(2) Scaffidi, P. e Misteli, T. Reversão do fenótipo celular na doença de envelhecimento precoce síndrome de progeria de Hutchinson-Gilford, Nature Medicine 11 (4): 440-445 (2005).
Junho 2011: Estudo financiado pelo PRF identifica a rapamicina como possível tratamento para a progéria
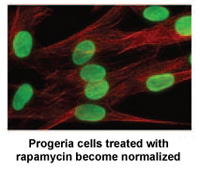
Pesquisadores do National Institutes of Health e Massachusetts General Hospital, em Boston, MA publicaram um novo estudo hoje em Ciência, Medicina Translacional isso pode levar a um novo tratamento medicamentoso para crianças com Progéria. *
rapamicina é um medicamento aprovado pela FDA que já demonstrou prolongar a vida de modelos de camundongos que não são da progéria. Este novo estudo demonstra que a rapamicina diminui a quantidade de proteína progerina causadora da doença em 50%, melhora a forma nuclear anormal e prolonga a vida útil das células progeria. Este estudo fornece a primeira evidência de que a rapamicina pode diminuir os efeitos prejudiciais da progerina em crianças com progéria.
Há uma enorme cobertura da mídia sobre isso! Clique abaixo para obter links para histórias da mídia:
Blog de saúde do Wall Street Journal
A Fundação Progeria Research teve o prazer de fornecer células para este projeto do Banco de células e tecidos PRFe ajudar a financiar a pesquisa por meio de nossos programa de bolsas.
Este novo e empolgante estudo demonstra o ritmo notável da pesquisa sobre progeria, ao mesmo tempo em que fornece mais informações sobre o processo de envelhecimento que afeta a todos nós.
* "A rapamicina reverte os fenótipos celulares e melhora a liberação de proteínas mutantes nas células de progeria de Hutchinson-Gilford"
Kan Cao, John J. Graziotto, Cecilia D. Blair, Joseph R. Mazzulli, Michael R. Erdos, Dimitri Krainc, Francis S. Collins
Sci Transl Med. 2011 Jun 29; 3 (89): 89ra58.
Junho 2011: Estudo inovador sobre a relação Progeria-envelhecimento
CBS Evening News, Wall Street Journal e Outros Relatório sobre Novo Estudo
Pesquisadores do National Institutes of Health descobriram uma ligação até então desconhecida entre Progeria e envelhecimento. Os resultados fornecem informações sobre a relação entre a proteína tóxica causadora da Progéria, conhecida como progerina e telômeros, que protegem as extremidades do DNA nas células até que se desgastem com o tempo e as células morram.
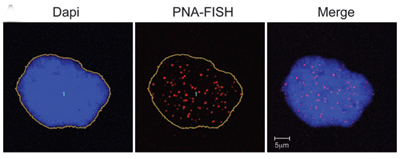
As células que expressam progerina de indivíduos normais apresentam sinais de senescência. O DNA no núcleo é corado em azul. Os telômeros são vistos como pontos vermelhos.
O estudo * aparece na edição inicial online de junho do 13, 2011 do Journal of Clinical Investigation. Conclui que no envelhecimento normal, os telômeros curtos ou disfuncionais estimulam as células a produzir progerina, que está associada ao dano celular relacionado à idade.
"Pela primeira vez, sabemos que o encurtamento e a disfunção dos telômeros influenciam a produção de progerina ”, diz Leslie B. Gordon, diretora médica da Fundação Progeria Research Foundation. "Portanto, esses dois processos, que influenciam o envelhecimento celular, estão realmente ligados."
Pesquisas anteriores mostraram que a progerina não é produzida apenas em crianças com Progéria, mas que é produzida em menor quantidade em todos nós, e os níveis de progerina aumentam com o envelhecimento. Independentemente, pesquisas anteriores sobre encurtamento e disfunção dos telômeros foram associadas ao envelhecimento normal. Desde a 2003, com a descoberta da mutação do gene Progeria e da proteína progerina que causa a doença, uma das principais áreas de pesquisa se concentra em entender se e como a Progeria e o envelhecimento estão relacionados.
"Conectar esse fenômeno de doença rara e o envelhecimento normal está dando frutos de uma maneira importante", disse o diretor do NIH, Francis S. Collins, MD, PhD, autor sênior do artigo. “Este estudo destaca que informações biológicas valiosas são obtidas através do estudo de desordens genéticas raras, como a Progéria. Desde o início, pensamos que a Progeria tinha muito a nos ensinar sobre o processo normal de envelhecimento. "
Os cientistas tradicionalmente estudam telômeros e progerina separadamente. Embora ainda haja muito a aprender sobre se essa nova conexão pode levar a uma cura para crianças com Progéria ou potencialmente ser aplicada para prolongar a vida humana, este estudo fornece mais evidências de que a progerina, a proteína tóxica descoberta ao encontrar a mutação genética em Progeria , desempenha um papel no processo normal de envelhecimento.
*Disfunção de progerina e telômeros colaboram para desencadear senescência celular em fibroblastos humanos normaisCao e cols. J Clin Invest doi: 10.1172 / JCI43578.
Clique aqui para o texto completo do comunicado de imprensa do NIH.
Pode 2011: descoberta da causa da síndrome progeroide, fornecendo mais informações sobre o vínculo da Progeria com o envelhecimento
Uma equipe de pesquisa liderada pelo pesquisador Progeria Dr. Carlos López-Otín da Universidade de Oviedo, na Espanha, encontrou duas famílias cujos filhos têm uma doença do envelhecimento acelerado desconhecida, semelhante à Progéria. As crianças não mostraram defeitos em nenhum gene anteriormente associado a doenças progeroides, mas estudando as partes "codificadoras" de seus genomas, a equipe encontrou um defeito em um gene chamado BANF1. Os membros da família com a doença progeroide tinham quantidades muito baixas da proteína produzida pelo BANF1 e, como as pessoas com Progéria, os envelopes nucleares em suas células eram marcadamente anormais. As anormalidades desapareceram em experimentos de cultura de células quando o gene defeituoso foi substituído pela versão correta. Os resultados foram publicados no American Journal of Human Genetics em maio 2011.
O BANF1 agora se junta ao grupo de genes conhecidos que parecem influenciar algumas formas de envelhecimento prematuro - e que também podem afetar o envelhecimento normal.
Nos últimos anos, os cientistas conseguiram entender melhor o envelhecimento normal em nível molecular, graças em parte a estudos de síndromes de envelhecimento prematuro como este e Progeria, que “causam o desenvolvimento precoce de características normalmente associadas à idade avançada, ”Disse López-Otín. Ele acrescentou que seu estudo "ressalta a importância da lâmina nuclear para o envelhecimento humano e demonstra a utilidade dos novos métodos de sequenciamento do genoma para identificar a causa genética de doenças raras e devastadoras, que tradicionalmente recebem atenção limitada".
Xose S. Puente, Victor Quesada, Fernando G. Osório, Rubén Cabanillas, Juan Cadiñanos, Julia M. Fraile, Gonzalo R. Ordóñez, Diana A. Puente, Ana Gutiérrez-Fernández, Miriam Fanjul-Fernández et al. "Seqüenciamento de exoma e análise funcional identificam a mutação BANF1 como a causa de uma síndrome progeroide hereditária". American Journal of Human Genetics, maio 5, 2011 DOI: 10.1016 / j.ajhg.2011.04.010
Agosto 2010: Fator de crescimento semelhante à insulina 1 melhora os sintomas e prolonga a vida de um rato progeroide
Em agosto 26, 2010, Arteriosclerose, trombose e biologia vascular publicado eletronicamente, antes da impressão, os resultados de um estudo comparando a Progéria e o envelhecimento cardiovascular típico, intitulado "Patologia Cardiovascular na Progeria de Hutchinson-Gilford: correlação com a patologia vascular do envelhecimento". O estudo constatou que a progerina, a proteína anormal que causa a Progéria, também está presente na vasculatura da população em geral e aumenta com a idade, aumentando o crescente caso de haver paralelos entre o envelhecimento normal e o envelhecimento da progeria.
Os pesquisadores examinaram autópsias cardiovasculares e distribuição de progerina em pacientes com Progéria, juntamente com um grupo sem Progeria entre as idades de um mês e os anos 97, e descobriram que a progerina em indivíduos sem Progeria aumentou uma média de 3.3 por cento ao ano nas artérias coronárias.
"Encontramos semelhanças entre muitos aspectos da doença cardiovascular na Progéria e na aterosclerose que afeta milhões de pessoas em todo o mundo", disse Leslie Gordon, autora sênior do estudo e diretora médica da Fundação Progeria Research. “Ao examinar uma das doenças mais raras do mundo, estamos obtendo uma visão crucial de uma doença que afeta milhões de pessoas em todo o mundo. Pesquisas em andamento têm o potencial de ter um impacto significativo em nossa compreensão de doenças cardíacas e envelhecimento. ”
Este estudo apóia a possibilidade de a progerina contribuir para o risco de aterosclerose na população em geral e merece o exame como uma nova característica em potencial para ajudar a prever o risco de doença cardíaca.
O objetivo deste trabalho foi avaliar os efeitos do uso de esteroides anabolizantes em pacientes com hipersensibilidade conhecida a qualquer componente da fórmula. Nabel EG, Gordon LB.
“Patologia Cardiovascular na Progeria de Hutchinson-Gilford: Correlação com a Patologia Vascular do Envelhecimento”. Arterioscler Thromb Vasc Biol. 2010 Nov; 30 (11): 2301-9; Epub 2010 Ago 26.
Maio 2010: Estudos em Oxford mostram como a pesquisa da Progeria pode melhorar nossa compreensão do envelhecimento normal
Esta situação é muito semelhante à da Progéria. Lá, a pré-lâmina A (chamada progerina) retém o grupo farnesil. Na verdade, o passo inicial para causar a doença é a falha em remover o grupo farnesil. Essa falha ocorre porque a mutação da Progéria resulta na deleção da parte da pré-lâmina A necessária para que o FACE 1 se ligue e remova o grupo farnesil. Assim, a causa dos defeitos no envelhecimento e na Progéria é a mesma: o FACE1 não consegue fazer seu trabalho.
É sabido há alguns anos que os inibidores da farnesil transferase (FTIs) inibem (e podem reverter) a presença de marcadores nucleares da doença nas células de Progéria. Agora, Shanahan et al descobriram que os FTIs inibem o aparecimento de marcadores nucleares semelhantes em células de indivíduos idosos normais. Os FTIs estão atualmente em uso em ensaios clínicos de Progeria e Shanahan et al observam que, esses ensaios clínicos “irão lançar mais luz sobre o potencial terapêutico dessas drogas no tratamento do envelhecimento”.
Os estudos descritos neste artigo são o melhor exemplo até o momento de como os estudos sobre Progéria estão aprimorando nossa compreensão do envelhecimento normal.
Ragnauth CD, Warren DT, Liu Y, Shanahan CM et al, "Prelamin A Acts to Accelerate Smooth Muscle Cell Senescence and is a Novel biomarker of Human Vascular Aging." Circulação: 25 de maio de 2010, pp. 2200-2210.
Abril 2010: Mais evidências de que na Progéria, a presença de um grupo farnesil na molécula de progerina é responsável pelos sintomas da doença.
Davies e colegas de trabalho prepararam um novo modelo de mouse cuja pré-laminina A, diferentemente da RD pré-laminina A, não é farnesilada, mas retém a sequência de aminoácidos 15 que normalmente é clivada no caminho para sintetizar a lâmina A. Este mouse não apresenta sintomas progeróides, indicando que na RD, bem como na Progéria, a presença do grupo farnesil, e não uma alteração na sequência de aminoácidos, é responsável pelos sintomas da doença.
Os dados foram analisados por meio de questionários, entrevistas e entrevistas com os participantes.
"Um acúmulo de prelamin A não-varnesilada causa cardiomiopatia, mas não progeria", Hum Mol Genet. 2010 abr 26. [Epub antes da impressão]
Fevereiro 2010: Mais evidências de que os FTIs proporcionam efeitos benéficos através da farnesilação de progerina
Os autores avaliaram a possibilidade de que a ameliação da doença progeroide por um inibidor de farnesiltransferase (FTI) em um modelo de Progeria em camundongos seja devida ao efeito do medicamento na farnesilação de proteínas que não sejam progerina. Eles construíram um camundongo que produzia progerina não desnesilada, mas não progerina farnesilada. Este camundongo também desenvolveu fenótipos de doenças semelhantes a progéria, mas o FTI não os melhorou. Este resultado indica que o medicamento não age inibindo outras proteínas além da progerina; deve estar atuando na farnesilação da progerina, a etapa bioquímica que não está presente no modelo testado.
Yang SH, Chang SY, Andres DA, Spielmann HP, SG Jovem, Fong LG. "Avaliando a eficácia dos inibidores da proteína farnesiltransferase em modelos de progeria em camundongos".
J Lipid Res. 2010 fev; 51 (2): 400-5. Epub 2009 Oct 26.
Outubro 2009: As artes encontram as ciências na história de Benjamin Button
Maloney WJ, “Síndrome de Hutchinson-Gilford Progeria: sua apresentação no conto de F. Scott Fitzgerald 'o curioso caso de Benjamin Button' e suas manifestações orais”.
J. Dent. Res 2009 Oct 88 (10): 873-6
Maio 2009: Artigo abre novos caminhos sobre o efeito HGPS nas funções celulares.
Já foi demonstrado que o HGPS afeta muitas funções celulares fundamentais, incluindo replicação, expressão gênica e reparo de DNA. Busch e colegas de trabalho adicionaram o transporte de proteínas do citoplasma ao núcleo nesta lista. Todas as proteínas são sintetizadas no citoplasma, e as que acabam por estar no núcleo precisam atravessar a membrana nuclear. O transporte é realizado através de canais na membrana nuclear chamados "poros nucleares". Muitas proteínas são grandes demais para simplesmente se difundir através dos poros nucleares, mas são "introduzidas" através delas por proteínas especiais que evoluíram para esse fim. Neste artigo, verificou-se que as células que expressam o gene mutante responsável pelo HGPS reduziram o transporte de proteínas para os núcleos por medição direta.
Busch A, Kiel T, Heupel WM, Wehnert M, Huebner S., "A importação de proteína nuclear é reduzida em células que expressam mutantes lamin A nucleares causadores de envelopatia nuclear". Exp Cell Res. 2009 Maio 11.
Abril 2009: Vinculando Progéria e Envelhecimento Normal: Novos Insights
→ Fornecendo estrutura e organização: arquitetura nuclear e integridade do genoma
→ Danos e reparos no DNA deram errado
→ Supressores de tumores antigos e além do reparo e senescência celular, e
→ Regeneração e renovação: biologia de células-tronco. Regeneração e renovação: biologia de células-tronco.
O artigo destaca as maneiras pelas quais os recentes avanços no estudo de doenças progeroides estão dando uma visão das funções celulares básicas e do envelhecimento.
Capell BS, Tlougan BE, Orlow SJ, “Do mais raro ao mais comum: percepções de síndromes progeroides sobre câncer de pele e envelhecimento”. Journal of Investigative Dermatology (2009 abr 23), 1-11
Abril 2009: Ex-bolsistas de pesquisa da PRF criam novo método para estudar progerina em células
Experiências anteriores com células de fibroblastos de pacientes com Progéria mostraram que o dano causado pela mutação é inicialmente o resultado da ação da forma alterada da Lamin A, chamada Progerin. Mas a interpretação desses experimentos pode ser difícil na cultura para vários números de gerações. Fong et. al. criaram um sistema experimental em que a quantidade de Progerin na Tipo selvagem as células podem ser aumentadas ou diminuídas. Esse método permitirá que os pesquisadores classifiquem os efeitos diretos do Progerin dos secundários, avançando, assim, o estudo dos mecanismos celulares que levam à fisiopatologia das células da Progéria.
Ativando a síntese de progerina, a mutante prelamin A na síndrome de progeria de Hutchinson-Gilford, com oligonucleotídeos antisense. (Artigo PubMed) Fong LG, Vickers TA, Farber EA, Choi C, Yun UJ, Hu Y, Yang SH, Coffinier C, Lee R, Yin L, Davies BS, Andres DA, Spielmann HP, Bennett CF, Young SG, “Ativando a síntese de progerina, a prelamin A mutante na síndrome de progeria de Hutchinson-Gilford, com oligonucleotídeos antisense. ” Hum Mol Genet. 2009 Apr 17.
Drs. Fong e Young foram anteriormente financiados com doações da Fundação Progeria de Pesquisa.
Janeiro 2009: Quantificação da expressão gênica de Progéria em células normais e de Progéria por uma nova e poderosa técnica.
Equipe sueca descobre acúmulo de RNA de progerina em células normais à medida que envelhece
Progerin é a proteína anormal que causa Progeria. Nos últimos anos, vários grupos de pesquisa descobriram que as células normais também produzem progerina, mas muito menos do que as células de uma criança com Progéria. Além disso, a quantidade de proteína progerina nas células normais aumenta à medida que envelhecem em laboratório. Esses resultados estabeleceram uma ligação direta no nível celular entre a Progéria e o envelhecimento normal.
A Dra. Maria Eriksson, autora da descoberta de genes para Progeria no 2003, agora inventou uma nova e poderosa técnica para medir quantitativamente a expressão do gene Progeria. O laboratório do Dr. Eriksson no Instituto Karolinska, na Suécia, usou a técnica para medir a quantidade de RNA de progerina nas células normais e nas células de Progéria. O RNA é a molécula da planta em nossas células para a produção de proteínas. O grupo sueco descobriu que as células normais e as células Progeria produzem quantidades cada vez maiores de RNA de progerina à medida que envelhecem. O resultado de Eriksson mostra que o sinal de RNA para a produção de progerina se acumula rapidamente nas células das crianças com Progéria e se desenvolve lentamente ao longo da vida em todos nós.
Essas novas descobertas fortalecem nossa compreensão da conexão entre envelhecimento normal e Progéria. Além disso, espera-se que a nova técnica seja amplamente utilizada em experimentos que abordem o mecanismo da ação da progerina.
Rodriguez S, Coppedè F, Sagelius H e Erikson M. “Expressão aumentada da transcrição de laminados A truncados da síndrome da progeria de Hutchinson-Gilford durante o envelhecimento celular”. Revista Européia de Genética Humana (2009), 1-10.
Agosto e outubro 2008: Progeria é reversível? Duas publicações recentes mostram que FTIs e terapia genética podem fazer exatamente isso!
Dois estudos separados mostram que a Progéria é reversível no sistema cardiovascular e na pele de modelos de ratos. Os experimentos foram significativos em não tratar os camundongos até que eles expressassem os sintomas da Progéria, enquanto a maioria dos estudos anteriores começaram o tratamento antes que a Progéria fosse aparente. A produção de progerina (a proteína prejudicial produzida a partir do gene Progeria) foi inibida pelo tratamento com um inibidor da farnesil transferase (FTI) ou pelo desligamento do gene. Em ambos os casos, os ratos voltaram às condições normais ou quase normais. Estas observações fornecem evidências encorajadoras para o ensaio clínico atual de FTIs para Progéria.
Em uma impressionante demonstração de progresso com o medicamento FTI - agora sendo usado no Primeiro Estudo Clínico sobre Medicamentos da Progeria - A equipe de pesquisa do Dr. Francis Collins no National Institutes of Health * descobriu que os FTIs preveniram e até reverteram o efeito mais devastador da Progéria em camundongos: doenças cardiovasculares. * “Ficamos surpresos que [a droga] funcionou tão bem”, diz Francis Collins, um geneticista e ex-diretor do Instituto Nacional de Pesquisa do Genoma Humano, que foi o autor sênior da equipe de pesquisa que identificou a mutação do gene da Progéria em 2003. “Esta droga não apenas evitou que esses ratos desenvolvessem doenças cardiovasculares, como reverteu os danos em ratos que já tinham doença. ”
Os camundongos Progeria desenvolvem doenças cardíacas que espelham as de crianças com Progeria. Os autores descobriram que o FTI foi capaz de impedir o desenvolvimento de doenças cardíacas em algum grau quando os ratos estavam em tratamento a partir do momento em que foram desmamados e reverter parcialmente a doença estabelecida quando os ratos foram tratados a partir dos meses 9 de idade. "Uma das coisas marcantes da minha perspectiva foi a capacidade de reverter a doença", disse Collins, o que é crítico, uma vez que a Progéria geralmente não é diagnosticada no nascimento, mas apenas quando as crianças começam a apresentar sintomas, quando parte do dano já foi causado. feito.
"Se esses medicamentos tiverem efeitos semelhantes em crianças, isso poderá marcar um grande avanço no tratamento dessa doença devastadora", disse o Dr. Nabel, do NHLBI, co-autor do estudo. "Além disso, esses achados lançam luz sobre o papel potencial dos medicamentos FTI no tratamento de outras formas de doença arterial coronariana".
Veja o artigo em Scientific American, “Nova esperança para a Progéria: medicamento para doenças raras do envelhecimento”, em https://www.sciam.com/article.cfm?id=new-hope-for-progeria-drug-for-rare-aging-disease e o press release do NIH em https://www.nih.gov/news/health/oct2008/nhgri-06.htm
* Capell et ai. al "Um inibidor da farnesiltransferase evita o início e a progressão tardia da doença cardiovascular em um modelo de camundongo Progeria". Anais da Academia Nacional de Ciências, Vol. 105, não. 41, 15902-15907 (outubro de 14, 2008)
Em um segundo estudo publicado online no Journal of Medical Genetics **, a equipe de pesquisa da Dra. Maria Eriksson no Karolinska Institutet, na Suécia, criou outro modelo de rato de Progéria com anormalidades na pele e nos dentes. Os ratos são geneticamente modificados para que a mutação da Progéria possa ser desligada a qualquer momento. Assim que a doença se tornou aparente, o gene da Progéria foi desativado. Após 13 semanas, a pele estava quase indistinguível da pele normal. Este estudo mostra que nesses tecidos a expressão da mutação da Progéria não causa danos irreversíveis e que a reversão da doença é possível, o que promete o tratamento da Progéria.
** Eriksson, et. al., "Fenótipo reversível em um modelo de camundongo da síndrome de Hutchinson-Gilford Progeria". J. Med. Genet publicado online 15 Ago 2008; doi: 10.1136 / jmg.2008.060772
Para adquirir este artigo, acesse: https://jmg.bmj.com/cgi/rapidpdf/jmg.2008.060772v1
Mais evidências da relação entre Progéria e envelhecimento normal e doenças cardíacas
Esses empolgantes estudos de Capell e Eriksson mostram que, além da Progéria, esses resultados têm o potencial de beneficiar todos os pacientes com doença cardiovascular. Os pesquisadores descobriram que a proteína tóxica responsável pela Progéria é realmente produzida em níveis baixos em todos os seres humanos, possivelmente se acumulando à medida que envelhecemos. Assim, estudando essas crianças raras, podemos aprofundar nossa compreensão de um importante mecanismo do envelhecimento humano - e, talvez, encontrar novas maneiras de retardar o processo.

