Ensaios clínicos e
Programa de acesso gerenciado
Ensaios clínicos de medicamentos Progeria: Histórico
 Os ensaios clínicos de medicamentos para Progeria são a melhor esperança para crianças com Progeria, testando tratamentos potenciais que podem permitir que vivam vidas mais longas e saudáveis. Esses ensaios são o ápice de anos de pesquisa focada em qual medicamento ou combinação de medicamentos tratará e curará as crianças.
Os ensaios clínicos de medicamentos para Progeria são a melhor esperança para crianças com Progeria, testando tratamentos potenciais que podem permitir que vivam vidas mais longas e saudáveis. Esses ensaios são o ápice de anos de pesquisa focada em qual medicamento ou combinação de medicamentos tratará e curará as crianças.
Desde 1999, quando fundamos a PRF e não havia recursos para essas crianças, nós voamos da obscuridade total, para a descoberta de genes, para os primeiros ensaios clínicos de Progeria, para o primeiro tratamento aprovado pela FDA, chamado lonafarnib – tudo em um ritmo praticamente inédito na comunidade científica. E enquanto ajudamos esse punhado de crianças, a conexão da Progeria com doenças cardíacas comuns e envelhecimento tem implicações tremendas para todos nós.
Quais são os próximos tratamentos e curas?
Iniciando um novo ensaio clínico de medicamentos: as inscrições para o ensaio com progerinina já começaram!
A PRF, em colaboração com o patrocinador do estudo sediado na Coreia, PRG Science & Technology (PRG S&T), iniciou a inscrição para um novo ensaio clínico com um medicamento chamado Progerinina. Evidências laboratoriais mostram que esse medicamento, quando tomado em combinação com lonafarnibe, pode ser mais eficaz do que lonafarnibe sozinho. A PRF financiou o trabalho laboratorial que levou à formação da PRG S&T e seu desenvolvimento da Progerinina. O trabalho pré-teste começou no Hospital Infantil de Boston, na expectativa de trazer crianças de todo o mundo para se inscreverem neste ensaio nos próximos meses. Estamos super animados em começar um novo ensaio com um medicamento tão promissor e ansiosos para compartilhar mais detalhes com você assim que estiverem disponíveis.
Entre em contato com Shelby Phillips para saber mais sobre o julgamento.
E-mail: sphillips@progeriaresearch.org
WhatsApp, Telegrama, WeChat: 1-978-876-2407
Telefone do escritório: 978-548-5308
A cofundadora e diretora executiva da PRF, Audrey Gordon, fecha o acordo em junho com o Dr. Bum-Joon Park da PRG S&T para prosseguir com o trabalho pré-julgamento.
Terapia de RNA: Administração de Medicamentos Estudo de viabilidade concluído!
A PRF deu os primeiros passos envolvendo pacientes em direção a um ensaio clínico em terapia de RNA – MUITO emocionante!
Contexto: Em janeiro de 2021, relatamos descobertas revolucionárias em terapêuticas de RNA, onde esta terapia inibiu a produção de RNA que codifica a proteína causadora da doença Progeria, progerina. O estudo*, liderado pelo Dr. Francis Collins, Conselheiro Científico da Casa Branca e ex-diretor do Instituto Nacional de Saúde (NIH), revelou que camundongos com Progeria tratados com um medicamento chamado SRP-2001 reduziu a expressão prejudicial do mRNA e da proteína da progerina nos vasos sanguíneos, assim como em outros tecidos. Os vasos sanguíneos eram mais fortes e os ratos mostraram uma aumento da sobrevivência de mais de 60% comparado a ratos não tratados. Assim, o trabalho com esta terapia promissora continuou, e nós tomamos a próximo passo com um Estudo de viabilidade do seguinte modo:
Normalmente, os terapêuticos de RNA são líquidos que são injetados intravenosamente (diretamente na veia). No entanto, aqueles com Progeria não seriam capazes de tolerar a administração intravenosa da dosagem diária necessária. Assim, a PRF desenvolveu um sistema de administração subcutânea onde o líquido pode ser injetado com uma pequena agulha sob a pele. Um estudo de 6 meses no BCH foi concluído para determinar a viabilidade desta abordagem de entrega para aqueles com Progéria. A equipe testou se a administração de uma solução salina pode ser confortavelmente injetada por via subcutânea e qual sistema de injeção e local seriam mais confortáveis. Uma vez que os dados deste estudo sejam analisados, estaremos um passo mais perto de um ensaio clínico em terapia genética!
*Erdos, MR, Cabral, WA, Tavarez, UL et al. Uma abordagem terapêutica antisense direcionada para a síndrome de progeria de Hutchinson–Gilford. NatMédico (2021).
O que está acontecendo HOJE com os ensaios clínicos da Progéria?
O ensaio mais recente envolveu 2 medicamentos: lonafarnibe e um novo medicamento, everolimo. A fase 1, para determinar a dosagem segura e apropriada de everolimus, começou em abril de 2016 e foi concluída com sucesso em junho de 2017. A fase 2, que testou a eficácia da combinação de dois medicamentos, começou em julho de 2017 e foi concluída em abril de 2022. Sessenta crianças de 27 países foram inscritas nesta fase de dois medicamentos!
Everolimus é uma forma do medicamento rapamicina; everolimus poderia ser administrado mais facilmente a crianças com Progeria porque requer menos coletas de sangue para medir os níveis do medicamento. Enquanto lonafarnib pode bloquear o desenvolvimento da progerina tóxica, a rapamicina parece permitir que as células limpem a progerina mais rapidamente. Assim, com a rapamicina mirando uma via diferente da lonafarnib, a combinação pode provar ser um "golpe duplo" para a Progeria - esperançosamente um tratamento melhor do que lonafarnib por si só.
Agora entramos em um período de análise de dados e esperamos eventualmente publicar os resultados em um periódico científico revisado por pares. Enquanto isso, os participantes do teste foram transferidos para a extensão de monoterapia do teste ou para outro programa de acesso. Por qualquer um dos caminhos, os participantes continuam a receber lonafarnib, o padrão atual de tratamento.
Histórico de julgamentos em resumo
Até o momento, a PRF financiou e co-coordenou quatro ensaios clínicos. A PRF é e sempre foi responsável por todas as despesas do teste, incluindo testes, viagens, alimentação, hospedagem, tradutores e equipe. Cada novo teste é mais caro que o anterior, pois mais crianças se inscrevem para ter uma chance de vidas mais longas e saudáveis.
Detalhes sobre os ensaios anteriores
#1 envolveu um único medicamento, lonafarnib, começou em 2007 e provou ser bem-sucedido. Leia tudo sobre a descoberta histórica do tratamento aqui.
#2, a parte de Viabilidade do “Triple Trial” envolveu 3 medicamentos: lonafarnib, pravastatina e zoledronato. Este “mini trial” de fase 1 de 1 mês ocorreu em março de 2009 para determinar se adicionar mais 2 medicamentos ao regime de lonafarnib era seguro para prosseguir com uma população maior (o que era).
#3, o “Triple Trial,” foi uma continuação do Feasibility trial, e foi um estudo de fase 2, que começou em agosto de 2009. Seu protocolo mudou ao longo de cinco anos, voltando para apenas lonafarnib e reabrindo a inscrição para que mais crianças pudessem participar. Leia mais aqui.
#4 é o ensaio de dois fármacos, lonafarnib e everolimus. A fase 1, para determinar a dosagem segura e apropriada de everolimus, começou em abril de 2016 e foi concluída com sucesso em junho de 2017. A fase 2, que testou a eficácia da combinação de dois fármacos, começou em julho de 2017 e foi concluída em abril de 2022. A extensão de monoterapia deste ensaio continua hoje.
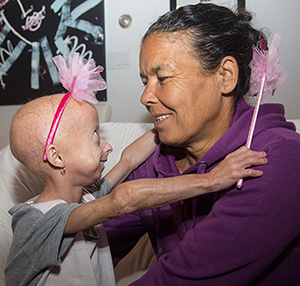
7 de maio de 2007: O início do primeiro ensaio clínico do medicamento Progeria marca um momento histórico na história da pesquisa sobre Progeria!
Em 2006, os pesquisadores identificaram um potencial tratamento medicamentoso para crianças com Progéria, chamados FTIs. Pela primeira vez, tínhamos diante de nós um possível tratamento para crianças com Progéria. Tempos emocionantes! O teste clínico do medicamento Progeria começou em 7 de maio de 2007 com duas crianças – Meghan e Megan – chegando ao Hospital Infantil de Boston em Boston, MA para sua primeira de sete visitas ao longo de um período de 2 anos. Nesta primeira visita, elas fizeram testes extensivos e suas primeiras doses do medicamento. Uma média de duas famílias viajou para Boston a cada semana depois disso, até dezembro de 2009, seguido por um período de tempo em que a equipe do teste analisou os muitos milhares de elementos de dados (cada criança passou por mais de 100 testes por visita!) e buscou a publicação dos resultados.
“Não conheço nenhuma outra doença genética rara que tenha passado da descoberta genética para o ensaio clínico em menos de quatro anos – um testemunho fenomenal do trabalho árduo da The Progeria Research Foundation.”
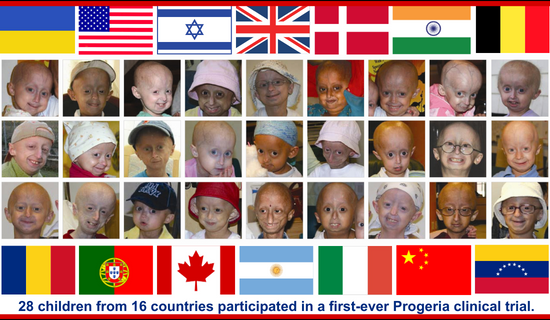
Vinte e oito (28) crianças de dezesseis países participaram, com idades entre 3 e 15 anos. As crianças retornavam ao Hospital Infantil de Boston a cada quatro meses, para testes e para receber novos suprimentos de medicamentos, e ficavam em Boston por 4 a 8 dias em cada visita. Enquanto estavam em casa, seus médicos mantinham uma vigilância rigorosa sobre as crianças e enviavam relatórios periódicos de saúde para a equipe de pesquisa de Boston. Durante a duração do teste, uma média de 2 crianças por semana viajavam para Boston para participar.
Quem, onde, quando, como e quanto…
Os três primeiros ensaios clínicos foram liderados por Mark Kieran MD, PhD, Diretor, Pediatric Medical Neuro-Oncology, Dana-Farber Cancer Institute e Children's Hospital Boston; Professor Assistente, Departamentos de Pediatria e Hematologia/Oncologia, Harvard Medical School. O Dr. Kieran é um oncologista pediátrico com ampla experiência com o medicamento em estudo (farnesiltransferase, ou FTI) em crianças. Em 2017, ele deixou seu cargo na Dana Farber para trabalhar no setor privado. Os copresidentes foram Monica Kleinman, MD, Diretora da Unidade de Terapia Intensiva Médico-Cirúrgica, Associada Sênior em Medicina de Cuidados Críticos no BCH, Professora Assistente na Harvard Medical School; e Leslie Gordon, MD, PhD, Diretora Médica da PRF, Palestrante no BCH e Harvard Medical School, Professora de Pediatria no Hasbro Children's Hospital e Brown University em Providence, RI. O Dr. Kleinman assumiu o papel principal de Pesquisador Principal.
Os ensaios clínicos são um esforço colaborativo, envolvendo médicos do Hospital Infantil de Boston, do Instituto de Câncer Dana-Farber e do Hospital Brigham and Women's, todas as instituições da Universidade de Harvard. Além disso, médicos e cientistas da The Warren Alpert Medical School da Brown University e do NIH ajudaram a tornar este primeiro e os outros testes um sucesso.
Como chegamos a esse ponto?
Em 2003, a equipe de pesquisa colaborativa da Progeria Research Foundation descobriu o gene Progeria. Esta descoberta não só levou a uma maior compreensão da Progeria, mas os cientistas agora sabem que estudar a Progeria pode nos ajudar a aprender mais sobre doenças cardíacas e o processo normal de envelhecimento que afeta a todos nós. Desde a descoberta do gene, o apoio de pesquisadores, clínicos, famílias de crianças com Progeria e pessoas como VOCÊ nos levaram a outra encruzilhada na busca por um tratamento. Os pesquisadores começaram um estudo intenso desta proteína inimiga chamada progerina, e em 2006 eles identificaram um potencial tratamento medicamentoso para crianças com Progéria, chamado inibidores de farnesiltransferase (FTIs), e conduziram estudos no laboratório que apoiaram um teste humano com o medicamento. O FTI escolhido foi inicialmente fornecido pela Merck e chamado lonafarnib. Clique aqui para mais detalhes sobre a pesquisa.
Por que os pesquisadores pensaram que esse medicamento funcionaria na Progéria?
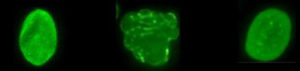
Célula normal, célula de Progéria, célula de Progéria após tratamento com FTI.
A proteína que acreditamos ser responsável pela Progeria é chamada progerina. Para bloquear a função celular normal e causar Progeria, uma molécula chamada “grupo farnesil” deve ser anexada à proteína progerina. Os FTIs agem bloqueando (inibindo) a ligação do grupo farnesil à progerina. Então, se o medicamento FTI pode bloquear essa ligação do grupo farnesil em crianças com Progeria, então a progerina pode ser “paralisada” e a Progeria melhorada. Clique aqui para mais informações sobre FTIs.
Como a PRF financiou o teste?
Graças ao apoio de milhares, conseguimos levantar todos os fundos necessários para cobrir os custos do teste. Nossa sincera gratidão vai para todos que contribuíram com seu “tempo, talentos e tesouro” para tornar essa conquista incrível possível e, claro, para todas as famílias corajosas que participaram.
O FTI lonafarnib é agora um tratamento comprovado para a Progeria.
Em 2012, os resultados do estudo foram publicados, demonstrando que cada criança experimentou melhora em uma ou mais áreas, incluindo o sistema cardiovascular vital. Em maio de 2014, um estudo mostrou que um ou mais de 3 medicamentos – incluindo lonafarnib – sendo testados em ensaios clínicos financiados pela PRF prolongaram a vida útil; não estava claro qual medicamento teve esse impacto positivo de mudança de vida. No entanto, em abril de 2018, um estudo publicado em O Jornal da Associação Médica Americana (JAMA) relataram que o lonafarnib sozinho prolongou a sobrevivência de crianças com Progéria em pelo menos 1,6 anos. Clique aqui para detalhes sobre o estudo histórico de descoberta do tratamento de 2012, aqui para obter detalhes sobre as conclusões de 2014 e aqui para detalhes sobre o estudo de 2018.
“TODOS foram tão maravilhosos. Para nós, vocês são TODOS ENVIADOS DE DEUS e APRECIAMOS tudo o que vocês fazem por esses anjinhos. Nossa família está tão emocionada com a animação e todos os tipos de emoções com a viagem de Adalia para Boston neste fim de semana, que não consigo nem começar a digitar as palavras de como estamos nos sentindo.”
“Este novo medicamento para Zach nos dá uma esperança renovada de que seu coração ficará mais forte, seu sorriso ficará mais brilhante e sua vida será mais longa. Este novo teste de medicamento é uma resposta às nossas orações. Obrigado a todos os envolvidos com a PRF que fizeram isso acontecer... os médicos, os pesquisadores e a equipe. Vocês são nossos heróis!”
“Em nome de Cam e da nossa família, muito obrigado a todos da PRF por tudo o que fizeram! Estaríamos perdidos em um mundo de confusão e tristeza sem vocês. Em vez disso, vivemos em um mundo de esperança e propósito. Obrigado de novo e de novo! Com muito amor e respeito.”

Sempre avançando: o teste triplo de medicamentos para progeria começa em agosto de 2009
Resumo:
Pesquisadores identificaram dois medicamentos adicionais que, quando usados em combinação com o medicamento FTI atual sendo testado (lonafarnib), podem fornecer um tratamento ainda mais eficaz para crianças com Progeria do que os FTIs sozinhos. Pravastatina e zoledronato foram adicionados ao tratamento atual lonafarnib. Este teste muito maior incluiu 45 crianças de 24 países diferentes!
Estratégia:
Todos os três medicamentos têm como alvo diferentes pontos ao longo do caminho que leva à produção da progerina causadora da doença. Em empolgantes estudos laboratoriais apresentados pelo Dr. Carlos Lopez-Otin da Espanha no Workshop Científico da Progeria Research Foundation de 2007, os dois novos medicamentos melhoraram a doença em células de Progeria e prolongaram a vida útil em modelos de camundongos de Progeria.
Meta:
Se os três medicamentos administrados neste teste puderem bloquear efetivamente essa ligação do grupo farnesil, então a progerina pode ser “paralisada” e a Progeria pode ser melhorada ainda mais do que com o lonafarnib sozinho. A esperança é que os medicamentos funcionem como parceiros, para se complementarem, de modo que a proteína progerina seja mais afetada pela combinação dos três medicamentos.
O teste de viabilidade:
A equipe conduziu um mini-teste para 5 crianças com Progéria. O curto teste de “viabilidade” de um mês perguntou se a combinação de três medicamentos seria bem tolerada, antes de embarcar em um teste internacional maior. Os efeitos colaterais foram aceitáveis, e a equipe seguiu em frente para o teste de eficácia maior.
O ensaio de eficácia:
45 crianças inscritas neste ensaio, de 24 países, falando 17 idiomas. Isso inclui crianças que participaram do ensaio somente FTI, os participantes do ensaio de viabilidade e outras crianças que eram muito jovens para participar do primeiro ensaio ou crianças que descobrimos durante o primeiro ensaio clínico (após o término da inscrição). As crianças inscritas no ensaio somente FTI tiveram a oportunidade de se inscrever no ensaio triplo quando participaram de sua última visita para o ensaio atual. Isso permitiu que essas crianças continuassem tomando FTI sem nenhuma dose esquecida.
Medicamentos experimentais em resumo
Pravastatina (comercializado como Pravachol ou Selektine) é um membro da classe de medicamentos das estatinas. É geralmente usado para reduzir o colesterol e prevenir doenças cardiovasculares.
Ácido zoledrônico é um bisfosfonato, geralmente usado como um medicamento ósseo para melhorar a osteoporose e para prevenir fraturas esqueléticas em pessoas que sofrem de alguns tipos de câncer.
Lonafarnibe é um FTI (Inibidor da farnesiltransferase), um medicamento que pode reverter uma anormalidade nas células de Progeria em laboratório e melhorou a doença em camundongos com Progeria.
Todos os três medicamentos bloqueiam a produção da molécula farnesil, necessária para que a progerina crie a doença na Progéria.
* “Tratamento combinado com estatinas e aminobifosfonatos prolonga a longevidade em um modelo murino de envelhecimento humano prematuro", de Ignacio Varela, Sandrine Pereira, Alejandro P. Ugalde, Claire L. Navarro, Marıa F. Suarez, Pierre Cau, Juan Cadinanos, Fernando G. Osorio, Nicolas Foray, Juan Cobo, Felix de Carlos, Nicolas Levy, Jose Deputados Freije e Carlos Lopez-Otan. Medicina Natural, 2008. 14(7): p. 767-72.
Em julho um estudar ** foi publicado que não mostrou nenhuma melhora significativa encontrada além da terapia única com lonafarnibe. **Gordon, et. al., Ensaio clínico de inibidores de farnesilação de proteínas lonafarnib, pravastatina e ácido zoledrônico em crianças com síndrome de Hutchinson-Gilford Progeria, Circulação, 10.1161/CIRCULAÇÃOAHA.116.022188
No entanto, o “Triple Trial” foi estendido além do seu prazo original de 2-3 anos e expandido para incluir até 80 crianças, para que cada criança pudesse ter acesso apenas ao lonafarnib porque sabemos que ele está ajudando as crianças. Normalmente, os ensaios clínicos seguem seu curso e os pacientes são retirados de todos os medicamentos até a aprovação do FDA; isso pode levar anos. O PRF garantiu que as crianças continuassem a tomar o único tratamento conhecido, enquanto elas e seus parceiros de pesquisa continuam explorando opções de tratamento adicionais (como o everolimus que está sendo testado atualmente).
A adição de um mais novo Medicamento: Everolimus
Everolimus é uma forma do medicamento rapamicina; everolimus poderia ser administrado mais facilmente a crianças com Progeria porque requer menos coletas de sangue para medir os níveis do medicamento. Enquanto lonafarnib pode bloquear o desenvolvimento da progerina tóxica, a rapamicina parece permitir que as células limpem a progerina mais rapidamente. Assim, com a rapamicina mirando uma via diferente da lonafarnib, a combinação pode provar ser um "golpe duplo" para a Progeria - esperançosamente um tratamento melhor do que lonafarnib por si só.
A ciência por trás da adição deste segundo medicamento
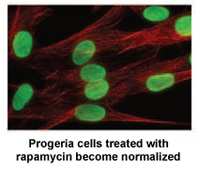
Rapamicina é um medicamento aprovado pela FDA que já demonstrou prolongar a vida de modelos de camundongos sem Progeria. Um estudo* realizado por pesquisadores do NIH em Bethesda, MD e do Massachusetts General Hospital em Boston demonstra que a rapamicina diminui a quantidade da proteína progerina causadora da doença em 50%, melhora o formato nuclear anormal e prolonga a vida útil das células de Progeria em laboratório.
A rapamicina é conhecida por suas propriedades antienvelhecimento em camundongos. Essas descobertas são parte de uma lista crescente de estudos que ajudam a validar a teoria de que encontrar a cura para a Progeria também pode beneficiar toda a população idosa.
* K. Cao, J. J. Graziotto, C. D. Blair, J. R. Mazzulli, M. R. Erdos, D. Krainc, F. S. Collins, “Rapamycin Reverses Cellular Fenótipos e Aumenta a Eliminação de Proteínas Mutantes em Células da Síndrome de Hutchinson-Gilford Progeria.” Sci. Transl. Med. 3, 89ra58 (2011).
A Progeria Research Foundation forneceu células para este projeto a partir do Banco de células e tecidos PRF e ajudou a financiar a pesquisa por meio de nosso programa de bolsas – mais uma prova de que os programas relacionados à pesquisa da PRF são essenciais para os avanços em direção à cura.
Este teste de 2 medicamentos foi um esforço colaborativo que se baseou no conhecimento obtido nos testes clínicos anteriores da PRF. As crianças foram vistas virtualmente pela mesma equipe de médicos do Boston Children's Hospital e do Brigham and Women's Hospital, todos os quais agora têm experiência mundialmente reconhecida em Progeria, bem como nos medicamentos envolvidos.
Sessenta crianças de 27 países foram inscritas nesta fase de dois medicamentos. Dados da parte de dois medicamentos do teste estão sendo analisados e os resultados estão sendo formulados e escritos para publicação em um periódico científico revisado por pares.
Nossa busca pela cura continua…
Nosso trabalho com terapias genéticas está avançando a todo vapor! Estudos de terapia de RNA e edição de genes de DNA mostraram uma vasta melhora na expectativa de vida dos camundongos Progeria. A PRF continua a investir fundos substanciais no seu desenvolvimento, com a esperança de que estes esforços de investigação levar a ensaios clínicos e, finalmente, à cura.
Estas terapias de ponta têm enorme potencial! Com a sua ajuda, a PRF pode continuar avançando o mais rápido possível em direção aos tratamentos mais eficazes e à cura.

