Progeria 101 / Perguntas frequentes
O que é Progéria?
Síndrome de Hutchinson-Gilford Progeria (HGPS ou Progeria) é uma doença ultra-rara, fatal, de “envelhecimento rápido”. Seu nome é derivado do grego e significa “prematuramente velho”. O tipo clássico é a Síndrome de Hutchinson-Gilford Progeria, que recebeu o nome dos médicos que a descreveram pela primeira vez: em 1886 pelo Dr. Jonathan Hutchinson, e em 1897 pelo Dr. Hastings Gilford.[1]
Quão comum é a Progéria?
A Progeria ocorre em aproximadamente 1 em 4 a 8 milhões de recém-nascidos, afetando ambos os sexos igualmente e todas as raças. Um em 18 a 20 milhões de indivíduos vivos tem Progeria clássica, e estima-se que existam 400 crianças vivendo com Progeria no mundo todo. Desde que a Progeria Research Foundation (PRF) foi criada em 1999, encontramos e ajudamos crianças com Progeria vivendo em 72 países e todos os continentes.[2]
Quais são as características do Progeria?
Embora geralmente nasçam com aparência saudável, a maioria das crianças com Progeria começa a apresentar características de Progeria no primeiro ano de vida. Às vezes, os primeiros sinais de Progeria são rigidez ou protuberância da pele na área abdominal e/ou coxa, e falha no desenvolvimento (caindo bem abaixo da curva de crescimento pediátrico). Outros sinais precoces de Progeria incluem perda de gordura corporal e cabelo, alterações na pele, contraturas articulares e alguns achados reveladores de raios-X. As crianças atingem uma altura máxima média de 125 cm (49,21 polegadas) e 25 kg (55,12 libras). As crianças têm uma aparência notavelmente semelhante, apesar das diferentes origens étnicas. À medida que as crianças envelhecem, elas desenvolvem aterosclerose acelerada e doença cardiovascular (cardíaca). Esta é a mesma aterosclerose que geralmente afeta pessoas na faixa dos 60 anos ou mais, mas afeta aquelas com Progeria muito mais cedo e em um ritmo rápido.
Qual é a causa da Progéria?
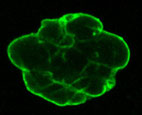
Núcleo celular de Progeria
Um grupo de cientistas líderes do Consórcio de Genética da PRF, incluindo o Dr. Francis Collins, então Diretor do Instituto Nacional de Pesquisa do Genoma Humano, isolou o gene Progeria. Em abril de 2003, o Consórcio relatou essa descoberta no principal periódico científico Natureza.[3]
“Isolando o Progéria gene é uma grande conquista para a comunidade de pesquisa médica”, disse o Dr. Francis Collins, autor sênior do relatório sobre a mutação do gene Progeria. “A descoberta não só dá esperança às crianças e famílias afetadas pela Progéria, mas também pode lançar luz sobre o fenômeno do envelhecimento e das doenças cardiovasculares.”
A descoberta do gene Progeria revelou que a Progeria é causada por uma mutação no gene chamado LMNA (pronuncia-se “lamin-A”). O LMNA gene produz a proteína lamin A, que faz parte do andaime estrutural que mantém o núcleo de uma célula unido e ajuda a manter as células saudáveis. A proteína lamin A anormal que causa Progeria é chamada progerina. A progerina torna as células instáveis, o que leva ao processo de envelhecimento prematuro e doenças na Progéria.
O que a Progéria tem a ver com o envelhecimento?
Talvez a pista mais emocionante sobre o processo de envelhecimento seja a descoberta de que a proteína progerina está presente em concentrações crescentes tanto na Progeria quanto nas células normais à medida que envelhecemos. Nossos corpos acumulam progerina dentro das células do sistema cardiovascular a uma taxa de cerca de 3% a cada ano (muito menor do que em crianças e adultos jovens com Progeria). Assim, entender a Progeria promete novos caminhos para entender o processo natural de envelhecimento.
Crianças com Progéria são geneticamente predispostas a doenças cardíacas prematuras e progressivas. A morte ocorre quase exclusivamente devido à disseminação doença cardíaca, a principal causa de morte no mundo.[4] Assim, há claramente uma tremenda necessidade de pesquisa em Progeria. Encontrar uma cura para Progeria não só ajudará aqueles com Progeria, mas também pode fornecer pistas para o tratamento de milhões de adultos com doenças cardíacas e derrames associado ao processo natural de envelhecimento.
A Progéria é transmitida de pais para filhos?
HGPS geralmente não é transmitido nas famílias. A alteração genética é quase sempre uma ocorrência casual que é extremamente rara. Crianças com outros tipos de síndromes "progeroides" que não são HGPS podem ter doenças que são transmitidas nas famílias. No entanto, HGPS é uma mutação "esporádica autossômica dominante" - esporádica porque é uma nova alteração naquela família e dominante porque apenas uma cópia do gene precisa ser alterada para ter a síndrome. Para pais que nunca tiveram um filho com Progeria, as chances são de uma em 4 a 8 milhões. Mas para pais que já tiveram um filho com Progeria, as chances de isso acontecer novamente com esses pais são muito maiores - cerca de 2-3%. Por que o aumento? Isso se deve a uma condição chamada "mosaicismo", onde um dos pais tem a mutação genética para Progeria em uma pequena proporção de suas células, mas não tem Progeria. O teste pré-natal durante a gravidez está disponível para procurar a LMNA alteração genética que causa HGPS no feto.
Como a Progéria é diagnosticada?
Devido à descoberta histórica do gene Progeria, temos uma forma definitiva e científica de diagnosticar as crianças. Isso resulta em diagnósticos mais precisos e precoces para que possam receber o tratamento adequado. A Progeria Research Foundation tem uma Programa de Testes de Diagnóstico que analisa a alteração genética específica, ou mutação, no gene Progeria que leva à HGPS. Após uma avaliação clínica inicial (analisando a aparência da criança e os registros médicos), uma amostra do sangue da criança é testada para Progeria. Testes genéticos também estão disponíveis em algumas instalações de diagnóstico genético. Aconselhamento genético de acompanhamento é sempre recomendado.
Existe tratamento para Progéria?
Sim! A história foi feita em Setembro de 2012, quando os resultados do primeiro ensaio clínico do medicamento Progeria demonstraram que o lonafarnib, um inibidor da farnesiltransferase (ou FTI), era um tratamento eficaz para a Progeria[5]. Todos os participantes do estudo apresentaram melhorias significativas no ganho de peso, na estrutura óssea e, mais importante, no sistema cardiovascular.
Dois estudos subsequentes, um de 2018 publicado no Jornal da Associação Médica Americana (JAMA)[6], e um de 2023 publicado em Circulação[7], demonstrou que o lonafarnib ajudou a prolongar a sobrevivência em crianças com Progéria.
O 2012 e 2018 estudos levaram ao extraordinário 2020 Aprovação da Food & Drug Administration (FDA) dos EUA para lonafarnib, agora com a marca 'Zokinvy', como o primeiro tratamento para Progeria. Um marco crítico na missão da PRF, essa aprovação foi o ápice de 13 anos de pesquisa clínica envolvendo quatro ensaios clínicos, trazendo 96 crianças de 37 países para tratamento em Boston.
Com esse marco, a Progeria se juntou às fileiras de menos de 5% de doenças raras com um tratamento aprovado pela FDA.
Logo após a aprovação do lonafarnibe pela FDA, a Agência Europeia de Medicamentos (EMA) aprovou o lonafarnibe para uso na Europa em julho de 2022, seguida pelo Ministério da Saúde, Trabalho e Bem-Estar do Japão (MHLW) em janeiro de 2024.
Sem lonafarnib, as crianças morrem de aterosclerose (insuficiência cardíaca ou derrames) com uma idade média de 14,5 anos [6] . Com o tratamento de longo prazo com lonafarnib, a saúde cardiovascular é significativamente melhorada e a esperança de vida aumentou em média 4,5 anos7. Isso é mais de 30% de aumento na expectativa de vida média, de 14,5 anos para quase 20 anos de idade!
Com as crianças vivendo mais devido à terapia com lonafarnib, os médicos estão vendo a estenose aórtica (estreitamento de uma válvula cardíaca crítica) como um problema em crianças mais velhas e adultos jovens com Progeria que pode ser passível de cirurgia para salvar vidas. Em alguns casos, a cirurgia para inserir novas válvulas cardíacas ou abrir vasos sanguíneos que irrigam o coração (stents) ajudou a melhorar a saúde de pacientes em estágios posteriores da doença[8].
Quais são os desenvolvimentos mais recentes na pesquisa sobre Progéria?
A PRF está fortemente envolvida no desenvolvimento de três outras vias terapêuticas, cada um dos quais mostrou níveis variados de aumento da expectativa de vida quando estudado em modelos de camundongos com Progeria – de 50% a um surpreendente 140%! Nossos objetivos são descobrir novos tratamentos que funcionem ainda melhor do que o lonafarnib sozinho e, eventualmente, curar a Progeria corrigindo a mutação genética. Estamos atacando a doença nos níveis de proteína, RNA e DNA.
- Edição de base de DNA:Este caminho visa corrigir permanentemente a mutação do gene Progeria no nível do DNA.
Em Janeiro de 2021, a revista científica Natureza publicou resultados inovadores demonstrando que a edição genética em um modelo murino de Progeria corrigiu a mutação de Progeria em muitas células, melhorou vários sintomas importantes da doença e aumento da expectativa de vida em camundongos por 140%[9]. Estudos pré-clínicos adicionais são necessários para investigar esses resultados, os quais esperamos que um dia levem a um ensaio clínico.
“Ver essa resposta dramática em nosso modelo de camundongo Progeria é um dos desenvolvimentos terapêuticos mais empolgantes dos quais participei em 40 anos como médico-cientista”, disse Francis Collins, MD, PhD.
- RNA Terapêutica:Esta via visa interromper a produção de progerina corrigindo a mutação genética no nível do RNA.
Em Março de 2021, PRF contribuiu para dois estudos inovadores muito interessantes sobre o uso de terapêuticas de RNA, ambos os quais tentam bloquear a capacidade do corpo de produzir progerina no nível de RNA. Um estudo mostrou que tratar camundongos Progeria com um medicamento chamado SRP2001 reduziu a expressão prejudicial de mRNA e proteína de progerina na aorta, a principal artéria do corpo, bem como em outros tecidos. No final do estudo, os camundongos demonstraram uma aumento da sobrevivência de 62%[10].
O outro estudo mostrou uma redução de 90 – 95% do RNA tóxico produtor de progerina em diferentes tecidos após o tratamento com um medicamento chamado LB143. A redução da proteína progerina foi mais eficaz no fígado, com melhorias adicionais no coração e na aorta.[11]Essa correção genética é temporária, portanto, é necessário tratamento contínuo para manter a correção. - Pequena Molécula (Drogas):Esta via visa reduzir o nível da proteína tóxica progerina que causa a Progéria.
Um medicamento chamado progerinina mostrou-se muito promissor. Em um modelo de camundongo Progeria, a progerinina aumentou o peso corporal e estendeu a expectativa de vida em 10 semanas, um avanço substancial, comparado com a extensão da expectativa de vida de duas semanas em camundongos tratados com lonafarnib.[12]O campo de pesquisa da Progeria está fazendo grandes avanços, crescendo continuamente em escopo e sofisticação à medida que a busca por tratamentos eficazes e a cura continua. Pesquisadores brilhantes e apaixonados estão liderando o campo para descobertas e novos tratamentos que ajudam crianças com Progeria a viver vidas mais longas e saudáveis, ao mesmo tempo em que impulsionam a descoberta em doenças cardíacas e envelhecimento. Além da exploração de novos caminhos para tratamentos e cura, em março de 2023, a PRF relatou descobertas sobre a descoberta de um biomarcador de Progeria, uma nova maneira de medir a progerina, a proteína tóxica que causa a Progeria. Um biomarcador tem uma capacidade de mudança de jogo para desbloquear a promessa de testes de medicamentos mais inteligentes e rápidos, e melhores tratamentos. Usando plasma sanguíneo para medir os níveis de progerina, os pesquisadores podem entender como os tratamentos estão afetando os participantes do teste clínico após um período de tempo mais curto e em vários pontos ao longo de cada teste clínico, em vez de depender de características clínicas subjetivas. Este teste pode otimizar o processo do teste clínico, fornecendo informações iniciais sobre a eficácia dos tratamentos que estão sendo testados, como uma introdução a outros testes clínicos, como ganho de peso, alterações dermatológicas, contratura e função articular, etc., todos os quais exigem muito mais tempo para se manifestar. Agora podemos entender os benefícios do tratamento já quatro meses após o início do tratamento, ou interromper um tratamento que pode não beneficiar o participante do teste, para evitar efeitos colaterais desnecessários.[13]
Como a PRF está promovendo a pesquisa em direção a uma cura futura e ajudando crianças com Progéria hoje?
 Fundação de Pesquisa Progeria financia pesquisa médica visando desenvolver tratamentos e a cura para a Progéria. A PRF também tem seu próprio Banco de Células e Tecidos que fornece os materiais biológicos que os pesquisadores precisam para conduzir seus experimentos. Além disso, a PRF tem uma Banco de dados médicos e de pesquisa – uma coleção centralizada de informações médicas de pacientes com Progeria no mundo todo. Os dados são rigorosamente analisados para nos ajudar a entender mais sobre a Progeria e elaborar recomendações de tratamento.
Fundação de Pesquisa Progeria financia pesquisa médica visando desenvolver tratamentos e a cura para a Progéria. A PRF também tem seu próprio Banco de Células e Tecidos que fornece os materiais biológicos que os pesquisadores precisam para conduzir seus experimentos. Além disso, a PRF tem uma Banco de dados médicos e de pesquisa – uma coleção centralizada de informações médicas de pacientes com Progeria no mundo todo. Os dados são rigorosamente analisados para nos ajudar a entender mais sobre a Progeria e elaborar recomendações de tratamento.
Para ajudar a responder a muitas perguntas sobre como cuidar de alguém com Progéria, a PRF publicou O Manual da Progéria para famílias e médicos. De fatos básicos de saúde a recomendações de cuidados diários e diretrizes de tratamento abrangentes, o manual fornece um recurso de suporte para ajudar a otimizar a qualidade de vida de pessoas com Progéria em todo o mundo. A edição mais recente do Manual está disponível em inglês, espanhol, japonês, português, italiano, árabe e chinês. O manual também estará disponível em outros idiomas.
A PRF também está conduzindo Ensaios clínicos de medicamentos Progeria que estão testando tratamentos potenciais e, até o momento, financiou e coordenou quatro ensaios clínicos. A PRF não mede esforços em nossa exploração de medicamentos promissores que nos aproximarão da cura.
O que você pode fazer para ajudar crianças com Progéria?
- Faça uma contribuição financeira. Doações são sempre necessárias para continuar o trabalho de salvar vidas da PRF. Nenhuma doação é muito pequena ou muito grande – cada dólar conta em nossa busca pela cura! Doações online são aceitas em Dar.
- Doe seu tempo. Os voluntários também são importantes para o sucesso da PRF. Organize um evento especial, como uma venda de bolos ou lavagem de carros; traduza documentos para as famílias; ajude com uma correspondência – encontraremos algo para você fazer que se encaixe na sua agenda, local e talentos! Visite nosso Envolva-se página para ver todas as maneiras como você pode ajudar.
- Saiba mais, divulgue e conecte-se. Quer saber mais sobre os diversos programas e serviços vitais que a PRF oferece às crianças e jovens adultos com Progéria? Confira nosso site em progeriaresearch.org
Você conhece alguém que pode ajudar? Conte aos seus amigos, familiares e colegas sobre a PRF e o trabalho que salva vidas que fazemos! Muitas vezes, as pessoas são mais propensas a doar para uma organização se tiverem recebido uma recomendação de alguém que conhecem. Então fale bem de nós e diga a todos para nos seguirem em X@progeria, “curta” a gente no Facebook, confira nossas fotos em Instagram @progeriaresearch, conheça a comunidade Progeria através de alguns Vídeos do YouTube, e entre em contato conosco diretamente em info@progeriaresearch.org.Estamos ansiosos para nos conectar com você!
JUNTOS ENCONTRAREMOS A CURA!
[1] Outras síndromes progeroides incluem a síndrome de Werner, também conhecida como “progeria adulta”, que não tem início até o final da adolescência, com uma expectativa de vida de até 40 e 50 anos.
[2] Para um mapa de onde residem as crianças vivas, acesse https://www.progeriaresearch.org/meet-the-kids/.
[3] “Mutações pontuais recorrentes de novo na lâmina A causam a Síndrome de Hutchinson-Gilford Progeria”, Nature, Vol. 423, 15 de maio de 2003.
[4] Estatísticas de doenças cardíacas e derrames da American Heart Association de 2021.
[5] Gordon LB, Kleinman ME, et al. Ensaio clínico de um inibidor de farnesiltransferase em crianças com síndrome de progeria de Hutchinson-Gilford. Proc Natl Acad Sci US A. 2012 Out 9;109(41):16666-71. doi: 10.1073/pnas.1202529109. Epub 2012 Set 24.
[6] Gordon LB, Shappell H, Massaro J, et al. Associação do tratamento com Lonafarnib versus nenhum tratamento com a taxa de mortalidade em pacientes com síndrome de Hutchinson-Gilford Progeria. JAMA. 2018;319(16):1687–1695.
[7] Gordon, LB, Norris, W., Hamren, S., e outros. Progerina plasmática em pacientes com síndrome de Hutchinson-Gilford Progeria: desenvolvimento de imunoensaio e avaliação clínica. Circulação, 2023.
[8] Gordon LB, Basso S, et al. Intervenção para estenose aórtica crítica na síndrome de progeria de Hutchinson-Gilford. Frente. Cardiovasc. Med. 11:1356010. doi: 10.3389/fcvm.2024.1356010 (2024).
[9] Koblan, LW, Erdos, MR, Wilson, C. et al. A edição de base in vivo resgata a síndrome de progeria de Hutchinson–Gilford em camundongos. Nature 589, 608–614 (2021).
[10] Erdos, MR, Cabral, WA, Tavarez, UL et al. Uma abordagem terapêutica antisense direcionada para a síndrome de progeria de Hutchinson–Gilford. Nat Med (2021). https://doi.org/10.1038/s41591-021-01274-0
[11] Puttaraju, M., Jackson, M., Klein, S. et al. Triagem sistemática identifica oligonucleotídeos antisense terapêuticos para síndrome de progeria de Hutchinson–Gilford. Nat Med (2021). https://doi.org/10.1038/s41591-021-01262-4
[12] Kang SM, Yoon MH, et al. Progerinina, um inibidor otimizado da ligação progerina-lamina A, melhora os fenótipos de senescência prematura da síndrome de progeria de Hutchinson-Gilford. Biologia Comunitária. 4 de janeiro de 2021; 4(1):5.
[13] Gordon, LB, Norris, W., Hamren, S., et al. Progerina plasmática em pacientes com síndrome de Hutchinson-Gilford Progeria: desenvolvimento de imunoensaio e avaliação clínica. Circulação, 2023
