Wat is er nieuw in
Progeria-onderzoek
We hebben deze sectie toegevoegd zodat u eenvoudig toegang hebt tot informatie over de nieuwste en belangrijkste wetenschappelijke publicaties over progeriaonderzoek.
Naast de hieronder gemarkeerde artikelen, zijn er nu honderden artikelen over Progeria en Progeria-gerelateerde onderwerpen. We raden u aan om PubMed te doorzoeken om de specifieke onderwerpen te vinden die u zoekt.
Maart 2023: Spannende onderzoeksmijlpalen in behandelingsevaluatie en levensverlenging!
We zijn verheugd om twee spannende onderzoeksupdates met u te delen, die vandaag online zijn gepubliceerd in 's werelds beste cardiovasculaire tijdschrift, Circulatie (1):
Biomarker bij Progeria
Een nieuwe manier om progerine te meten, het toxische eiwit dat Progeria veroorzaakt, is ontwikkeld door een team onder leiding van PRF medeoprichter en medisch directeur, Dr. Leslie Gordon. Met de ontdekking van deze biomarker, die bloedplasma gebruikt om progerineniveaus te meten, onderzoekers kunnen na een kortere tijdsperiode begrijpen hoe behandelingen deelnemers aan klinische proeven beïnvloeden en op meerdere punten tijdens elke klinische proef.
Deze test kan het klinische proefproces optimaliseren door: het verstrekken van vroege informatie over de effectiviteit van de behandelingen die worden getest, als een aanloop naar andere klinische tests zoals gewichtstoename, dermatologische veranderingen, gewrichtscontractuur en -functie, enz., die allemaal veel meer tijd nodig hebben om zich te manifesteren. Deze klinische kenmerken van Progeria zijn belangrijke langetermijnmetingen van behandelingseffecten die nu worden aangevuld met de progerineniveaus die eerder in de therapie zijn gemeten. We kunnen nu mogelijk al vier maanden na het starten van de behandeling de voordelen van de behandeling begrijpen, of een behandeling stoppen die de proefdeelnemer mogelijk niet ten goede komt, om onnodige bijwerkingen te voorkomen.
Nog langere levens met lonafarnib
Deze nieuwe en innovatieve manier om progerine te meten, versnelt niet alleen toekomstige ontdekkingen op het gebied van behandelingen en genezingen, maar geeft ook aan dat de Het langetermijnvoordeel van lonafarnib voor kinderen met Progeria is groter dan eerder vastgesteld.
Onderzoeksgegevens geven aan dat lagere progerinespiegels in het bloed overlevingsvoordelen weerspiegelden: hoe langer iemand met Progeria lonafarnib bleef gebruiken, hoe groter het overlevingsvoordeel van de therapie. Progerinespiegels werden met ongeveer 30-60% verlaagd zolang het medicijn werd ingenomen, en de levensverwachting van patiënten die meer dan 10 jaar werden behandeld, werd geschat op een toename van bijna 5 jaar. Dat is meer dan 35% toename van de gemiddelde levensduur, van 14,5 jaar tot bijna 20 jaar!
Voor meer informatie, zie hier ons persbericht
“Een van de meest opmerkelijke verhalen die ooit in deze podcast is gedeeld”
– Dr. Carolyn Lam, wereldberoemd hartspecialist en gastheer van de podcast Circulatie op de vlucht, over de reis die leidde tot deze opwindende bevindingen. Luister naar het volledige interview over de diepgaande impact van deze studie rechtstreeks van Dr. Gordon. Luister hier (vanaf 6:41).
Luister naar Dr. Leslie Gordon op de Circulation on the Run-podcast
En in juni verschenen er twee redactionele artikelen (2) En (3) werden gepubliceerd in Circulatie Hiermee wordt het cruciale belang van deze biomarker voor het verbeteren van behandelingen en genezing van kinderen met Progeria benadrukt, en voor een beter begrip van veroudering.

(1) Gordon, LB, Norris, W., Hamren, S., et alPlasma Progerine bij patiënten met Hutchinson-Gilford Progeria-syndroom: immunoassay-ontwikkeling en klinische evaluatie. Circulatie, 2023
(2) Progressie van hartafwijkingen bij het Hutchinson-Gilford Progeria-syndroom: een prospectieve longitudinale studie.
Olsen FJ, Gordon LB, Smoot L, Kleinman ME, Gerhard-Herman M, Hegde SM, Mukundan S, Mahoney T, Massaro J, Ha S, Prakash A. Circulatie. 2023 6 juni;147(23):1782-1784. doi: 10.1161/CIRCULATIONAHA.123.064370. Epub 2023 5 juni.
(3) Gemakkelijk beschikbare hulpmiddelen om progerine en progressie van hartziekten bij het Hutchinson-Gilford Progeria-syndroom te detecteren.
Eriksson M, Haugaa K, Revêchon G. Circulatie. 2023 6 juni;147(23):1745-1747. doi: 10.1161/CIRCULATIONAHA.123.064765. Epub 2023 5 juni.
Maart 2021: Spannende doorbraken in RNA-therapie voor progeria!
We zijn verheugd om de resultaten van twee zeer opwindende baanbrekende studies over het gebruik van RNA-therapieën in Progeria-onderzoek. Beide studies werden medegefinancierd door The Progeria Research Foundation (PRF) en mede geschreven door PRF's medisch directeur, Dr. Leslie Gordon.
Progerine is het ziekteverwekkende eiwit in Progeria. De RNA-therapieën verstoren het vermogen van het lichaam om progerine te produceren, door de productie ervan op RNA-niveau te blokkeren. Dit betekent dat de behandeling is specifieker dan de meeste therapieën die progerine op proteïneniveau aanpakken.
Hoewel elke studie een ander medicijnafgiftesysteem gebruikte, richtten beide studies zich op dezelfde basisbehandelingsstrategie, namelijk het remmen van de productie van RNA dat codeert voor het abnormale eiwit, progerine. Beide werden geleid door onderzoekers van de National Institutes of Health (NIH) en werden vandaag gepubliceerd in het tijdschrift Natuurgeneeskunde.
Eén studie, onder leiding van Francis Collins, MD, PhD, directeur van het NIH, toonde aan dat de behandeling van Progeria-muizen met een medicijn genaamd SRP2001 rverminderde de schadelijke progerine mRNA- en proteïne-expressie in de aorta, de belangrijkste slagader in het lichaam, en ook in andere weefsels. Aan het einde van de studie bleef de aortawand sterker en vertoonden de muizen een verhoogde overleving van meer dan 60%.
"Dat een gerichte RNA-therapie zulke significante resultaten laat zien in een diermodel geeft mij hoop dat dit kan leiden tot een grote vooruitgang in de behandeling van progeria", aldus Collins.
De andere studie, onder leiding van Tom Misteli, PhD, directeur van het Center for Cancer Research, National Cancer Institute, NIH, toonde een 90 – 95% reductie van het toxische progerine-producerende RNA in verschillende weefsels na behandeling met een medicijn genaamd LB143. Misteli's lab ontdekte dat progerine-eiwitreductie het meest effectief was in de lever, met aanvullende verbeteringen in het hart en de aorta.
We weten nu dat er meerdere manieren zijn om de productie van het schadelijke progerine-eiwit te verminderen met behulp van RNA-therapieën. Elke studie vond verschillende stukken RNA in de muismodellen die, wanneer gericht, een effectief pad voor behandeling opleverden, wat resulteerde in Progeria-muizen die veel langer leefden dan de muizen die in eerdere onderzoeken met Zokinvy (lonafarnib) werden behandeld, het enige door de FDA goedgekeurde medicijn voor kinderen met Progeria. Bovendien ontdekten onderzoekers dat een combinatiebehandeling met RNA-therapieën en Zokinvy (lonafarnib) de progerine-eiwitniveaus in de lever en het hart effectiever verlaagde dan beide behandelingen afzonderlijk.
“Deze twee uiterst belangrijke onderzoeken tonen aan dat grote ontwikkelingen die nu voor ons liggen op het gebied van gerichte Progeria-therapieën,” zei PRF medisch directeur, Dr. Leslie Gordon. “Ik was verheugd om met deze briljante onderzoeksgroepen samen te werken om RNA-therapie voor kinderen met Progeria te verbeteren. Beide zijn opwindende proof-of-principle-studies en PRF is enthousiast om door te gaan met klinische proeven die deze behandelingsstrategieën toepassen.
—
Erdos, MR, Cabral, WA, Tavarez, UL et al. Een gerichte antisense therapeutische aanpak voor het Hutchinson-Gilford progeriasyndroom. Nat Med (2021). https://doi.org/10.1038/s41591-021-01274-0
Puttaraju, M., Jackson, M., Klein, S. et al. Systematische screening identificeert therapeutische antisense-oligonucleotiden voor het Hutchinson-Gilford-progeriasyndroom. Nat Med (2021). https://doi.org/10.1038/s41591-021-01262-4
Januari 2021: Opmerkelijke vooruitgang in genetische bewerking in Progeria-muismodellen
Het wetenschappelijke tijdschrift Natuur gepubliceerde baanbrekende resultaten waaruit blijkt dat genetische bewerking in een muizenmodel van Progeria de mutatie corrigeert die Progeria in veel cellen veroorzaakt, een aantal belangrijke ziektesymptomen verbetert en de levensduur van de muizen aanzienlijk verhoogt.
Medegefinancierd door PRF en mede geschreven door PRF's medisch directeur Dr. Leslie Gordon, ontdekte de studie dat met een enkele injectie van een base-editor die geprogrammeerd was om de ziekteveroorzakende mutatie te corrigeren, muizen 2,5 keer langer overleefden dan onbehandelde Progeria-muizen, tot een leeftijd die overeenkomt met het begin van de ouderdom bij gezonde muizen. Belangrijk is dat behandelde muizen ook gezond vaatweefsel behielden - een significante bevinding, aangezien verlies van vasculaire integriteit een voorspeller is van sterfte bij kinderen met Progeria.
Het onderzoek werd gezamenlijk geleid door David Liu, PhD, een expert op het gebied van genetische bewerking van het Broad Institute van het MIT, Jonathan Brown, universitair hoofddocent geneeskunde bij de afdeling cardiovasculaire geneeskunde aan de Vanderbilt University, en Francis Collins, MD, PhD, directeur van de National Institutes of Health.
"Deze dramatische respons zien in ons Progeria-muismodel is een van de meest opwindende therapeutische ontwikkelingen waar ik in 40 jaar als arts-wetenschapper aan heb meegewerkt", aldus Dr. Collins.
“Vijf jaar geleden waren we nog bezig met de ontwikkeling van de allereerste base-editor,” zei Dr. Liu. “Als je me toen had verteld dat binnen vijf jaar een enkele dosis van een base-editor Progeria in een dier op het niveau van DNA, RNA, proteïne, vasculaire pathologie en levensduur zou kunnen aanpakken, zou ik hebben gezegd: ‘dat kan niet.’ Het is een echt bewijs van de toewijding van het team dat dit werk mogelijk heeft gemaakt.”
Er zijn aanvullende preklinische studies nodig om deze resultaten te onderzoeken, waarvan we hopen dat ze ooit zullen leiden tot een klinische proef. Lees meer over dit opwindende nieuws in dit Wall Street-journaal artikel.
November 2020: FDA-goedkeuring voor lonafarnib (Zokinvy)
Op 20 november 2020 heeft PRF een belangrijk onderdeel van onze missie voltooid: lonafarnib, de allereerste behandeling voor Progeria, heeft goedkeuring gekregen van de FDA.
Progeria behoort nu tot de zeldzame ziekten waarvoor de FDA een behandeling heeft goedgekeurd.* Kinderen en jongvolwassenen met Progeria in de VS kunnen nu op recept lonafarnib (nu 'Zokinvy' genoemd) krijgen, in plaats van via een klinische proef.
Deze belangrijke mijlpaal is bereikt dankzij 13 jaar hard werken aan onderzoek, bestaande uit vier klinische onderzoeken die allemaal gecoördineerd werden door PRF, mogelijk gemaakt werden door de dappere kinderen en hun families en gefinancierd werden door jullie, de geweldige gemeenschap van donateurs van PRF.
Klik hier voor meer informatie.
*300 zeldzame ziekten waarvoor een door de FDA goedgekeurde behandeling bestaat (https://www.rarediseases.info.nih.gov/diseases/FDS-orphan-drugs)/7.000 zeldzame ziekten waarvan de moleculaire basis bekend is (www.OMIM.org) =4,2%
April 2018: Wereldwijd onderzoek gepubliceerd in JAMA toont aan dat behandeling met Lonafarnib de overleving van kinderen met Progeria verlengt
Klik hier voor meer informatie.
Verband tussen behandeling met lonafarnib en geen behandeling met het sterftecijfer bij patiënten met het Hutchinson-Gilford Progeria-syndroom, Leslie B. Gordon, MD, PhD; Heather Shappell, PhD; Joe Massaro, PhD; Ralph B. D'Agostino Sr., PhD; Joan Brazier, MS; Susan E. Campbell, MA; Monica E. Kleinman, MD; Mark W. Kieran, MD, PhD; JAMA-nummer, 24 april 2018.
Juli 2016: Resultaten van de drievoudige proef
Oktober 2014: PRF's opmerkelijke reis gepubliceerd in Expert Opinion
 In een artikel gepubliceerd in Deskundig advies en geschreven door directeur Audrey Gordon en medisch directeur Leslie Gordon, bespreken de twee PRF-leiders de geschiedenis, doelen en prestaties van PRF en hoe de PRF-programma's cruciaal zijn geweest in de reis van onbekendheid naar behandeling.
In een artikel gepubliceerd in Deskundig advies en geschreven door directeur Audrey Gordon en medisch directeur Leslie Gordon, bespreken de twee PRF-leiders de geschiedenis, doelen en prestaties van PRF en hoe de PRF-programma's cruciaal zijn geweest in de reis van onbekendheid naar behandeling.
De auteurs schrijven: “Het is onze hoop dat de beschrijving van de PRF-programma's en -diensten die volgt, samen met een verslag van hoe zij PRF helpen haar missie te volbrengen om kinderen met Progeria te redden, anderen zal helpen en inspireren om soortgelijke actie te ondernemen voor de vele zeldzame ziektepopulaties die onmiddellijke aandacht nodig hebben.”
Mei 2014: Onderzoek toont aan dat proefmedicijnen de geschatte levensduur van kinderen met progeria verlengen
Deze studie toont aan dat er bewijs is dat een farnesyltransferaseremmer (FTI) de levens van kinderen met Progeria met ten minste anderhalf jaar kan verlengen. De studie toonde een verlenging van de gemiddelde overleving van 1,6 jaar gedurende de zes jaar na aanvang van de behandeling. Twee extra medicijnen die later in de trials werden toegevoegd, pravastatine en zoledronaat, kunnen ook bijdragen aan deze bevinding. Dit is het eerste bewijs dat behandelingen de overlevingskans bij deze dodelijke ziekte beïnvloeden.
Klik hier voor meer informatie.
Impact van farnesyleringsremmers op overleving bij het Hutchinson-Gilford Progeria-syndroom, Leslie B. Gordon, MD, PhD, Joe Massaro, PhD, Ralph B. D'Agostino Sr., PhD, Susan E. Campbell, MA, Joan Brazier, MS, W. Ted Brown, MD, PhD, Monica E Kleinman, MD, Mark W. Kieran MD, PhD en de Progeria Clinical Trials Collaborative; Circulatie, 2 mei 2014 (online).
September 2012: Eerste Progeria-behandeling ooit ontdekt
De resultaten van de allereerste klinische medicijnproef voor kinderen met Progeria blijkt dat Lonafarnib, een type farnesyltransferaseremmer (FTI) dat oorspronkelijk is ontwikkeld om kanker te behandelen, effectief is gebleken voor Progeria. Elk kind vertoont verbetering op een of meer van de vier volgende manieren: extra gewichtstoename, beter gehoor, verbeterde botstructuur en/of, het allerbelangrijkst, toegenomen flexibiliteit van bloedvaten. De studie* werd gefinancierd en gecoördineerd door The Progeria Research Foundation.
Klik hier voor meer informatie.
*Gordon LB, Kleinman ME, Miller DT, Neuberg D, Giobbie-Hurder A, Gerhard-Herman M, Smoot L, Gordon CM, Cleveland R, Snyder BD, Fligor B, Bishop WR, Statkevich P, Regen A, Sonis A, Riley S, Ploski C, Correia A, Quinn N, Ullrich NJ, Nazarian A, Liang MG, Huh SY, Schwartzman A, Kieran MW, Klinische proef van een farnesyltransferaseremmer bij kinderen met Hutchinson-Gilford Progeria-syndroom, Handelingen van de Nationale Academie van Wetenschappen, 9 oktober 2012 jaargang 109 nr. 41 16666-16671
Oktober 2011: Een nieuwe benadering van progeriatherapie
Dat afwijkende splicing in gekweekte huidcellen van Progeria op deze manier kan worden voorkomen, werd in 2005 aangetoond (2). Voor de behandeling van patiënten moet het remmende reagens echter intact in alle weefsels van de patiënt worden toegediend. Het duurde nog eens zes jaar en er was werk in verschillende laboratoria nodig om deze 'toedieningsmethoden' te ontwikkelen.
In het nieuwe onderzoek (1) resulteerde het blokkeren van de afwijkende splicing in de modelmuis in indrukwekkende resultaten. Er waren duidelijke reducties in progerineconcentraties in alle geanalyseerde weefsels, behalve skeletspieren, die mogelijk een verminderde opname van het blokkerende middel hebben. De modelmuizen herhaalden veel van de fenotypes van Progeria-patiënten, waaronder
- Sterk verkorte levensduur (103 dagen vergeleken met 2 jaar voor wilde-type muizen.)
- Vermindering van de groeisnelheid.
- Abnormale houding met kromming van de wervelkolom.
- Ernstige nucleaire afwijkingen als gevolg van progerine-accumulatie.
- Algemeen verlies van de vetlaag onder de huid.
- Diepgaande botafwijkingen.
- Cardiovasculaire veranderingen, waaronder aanzienlijk verlies van gladde spiercellen in de bloedvaten.
- Veranderingen in de concentraties van verschillende hormonen in het circulerende bloedplasma, waaronder insuline en groeihormoon.
De in levenden lijve Het aantonen van de doeltreffendheid van het verminderen van de progerineproductie door het blokkeren van de afwijkende splicing is een sterke kandidaat voor een waardevolle nieuwe benadering van de behandeling van Progeria.
(1) Osorio FG, Navarro CL, Cadiñanos J, López-Mejia IC, Quirós PM, et al, Science Translational Medicine, 3: Nummer 106, online vooruitpublicatie, 26 oktober (2011).
(2) Scaffidi, P. en Misteli, T. Omkering van het cellulaire fenotype bij de vroegtijdige verouderingsziekte Hutchinson-Gilford progeriasyndroom, Nature Medicine 11 (4): 440-445 (2005).
Juni 2011: PRF-gefinancierde studie identificeert rapamycine als mogelijke behandeling voor progeria
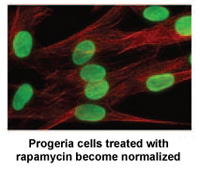
Onderzoekers van de National Institutes of Health en het Massachusetts General Hospital in Boston, MA hebben vandaag een nieuwe studie gepubliceerd in Wetenschap, Translationele Geneeskunde die kan leiden tot een nieuwe medicamenteuze behandeling voor kinderen met Progeria.*
Rapamycine is een door de FDA goedgekeurd medicijn waarvan eerder is aangetoond dat het de levensduur van niet-progeria muismodellen verlengt. Deze nieuwe studie toont aan dat rapamycine de hoeveelheid van het ziekteverwekkende eiwit progerine met 50% verlaagt, de abnormale kernvorm verbetert en de levensduur van progeriacellen verlengt. Deze studie levert het eerste bewijs dat rapamycine de schadelijke effecten van progerine bij kinderen met progeria kan verminderen.
Er is enorm veel media-aandacht voor dit onderwerp! Klik hieronder voor links naar mediaverhalen:
Wall Street Journal Gezondheidsblog
Amerikaans nieuws en wereldrapport
De Progeria Research Foundation was verheugd om cellen voor dit project te kunnen leveren van de PRF-cel- en weefselbanken help het onderzoek te financieren via onze subsidieprogramma.
Deze nieuwe, interessante studie toont aan hoe snel progeriaonderzoek verloopt en biedt meer inzicht in het verouderingsproces dat ons allemaal treft.
*”Rapamycine keert cellulaire fenotypes om en verbetert de verwijdering van mutante eiwitten in Hutchinson-Gilford Progeria-cellen”
Kan Cao, John J. Graziotto, Cecilia D. Blair, Joseph R. Mazzulli, Michael R. Erdos, Dimitri Krainc, Francis S. Collins
Sci Transl Med. 29 juni 2011;3(89):89ra58.
Juni 2011: baanbrekende studie over het verband tussen progeria en veroudering
CBS Avondnieuws, Wall Street-journaal En Anderen Rapport over nieuwe studie
Onderzoekers van de National Institutes of Health hebben een voorheen onbekende link ontdekt tussen Progeria en veroudering. De bevindingen bieden inzicht in de relatie tussen het toxische, Progeria-veroorzakende eiwit bekend als progerine En telomeren, die de uiteinden van het DNA in cellen beschermen totdat ze na verloop van tijd afslijten en de cellen afsterven.
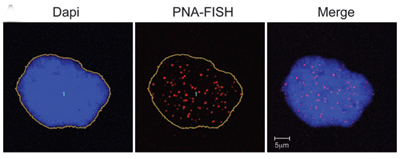
Progerine-expressieve cellen van normale individuen vertonen tekenen van veroudering. DNA in de kern is blauw gekleurd. Telomeren worden gezien als rode stippen.
De studie* verschijnt in de vroege online editie van het Journal of Clinical Investigation van 13 juni 2011. De conclusie is dat bij normale veroudering korte of disfunctionele telomeren cellen stimuleren om progerine te produceren, wat geassocieerd wordt met leeftijdsgebonden celschade.
“Voor het eerst weten we dat telomeerverkorting en disfunctie de productie van progerine beïnvloeden,” zegt Leslie B. Gordon, MD, PhD, medisch directeur van de Progeria Research Foundation. “Dus deze twee processen, die beide de cellulaire veroudering beïnvloeden, zijn feitelijk met elkaar verbonden.”
Eerder onderzoek heeft aangetoond dat progerine niet alleen wordt geproduceerd bij kinderen met Progeria, maar dat het in kleinere hoeveelheden wordt geproduceerd bij ons allemaal, en dat progerineniveaus toenemen met het ouder worden. Onafhankelijk daarvan is eerder onderzoek naar telomeerverkorting en disfunctie geassocieerd met normale veroudering. Sinds 2003, met de ontdekking van de Progeria-genmutatie en het progerine-eiwit dat de ziekte veroorzaakt, is een van de belangrijkste onderzoeksgebieden gericht op het begrijpen of en hoe Progeria en veroudering met elkaar verbonden zijn.
"Het verbinden van dit zeldzame ziekteverschijnsel met normale veroudering werpt op een belangrijke manier vruchten af", aldus NIH-directeur Francis S. Collins, MD, PhD, een van de hoofdauteurs van het artikel. "Deze studie benadrukt dat waardevolle biologische inzichten worden verkregen door zeldzame genetische aandoeningen zoals Progeria te bestuderen. Vanaf het begin hadden we het gevoel dat Progeria ons veel te leren had over het normale verouderingsproces."
Wetenschappers hebben telomeren en progerine traditioneel apart bestudeerd. Hoewel er nog veel te leren valt over de vraag of deze nieuwe verbinding kan leiden tot een genezing voor kinderen met Progeria of mogelijk kan worden toegepast op het verlengen van de menselijke levensduur, levert deze studie verder bewijs dat progerine, het toxische eiwit dat werd ontdekt door de genmutatie in Progeria te vinden, een rol speelt in het normale verouderingsproces.
*Progerine en telomeerdisfunctie werken samen om cellulaire veroudering in normale menselijke fibroblasten te veroorzaken, Cao et al., J Clin Invest doi:10.1172/JCI43578.
Klik hier voor de volledige tekst van het NIH-persbericht.
Mei 2011: Oorzaak van progeroïdesyndroom ontdekt, wat meer inzicht biedt in de link tussen progeria en veroudering
Een onderzoeksteam onder leiding van Progeria-onderzoeker Dokter Carlos López-Otín van de Universiteit van Oviedo in Spanje kwamen twee families tegen waarvan de kinderen een voorheen onbekende versnelde verouderingsziekte hadden die vergelijkbaar was met Progeria. De kinderen vertoonden geen defecten in genen die eerder in verband waren gebracht met progeroïde ziekten, maar door de "coderende" delen van hun genoom te bestuderen, vond het team een defect in een gen genaamd BANF1. Familieleden met de progeroïde ziekte hadden zeer lage hoeveelheden van het eiwit dat door BANF1 wordt gemaakt en, net als mensen met Progeria, waren de nucleaire enveloppen in hun cellen opvallend abnormaal. De afwijkingen verdwenen in celcultuurexperimenten toen het defecte gen werd vervangen door de juiste versie. De bevindingen werden gepubliceerd in de Amerikaans tijdschrift voor menselijke genetica in mei 2011.
BANF1 voegt zich nu bij de groep bekende genen die invloed lijken te hebben op bepaalde vormen van vroegtijdige veroudering, en die mogelijk ook normale veroudering beïnvloeden.
De afgelopen jaren hebben wetenschappers de normale veroudering op moleculair niveau beter kunnen begrijpen, deels dankzij studies van premature verouderingssyndromen zoals deze en Progeria, die "de vroege ontwikkeling van kenmerken veroorzaken die normaal gesproken worden geassocieerd met gevorderde leeftijd", aldus López-Otín. Hij voegde toe dat zijn studie "het belang van de nucleaire lamina voor menselijke veroudering onderstreept en het nut aantoont van de nieuwe methoden van genoomsequentiebepaling om de genetische oorzaak van zeldzame en verwoestende ziekten te identificeren, die traditioneel weinig aandacht hebben gekregen."
Xose S. Puente, Victor Quesada, Fernando G. Osorio, Rubén Cabanillas, Juan Cadiñanos, Julia M. Fraile, Gonzalo R. Ordóñez, Diana A. Puente, Ana Gutiérrez-Fernández, Miriam Fanjul-Fernández et al. "Exome-sequencing en functionele analyse identificeren BANF1-mutatie als de oorzaak van een erfelijk progeroidsyndroom." American Journal of Human Genetics, 5 mei 2011 DOI: 10.1016/j.ajhg.2011.04.010
Augustus 2010: Insuline-achtige groeifactor 1 verbetert symptomen en verlengt leven bij een progeroid muis
Op 26 augustus 2010, Arteriosclerose, trombose en vasculaire biologie elektronisch gepubliceerd, vóór de druk, de resultaten van een studie die Progeria en typische cardiovasculaire veroudering vergelijkt, getiteld "Cardiovasculaire pathologie in Hutchinson-Gilford Progeria: Correlatie met de vasculaire pathologie van veroudering". De studie ontdekte dat progerine, het abnormale eiwit dat Progeria veroorzaakt, ook aanwezig is in de vasculatuur van de algemene bevolking en toeneemt met de leeftijd, wat bijdraagt aan het groeiende geval dat er parallellen zijn tussen normale veroudering en progeria-veroudering.
Onderzoekers bestudeerden cardiovasculaire autopsieën en de progerineverdeling bij patiënten met Progeria en bij een groep zonder Progeria tussen de leeftijd van één maand en 97 jaar. Ze ontdekten dat progerine bij personen zonder Progeria gemiddeld met 3,3 procent per jaar toenam in de kransslagaders.
"We vonden overeenkomsten tussen veel aspecten van hart- en vaatziekten in zowel Progeria als de atherosclerose die miljoenen mensen over de hele wereld treft", aldus Dr. Leslie Gordon, hoofdauteur van de studie en medisch directeur van The Progeria Research Foundation. "Door een van de zeldzaamste ziekten ter wereld te onderzoeken, krijgen we cruciaal inzicht in een ziekte die miljoenen mensen over de hele wereld treft. Doorlopend onderzoek heeft het potentieel om een aanzienlijke impact te hebben op ons begrip van hartziekten en veroudering."
Deze studie ondersteunt de mogelijkheid dat progerine bijdraagt aan het risico op atherosclerose bij de algemene bevolking. Het verdient daarom nader onderzoek als een potentiële nieuwe eigenschap die het risico op hartziekten kan helpen voorspellen.
Olive M, Harten I, Mitchell R, Beers J, Djabali K, Cao K, Erdos MR, Blair C, Funke B, Smoot L, Gerhard-Herman M, Machan JT, Kutys R, Virmani R, Collins FS, Wight TN, Nabel EG, Gordon LB.
“Cardiovasculaire pathologie bij Hutchinson-Gilford Progeria: correlatie met de vasculaire pathologie van veroudering”. Arterioscler trombus Vasc Biol. 2010 nov;30(11):2301-9; Epub 26 augustus 2010.
Mei 2010: Oxford-onderzoeken tonen aan hoe Progeria-onderzoek ons begrip van normale veroudering kan vergroten
Deze situatie is erg vergelijkbaar met die in Progeria. Daar behoudt prelamine A (progerine genoemd) de farnesylgroep. De eerste stap in het veroorzaken van de ziekte is het falen om de farnesylgroep te verwijderen. Dit falen gebeurt omdat de Progeria-mutatie resulteert in het verwijderen van het deel van prelamine A dat nodig is voor FACE 1 om de farnesylgroep te binden en te verwijderen. De oorzaak van de defecten in veroudering en Progeria zijn dus hetzelfde: FACE1 kan zijn werk niet doen.
Het is al een aantal jaren bekend dat farnesyltransferaseremmers (FTI's) de aanwezigheid van nucleaire markers van ziekte in Progeria-cellen remmen (en kunnen omkeren). Nu hebben Shanahan et al. ontdekt dat FTI's de verschijning van vergelijkbare nucleaire markers in cellen van oudere normale individuen remmen. FTI's worden momenteel gebruikt in klinische onderzoeken naar Progeria en Shanahan et al. merken op dat deze klinische onderzoeken "verder licht zullen werpen op het therapeutische potentieel van deze medicijnen bij de behandeling van veroudering."
De onderzoeken die in dit artikel worden beschreven, zijn tot nu toe het beste voorbeeld van hoe onderzoeken naar Progeria ons inzicht in normaal verouderingsproces vergroten.
Ragnauth CD, Warren DT, Liu Y, Shanahan CM et al, “Prelamine A versnelt de veroudering van gladde spiercellen en is een nieuwe biomarker voor vasculaire veroudering bij mensen.” Circulation: 25 mei 2010, pp. 2200-2210.
April 2010: Verder bewijs dat bij Progeria de aanwezigheid van een farnesylgroep in het progerinemolecuul verantwoordelijk is voor de ziekteverschijnselen.
Davies en collega's bereidden een nieuw modelmuis voor waarvan prelamine A, in tegenstelling tot RD-prelamine A, niet gefarnesyleerd is, maar wel de 15 aminozuursequentie behoudt die normaal gesproken wordt gesplitst in het pad om lamin A te synthetiseren. Deze muis heeft geen progeroïde symptomen, wat aangeeft dat bij RD, evenals bij Progeria, de aanwezigheid van de farnesylgroep, en niet een verandering in aminozuursequentie, verantwoordelijk is voor de ziektesymptomen.
DaviesBS, Barnes RH 2e, Tu Y, Ren S, Andres DA, Spielmann HP, Lammerding J, Wang Y, Young SG, Fong LG,
“Een ophoping van niet-gefarnesyleerd prelamine A veroorzaakt cardiomyopathie, maar geen progeria”, Hum Mol Genet. 26 april 2010. [Epub vóór druk]
Februari 2010: Meer bewijs dat FTI's gunstige effecten hebben door farnesylering van progerine
De auteurs evalueerden de mogelijkheid dat de verbetering van progeroïde ziekte door een farnesyltransferase-remmer (FTI) in een muizenmodel van Progeria te wijten is aan het effect van het medicijn op farnesylering van andere proteïne(n) dan progerine. Ze construeerden een muis die ongefarnesyleerde progerine maakte, maar geen gefarnesyleerde progerine. Deze muis ontwikkelde ook progeria-achtige ziektefenotypes, maar FTI verbeterde deze niet. Dit resultaat geeft aan dat het medicijn niet werkt door andere proteïnen dan progerine te remmen; het moet werken op de farnesylering van progerine, de biochemische stap die niet aanwezig is in het geteste model.
Yang SH, Chang SY, Andres DA, Spielmann HP, Young SG, Fong LG. “Beoordeling van de werkzaamheid van proteïne farnesyltransferase-remmers in muismodellen van progeria.”
J Lipide Res. 2010 feb;51(2):400-5. Epub 26 okt 2009.
Oktober 2009: De kunsten ontmoeten de wetenschappen in het verhaal van Benjamin Button
Maloney WJ, “Hutchinson-Gilford Progeria-syndroom: de presentatie ervan in het korte verhaal 'The Curious Case of Benjamin Button' van F. Scott Fitzgerald en de orale manifestaties ervan.”
J. Dent.Res. 2009 okt 88 (10): 873-6
Mei 2009: Artikel opent nieuw terrein over het effect van HGPS op cellulaire functies.
Eerder is aangetoond dat HGPS veel fundamentele cellulaire functies beïnvloedt, waaronder replicatie, genexpressie en DNA-herstel. Busch en collega's hebben het transport van eiwitten van het cytoplasma naar de kern aan deze lijst toegevoegd. Alle eiwitten worden gesynthetiseerd in het cytoplasma en de eiwitten die uiteindelijk in de kern terechtkomen, moeten door het kernmembraan heen. Het transport wordt bereikt via kanalen in het kernmembraan, die 'kernporiën' worden genoemd. Veel eiwitten zijn te groot om eenvoudigweg door de kernporiën te diffunderen, maar worden erdoorheen 'geleid' door speciale eiwitten die voor dit doel zijn geëvolueerd. In dit artikel werd ontdekt dat cellen die het gemuteerde gen tot expressie brengen dat verantwoordelijk is voor HGPS, door directe meting een verminderd transport van eiwitten naar de kernen hebben.
Busch A, Kiel T, Heupel WM, Wehnert M, Huebner S., “De import van nucleaire eiwitten is verminderd in cellen die lamin A-mutanten tot expressie brengen die nucleaire envelopathie veroorzaken.” Exp Cel Res. 11 mei 2009.
April 2009: Progeria en normale veroudering koppelen: nieuwe inzichten
→ Structuur en organisatie bieden: nucleaire architectuur en genoomintegriteit
→ DNA-schade en -herstel zijn misgegaan
→ Oude en niet meer te repareren tumorsuppressoren en cellulaire veroudering, en
→ Regeneratie en vernieuwing: stamcelbiologie. Regeneratie en vernieuwing: stamcelbiologie.
Het artikel belicht de manieren waarop recente ontwikkelingen in het onderzoek naar progeroïde ziekten inzicht bieden in fundamentele cellulaire functies en veroudering.
Capell BS, Tlougan BE, Orlow SJ, “Van de zeldzaamste tot de meest voorkomende: inzichten uit progeroid syndromen in huidkanker en veroudering.” Tijdschrift voor Onderzoekende Dermatologie (23 april 2009), 1-11
April 2009: Eerdere PRF-onderzoekssubsidies ontwikkelen nieuwe methode om progerine in cellen te bestuderen
Eerdere experimenten met fibroblastcellen van Progeria-patiënten hebben aangetoond dat de schade die door de mutatie wordt veroorzaakt, in eerste instantie het resultaat is van de actie van de gewijzigde vorm van Lamin A, genaamd Progerin. Maar de interpretatie van deze experimenten kan moeilijk zijn in cultuur voor verschillende aantallen generaties. Fong et. al. hebben een experimenteel systeem opgezet waarin de hoeveelheid Progerin in Wildtype cellen kunnen worden vergroot of verkleind. Deze methode zal onderzoekers in staat stellen om de directe effecten van Progerin te onderscheiden van secundaire effecten, waardoor de studie van cellulaire mechanismen die leiden tot de pathofysiologie van Progeria-cellen wordt bevorderd.
Activering van de synthese van progerine, het gemuteerde prelamine A bij het Hutchinson-Gilford progeriasyndroom, met antisense-oligonucleotiden. (PubMed-artikel) Fong LG, Vickers TA, Farber EA, Choi C, Yun UJ, Hu Y, Yang SH, Coffinier C, Lee R, Yin L, Davies BS, Andres DA, Spielmann HP, Bennett CF, Young SG, “Activering van de synthese van progerine, de mutante prelamine A bij het Hutchinson-Gilford progeriasyndroom, met antisense-oligonucleotiden.” Hum Mol Genet. 17 april 2009.
Drs. Fong en Young ontvingen eerder subsidies van The Progeria Research Foundation.
Januari 2009: Kwantificering van de genexpressie van Progeria in normale en Progeria-cellen door een nieuwe, krachtige techniek.
Zweeds team vindt opbouw van progerine-RNA in normale cellen naarmate ze ouder worden
Progerine is het abnormale eiwit dat Progeria veroorzaakt. In de afgelopen jaren hebben verschillende onderzoeksgroepen ontdekt dat normale cellen ook progerine produceren, maar veel minder dan de cellen van een kind met Progeria. Bovendien neemt de hoeveelheid progerine-eiwit in normale cellen toe naarmate ze ouder worden in het laboratorium. Deze resultaten hebben een direct verband op cellulair niveau vastgesteld tussen Progeria en normale veroudering.
Dr. Maria Eriksson, auteur van de genbevinding voor Progeria in 2003, heeft nu een nieuwe, krachtige techniek uitgevonden om de expressie van het Progeria-gen kwantitatief te meten. Dr. Erikssons laboratorium aan het Karolinska Instituut in Zweden gebruikte de techniek om de hoeveelheid progerine-RNA in zowel normale als Progeria-cellen te meten. RNA is het blauwdrukmolecuul in onze cellen voor het maken van eiwitten. De Zweedse groep ontdekte dat zowel normale als Progeria-cellen steeds grotere hoeveelheden progerine-RNA aanmaken naarmate ze ouder worden. Erikssons resultaat toont aan dat het RNA-signaal voor het maken van progerine zich snel opbouwt in de cellen van kinderen met Progeria, en zich langzaam opbouwt gedurende een heel leven bij ons allemaal.
Deze nieuwe bevindingen versterken ons begrip van het verband tussen normale veroudering en Progeria. Bovendien wordt verwacht dat de nieuwe techniek op grote schaal zal worden gebruikt in experimenten die het mechanisme van progerine-actie onderzoeken.
Rodriguez S, Coppedè F, Sagelius H en Erikson M. “Verhoogde expressie van het Hutchinson-Gilford progeriasyndroom afgeknot lamin A-transcript tijdens celveroudering”. Europees tijdschrift voor menselijke genetica (2009), 1-10.
Augustus en oktober 2008: Is Progeria omkeerbaar? Twee recente publicaties laten zien dat FTI's en gentherapie dat wel eens kunnen doen!
Twee afzonderlijke onderzoeken tonen aan dat Progeria reversibel is in het cardiovasculaire systeem en de huid van muismodellen. De experimenten waren significant in het niet behandelen van de muizen totdat ze Progeria-symptomen vertoonden, terwijl de meeste eerdere onderzoeken met de behandeling begonnen voordat Progeria zichtbaar was. De productie van progerine (het schadelijke eiwit dat wordt gemaakt door het Progeria-gen) werd geremd door behandeling met een farnesyltransferaseremmer (FTI) of door het gen uit te schakelen. In beide gevallen keerden de muizen terug naar normale of bijna normale omstandigheden. Deze observaties leveren bemoedigend bewijs voor de huidige klinische proef met FTI's voor Progeria.
In een verbluffende demonstratie van de vooruitgang met het FTI-medicijn – dat nu in de Eerste klinische medicijnproef voor Progeria ooit – Het onderzoeksteam van Dr. Francis Collins bij de National Institutes of Health * ontdekte dat FTI's het meest verwoestende effect van Progeria bij muizen voorkwamen en zelfs terugdraaiden: hart- en vaatziekten.* "We waren verbaasd dat [het medicijn] zo goed werkte," zegt Francis Collins, een geneticus en voormalig directeur van het National Human Genome Research Institute, die hoofdauteur was van het onderzoeksteam dat de Progeria-genmutatie in 2003 identificeerde. "Dit medicijn voorkwam niet alleen dat deze muizen hart- en vaatziekten ontwikkelden, het draaide ook de schade terug bij muizen die al ziek waren."
De Progeria-muizen ontwikkelen hartziekten die lijken op die van kinderen met Progeria. De auteurs ontdekten dat de FTI zowel in staat was om de ontwikkeling van hartziekten tot op zekere hoogte te voorkomen wanneer muizen werden behandeld vanaf het moment dat ze werden gespeend, en gedeeltelijk de vastgestelde ziekte omkeerde wanneer muizen werden behandeld vanaf de leeftijd van 9 maanden. "Een van de opvallende dingen vanuit mijn perspectief was het vermogen om de ziekte om te keren", zei Collins, wat cruciaal is aangezien Progeria over het algemeen niet bij de geboorte wordt vastgesteld, maar pas wanneer kinderen symptomen beginnen te vertonen, wanneer een deel van de schade al is aangericht.
"Als deze medicijnen vergelijkbare effecten bij kinderen blijken te hebben, zou dit een grote doorbraak kunnen betekenen voor de behandeling van deze verwoestende ziekte", aldus Dr. Nabel van NHLBI, die medeauteur was van de studie. "Bovendien werpen deze bevindingen licht op de potentiële rol van FTI-medicijnen bij de behandeling van andere vormen van coronaire hartziekte."
Bekijk het artikel in Wetenschappelijk Amerikaans, “Nieuwe hoop voor progeria: medicijn voor zeldzame ouderdomsziekte”, op https://www.sciam.com/article.cfm?id=new-hope-for-progeria-drug-for-rare-aging-disease en het persbericht van de NIH op https://www.nih.gov/news/health/oct2008/nhgri-06.htm
* Capell, et al., “Een farnesyltransferase-remmer voorkomt zowel het begin als de late progressie van hart- en vaatziekten in een Progeria-muismodel.” Verhandelingen van de Nationale Academie van Wetenschappen, Vol. 105, nr. 41, 15902-15907 (14 oktober 2008)
In een tweede studie die online werd gepubliceerd in het Journal of Medical Genetics**, creëerde het onderzoeksteam van Dr. Maria Eriksson aan het Karolinska Institutet in Zweden een ander muizenmodel van Progeria met afwijkingen aan de huid en tanden. De muizen zijn genetisch gemanipuleerd zodat de Progeria-mutatie op elk moment kan worden uitgeschakeld. Zodra de ziekte zichtbaar werd, werd het gen voor Progeria uitgeschakeld. Na 13 weken was de huid bijna niet meer te onderscheiden van normale huid. Deze studie toont aan dat in deze weefsels de expressie van de Progeria-mutatie geen onomkeerbare schade veroorzaakt en dat het mogelijk is de ziekte om te keren, wat veelbelovend is voor de behandeling van Progeria.
**Eriksson, et. al., “Omkeerbaar fenotype in een muizenmodel van het Hutchinson-Gilford Progeria-syndroom.” J. Med. Genet. gepubliceerd online 15 aug. 2008; doi:10.1136/jmg.2008.060772
Om dit artikel te kopen, ga naar: https://jmg.bmj.com/cgi/rapidpdf/jmg.2008.060772v1
Meer bewijs voor het verband tussen progeria en normale veroudering en hartziekten
Deze opwindende Capell en Eriksson studies tonen aan dat deze resultaten, naast Progeria, het potentieel hebben om alle patiënten met hart- en vaatziekten te helpen. Onderzoekers hebben ontdekt dat het toxische eiwit dat verantwoordelijk is voor Progeria, in feite in lage niveaus wordt geproduceerd bij alle mensen, en zich mogelijk ophoopt naarmate we ouder worden. Dus door deze zeldzame kinderen te bestuderen, kunnen we ons begrip van een belangrijk mechanisme van menselijke veroudering vergroten - en misschien nieuwe manieren vinden om het proces te vertragen.
