מה חדש ב
מחקר פרוגריה
הוספנו סעיף זה כדי שתוכל לגשת בקלות למידע על הפרסומים המדעיים העדכניים ביותר והמשמעותיים ביותר על מחקר פרוגריה.
בנוסף למאמרים המודגשים להלן, יש כעת מאות מאמרים על פרוגריה ונושאים הקשורים לפרוג'ריה. אנו מציעים לך לחפש ב-PubMed כדי למצוא את הנושא/ים הספציפיים שאתה מחפש.
מרץ 2023: אבני דרך מחקר מרגשות בהערכת טיפול והארכת חיים!
אנו נרגשים לשתף אתכם בשני עדכוני מחקר מרגשים, שפורסמו באינטרנט היום בכתב העת הקרדיווסקולרי המוביל בעולם, תפוצה (1):
סמן ביולוגי בפרוג'ריה
דרך חדשה למדידת פרוגרין, החלבון הרעיל שגורם לפרוג'ריה, פותחה על ידי צוות בראשות מייסד שותף של PRF והמנהלת הרפואית, ד"ר לסלי גורדון. עם גילויו של הסמן הביולוגי הזה, המשתמש בפלזמה בדם למדידת רמות פרוגרין, חוקרים יכולים להבין כיצד טיפולים משפיעים על משתתפי הניסוי הקליני לאחר פרק זמן קצר יותר ובמספר נקודות לאורך כל ניסוי קליני.
בדיקה זו יכולה לייעל את תהליך הניסוי הקליני על ידי מתן מידע מוקדם על יעילות הטיפולים הנבדקים, כהובלה לבדיקות קליניות אחרות כגון עלייה במשקל, שינויים דרמטולוגיים, התכווצות ותפקוד מפרקים וכו', שלכולן נדרשות הרבה יותר זמן להתבטא. מאפיינים קליניים אלה של פרוגריה הם מדדים חשובים לטווח ארוך יותר של השפעות הטיפול, אשר כעת משלימים על ידי רמות הפרוג'רין שנמדדו מוקדם יותר בטיפול. ייתכן שכעת נוכל להבין את יתרונות הטיפול כבר ארבעה חודשים לאחר התחלת הטיפול, או להפסיק טיפול שאולי לא יועיל למשתתף בניסוי, כדי למנוע תופעות לוואי מיותרות.
חיים ארוכים אף יותר עם לונפרניב
בנוסף להאצת טיפול וגילויי ריפוי עתידיים, דרך חדשה וחדשנית זו למדידת פרוגרין מצביעה על כך שה התועלת לטווח ארוך של לונפרניב לילדים עם פרוגריה גדולה ממה שנקבע קודם לכן.
נתוני מחקר מצביעים על כך שרמות נמוכות יותר של פרוגרין בדם שיקפו תועלת הישרדותית: ככל שמישהו עם פרוגריה נשאר על לונפרניב, כך גדל היתרון ההישרדותי מהטיפול. רמות הפרוג'רין ירדו בכ-30-60% כל עוד התרופה נלקחה, ותוחלת החיים של חולים בטיפול מעל 10 שנים הוערכה לעלות בכמעט 5 שנים. זהו עלייה של יותר מ-35% בתוחלת החיים הממוצעת, מ-14.5 שנים לכמעט 20 שנים.!
למידע נוסף, עיין בהודעה לעיתונות שלנו כאן
"אחד הסיפורים המדהימים ביותר ששותפו אי פעם בפודקאסט הזה"
– ד"ר קרולין לאם, מומחית לב ידועה בעולם ומנחת הפודקאסט מחזור במנוסה, על המסע שהוביל לממצאים המרגשים הללו. שמע את הראיון המלא על ההשפעה העמוקה של מחקר זה ישירות מד"ר גורדון. לְהַקְשִׁיב כָּאן (החל מ-6:41).
שמע את ד"ר לסלי גורדון על הפודקאסט Circulation on the Run
וביוני, שני עיתוני מערכת (2) ו (3) פורסמו ב מַחזוֹר הדגשת החשיבות הקריטית של סמן ביולוגי זה לקידום הטיפולים והריפוי לילדים עם פרוגריה ולהבנה טובה יותר של הזדקנות.

(1) Gordon, LB, Norris, W., Hamren, S., et al. פלזמה פרוגרין בחולים עם תסמונת האצ'ינסון-גילפורד פרוגריה: פיתוח בדיקות אימונו והערכה קלינית. מַחזוֹר, 2023
(2) התקדמות הפרעות בלב בתסמונת פרוגריה האצ'ינסון-גילפורד: מחקר אורך פרוספקטיבי.
Olsen FJ, Gordon LB, Smoot L, Kleinman ME, Gerhard-Herman M, Hegde SM, Mukundan S, Mahoney T, Massaro J, Ha S, Prakash A. מַחזוֹר. 2023 יוני 6;147(23):1782-1784. doi: 10.1161/CIRCULATIONAHA.123.064370. Epub 2023 5 ביוני.
(3) כלים זמינים לזיהוי התקדמות פרוגרין ומחלות לב בתסמונת האצ'ינסון-גילפורד פרוגריה.
Eriksson M, Haugaa K, Revêchon G. מַחזוֹר. 2023 יוני 6;147(23):1745-1747. doi: 10.1161/CIRCULATIONAHA.123.064765. Epub 2023 5 ביוני.
מרץ 2021: פריצות דרך מרגשות ב-RNA Therapeutics for Progeria!
אנו נרגשים לחלוק את התוצאות מ שני מחקרים פורצי דרך מרגשים על השימוש בתרופות RNA במחקר פרוגריה. שני המחקרים מומנו על ידי The Progeria Research Foundation (PRF) ונכתבו על ידי המנהלת הרפואית של PRF, ד"ר לסלי גורדון.
פרוגרין הוא החלבון הגורם למחלה בפרוגריה. טיפולי ה-RNA מפריעים ליכולת הגוף לייצר פרוגרין, על ידי חסימת ייצורו ברמת ה-RNA. זה אומר ש הטיפול ספציפי יותר מרוב הטיפולים שמכוון לפרוגרין ברמת החלבון.
למרות שכל מחקר השתמש במערכת שונה למתן תרופות, שני המחקרים כוונו לאותה אסטרטגיית טיפול בסיסית, תוך עיכוב ייצור של RNA המקודד לחלבון החריג, פרוגרין. שניהם הובלו על ידי חוקרים מהמכונים הלאומיים לבריאות (NIH), ופורסמו היום בכתב העת רפואת טבע.
מחקר אחד, בראשות פרנסיס קולינס, MD, PhD, מנהל ה-NIH, הראה שטיפול בעכברי פרוגריה בתרופה בשם SRP2001 rחינך את ביטוי ה-mRNA והחלבון המזיק של פרוגרין באבי העורקים, העורק הראשי בגוף, כמו גם ברקמות אחרות. בסוף המחקר, דופן אבי העורקים נשאר חזק יותר והעכברים הפגינו א הישרדות מוגברת של מעל 60%.
"כדי שטיפול RNA ממוקד יראה תוצאות כה משמעותיות במודל של בעלי חיים נותן לי תקווה שזה יכול להוביל להתקדמות משמעותית בטיפול בפרוגריה", אמר קולינס.
ה מחקר אחר, בראשות טום מיסטלי, דוקטורט, מנהל המרכז לחקר הסרטן, המכון הלאומי לסרטן, NIH, הראה הפחתה של 90 - 95% של ה-RNA המייצר פרוגרין רעיל ברקמות שונות לאחר טיפול בתרופה בשם LB143. המעבדה של Misteli מצאה שהפחתת חלבון פרוגרין הייתה היעילה ביותר בכבד, עם שיפורים נוספים בלב ובאבי העורקים.
כעת אנו יודעים שישנן מספר דרכים להפחית את הייצור של חלבון הפרוגרין המזיק באמצעות תרופות RNA. כל מחקר מצא מתיחות שונות של RNA במודלים של העכברים, שכאשר התמקדו, סיפקו מסלול יעיל לטיפול, וכתוצאה מכך עכברי פרוגריה שחיו הרבה יותר מאלה שטופלו במחקרים קודמים עם זוקינבי (lonafarnib), התרופה היחידה שאושרה על ידי ה-FDA לילדים עם פרוגריה. יתר על כן, חוקרים מצאו שטיפול משולב עם תרופות RNA ו-Zokinvy (lonafarnib) הפחית את רמות חלבון הפרוגרין בכבד ובלב בצורה יעילה יותר מכל טיפול בודד בפני עצמו.
"שני המחקרים החשובים ביותר הללו מדגימים את התקדמות גדולה שעומדת בפנינו כעת בתחום טיפולי פרוגריה ממוקדים", אמרה המנהלת הרפואית של PRF, ד"ר לסלי גורדון. "התרגשתי לעבוד עם קבוצות המחקר המבריקות האלה כדי לקדם טיפול ב-RNA לילדים עם פרוגריה. שניהם מחקרים מרגשים של הוכחה לעיקרון, וכן PRF נרגש להתקדם לקראת ניסויים קליניים שמיישמים אסטרטגיות טיפול אלו.
—
Erdos, MR, Cabral, WA, Tavarez, UL et al. גישה טיפולית אנטי-סנס ממוקדת לתסמונת פרוגריה של האצ'ינסון-גילפורד. נאט מד (2021). https://doi.org/10.1038/s41591-021-01274-0
Puttaraju, M., Jackson, M., Klein, S. et al. סקר שיטתי מזהה אוליגונוקלאוטידים אנטי-סנס טיפוליים לתסמונת פרוגריה של Hutchinson-Gilford. נאט מד (2021). https://doi.org/10.1038/s41591-021-01262-4
ינואר 2021: התקדמות עריכה גנטית מדהימה בדגמי עכברי פרוגריה
כתב העת המדעי טֶבַע פרסמו תוצאות פורצות דרך הדגימה כי עריכה גנטית במודל עכבר של פרוגריה תיקנה את המוטציה שגורמת לפרוגריה בתאים רבים, שיפרה מספר תסמיני מחלה מרכזיים והגדילה באופן דרמטי את תוחלת החיים בעכברים.
במימון משותף של PRF ובשיתוף המנהלת הרפואית של PRF, ד"ר לסלי גורדון, המחקר מצא שעם זריקה אחת של עורך בסיס שתוכנת לתקן את המוטציה הגורמת למחלה, עכברים שרדו פי 2.5 יותר מאשר עכברי פרוגריה שלא טופלו. לגיל המקביל לתחילת הזקנה בעכברים בריאים. חשוב לציין, עכברים שטופלו שמרו גם על רקמת כלי דם בריאה - ממצא משמעותי, שכן אובדן שלמות כלי הדם הוא מנבא לתמותה בילדים עם פרוגריה.
המחקר הובל בשיתוף המומחה העולמי לעריכה גנטית, דיוויד ליו, PhD, ממכון Broad, MIT, ג'ונתן בראון, עוזר פרופסור לרפואה בחטיבה לרפואת לב וכלי דם באוניברסיטת ונדרבילט, ופרנסיס קולינס, MD, PhD, מנהל המכונים הלאומיים לבריאות.
"לראות את התגובה הדרמטית הזו במודל עכבר הפרוגריה שלנו הוא אחד הפיתוחים הטיפוליים המרגשים ביותר שהייתי חלק מהם מזה 40 שנה כרופא-מדען", אמר ד"ר קולינס.
"לפני חמש שנים, עדיין סיימנו את הפיתוח של עורך הבסיס הראשון", אמר ד"ר ליו. "אם היית אומר לי אז שבתוך חמש שנים, מנה בודדת של עורך בסיס יכולה לטפל בפרוגריה בבעל חיים ברמות ה-DNA, RNA, חלבון, פתולוגיה של כלי הדם ותוחלת החיים, הייתי אומר 'אין סיכוי'. זו עדות אמיתית למסירות של הצוות שאיפשר את העבודה הזו".
דרושים מחקרים פרה-קליניים נוספים כדי לחקור את התוצאות הללו, שאנו מקווים שיובילו יום אחד לניסוי קליני. קרא עוד על החדשות המרגשות האלה כאן וול סטריט ג'ורנל סָעִיף.
נובמבר 2020: אישור ה-FDA עבור lonafarnib (Zokinvy)
ב-20 בנובמבר 2020, PRF השיג חלק חשוב מהמשימה שלנו: lonafarnib, הטיפול הראשון אי פעם בפרוגריה, קיבל אישור FDA.
פרוגריה מצטרפת כעת לפחות מ-5% מהמחלות הנדירות עם טיפול המאושר על ידי ה-FDA.* ילדים ומבוגרים צעירים עם פרוגריה בארה"ב עשויים כעת לגשת ל-lonafarnib (המכונה כעת 'Zokinvy') על ידי מרשם, במקום באמצעות ניסוי קליני.
אבן דרך חשובה זו הגיעה הודות ל-13 שנים איתנות של מחקר שכללו ארבעה ניסויים קליניים, כולם בתיאום של PRF, שהתאפשרו על ידי הילדים האמיצים ומשפחותיהם, וממומנת על ידכם, קהילת התורמים הנפלאה של PRF.
לחץ כאן למידע נוסף.
*300 מחלות נדירות בעלות טיפול המאושר על ידי ה-FDA (https://www.rarediseases.info.nih.gov/diseases/FDS-orphan-drugs)/7,000 מחלות נדירות שהבסיס המולקולרי שלהן ידוע (www.OMIM. org) =4.2%
אפריל 2018: מחקר גלובלי שפורסם ב-JAMA מוצא טיפול עם Lonafarnib מאריך את ההישרדות בילדים עם פרוגריה
איגוד טיפול בלונפרניב לעומת אי טיפול עם שיעור תמותה בחולים עם תסמונת פרוגריה של האצ'ינסון-גילפורד, לסלי ב. גורדון, MD, PhD; הת'ר שאפל, דוקטורט; ג'ו מסארו, דוקטורט; Ralph B. D'Agostino Sr., PhD; ג'ואן ברזייר, MS; סוזן א. קמפבל, MA; מוניקה א. קליינמן, MD; מארק W. Kieran, MD, PhD; ג'אמה, 24 באפריל, 2018.
יולי 2016: תוצאות ניסוי משולש
אוקטובר 2014: המסע המדהים של PRF פורסם ב- Expert Opinion
 במאמר שפורסם ב חוות דעת מומחה ומחברת המנהלת המבצעת אודרי גורדון והמנהלת הרפואית לסלי גורדון, שני מנהיגי ה-PRF דנים בהיסטוריה, היעדים וההישגים של PRF, וכיצד תוכניות ה-PRF היו מרכזיות במסע מעורפל לטיפול.
במאמר שפורסם ב חוות דעת מומחה ומחברת המנהלת המבצעת אודרי גורדון והמנהלת הרפואית לסלי גורדון, שני מנהיגי ה-PRF דנים בהיסטוריה, היעדים וההישגים של PRF, וכיצד תוכניות ה-PRF היו מרכזיות במסע מעורפל לטיפול.
*"קרן המחקר פרוגריה: המסע המדהים שלה מאפלה לטיפול" 30 באוקטובר 2014
המחברים כותבים, "אנו תקוותנו שהתיאור של התוכניות והשירותים של ה-PRF שלאחר מכן, יחד עם תיאור של האופן שבו הם עוזרים ל-PRF להגשים את משימתו להציל ילדים עם פרוגריה, יסייעו ויעוררו אחרים לנקוט פעולה דומה עבור אוכלוסיות המחלות הנדירות הרבות שזקוקות לטיפול מיידי".
מאי 2014: מחקר מגלה שתרופות ניסוי מגדילות את תוחלת החיים המשוערת בילדים עם פרוגריה
מחקר זה מוכיח שיש ראיות לכך שמעכבי פרנסילטרנספראז (FTI) יכול להאריך את חייהם של ילדים עם פרוגריה לפחות בשנה וחצי. המחקר הראה הארכה של ההישרדות הממוצעת של 1.6 שנים במהלך שש השנים שלאחר התחלת הטיפול. שתי תרופות נוספות שנוספו בהמשך הניסויים, פרבסטטין וזולדרונאט, עשויות אף הן לתרום לממצא זה. זוהי העדות הראשונה לטיפולים המשפיעים על ההישרדות למחלה קטלנית זו.
לחץ כאן לפרטים נוספים.
ההשפעה של מעכבי פרנסילציה על הישרדות בתסמונת האצ'ינסון-גילפורד פרוגריה, לסלי ב' גורדון, ד"ר, דוקטורט, ג'ו מסארו, דוקטור, ראלף ב. ד'אגוסטינו האב, דוקטור, סוזן א. קמפבל, MA, ג'ואן ברזייר, MS, W. Ted Brown, MD, PhD, Monica E Kleinman, MD, Mark W. Kieran MD, PhD וה-Progeria Clinical Trials Collaborative; מַחזוֹר, 2 במאי 2014 (מקוון).
ספטמבר 2012: התגלה טיפול פרוגריה ראשון בפרוגריה
התוצאות של ניסוי התרופות הקליני הראשון אי פעם לילדים עם פרוגריה חושפים כי Lonafarnib, סוג של מעכב פרנסילטרנספראז (FTI) שפותח במקור לטיפול בסרטן, הוכח כיעיל עבור פרוגריה. כל ילד מראה שיפור באחת או יותר מארבע דרכים: עלייה במשקל נוסף, שמיעה טובה יותר, שיפור במבנה העצמות ו/או, והכי חשוב, גמישות מוגברת של כלי הדם. המחקר* מומן ומתואם על ידי The Progeria Research Foundation.
לחץ כאן לפרטים נוספים.
* גורדון ל.ב, Kleinman ME, Miller DT, Neuberg D, Giobbie-Hurder A, Gerhard-Herman M, Smoot L, Gordon CM, Cleveland R, Snyder BD, Fligor B, Bishop WR, Statkevich P, Regen A, Sonis A, Riley S, Ploski C, Correia A, Quinn N, Ullrich NJ, Nazarian A, Liang MG, Huh SY, שוורצמן A, Kieran MW, ניסוי קליני של מעכב פרנסילטרנספראז בילדים עם תסמונת פרוגריה של האצ'ינסון-גילפורד, הליכים של האקדמיה הלאומית למדעים, 9 באוקטובר 2012 כרך. 109 מס. 41 16666-16671
אוקטובר 2011: גישה חדשה לטיפול פרוגריה
כי ניתן למנוע שחבור חריג בתאי עור מתורבתים של פרוגריה באופן זה הוכח בשנת 2005 (2). עם זאת, לטיפול בחולים יש להעביר את המגיב המעכב שלם לכל רקמות החולה. נדרשו עוד שש שנים, ועבודה בכמה מעבדות, כדי לפתח את שיטות ה"מסירה" הללו.
במחקר החדש (1), חסימת השחבור השגוי בעכבר הדגם הביאה לתוצאות מרשימות. היו הפחתות ברורות בריכוזי הפרוג'רין בכל הרקמות שנותחו למעט שריר השלד, אשר עשוי להיות בעל ספיגה מופחתת של החומר החוסם. עכברי המודל חזרו על רבים מהפנוטיפים של חולי פרוגריה, כולל
- תוחלת החיים קיצרה מאוד (103 ימים לעומת שנתיים לעכברים מסוג פרא).
- הפחתת קצב הצמיחה.
- יציבה לא תקינה עם עקמומיות של עמוד השדרה.
- סטיות גרעיניות עמוקות כתוצאה מהצטברות פרוגרין.
- איבוד כללי של שכבת השומן מתחת לעור.
- שינויים עמוקים בעצמות.
- שינויים קרדיווסקולריים, כולל אובדן משמעותי של תאי שריר חלק של כלי הדם.
- שינויים בריכוזים של הורמונים שונים בפלסמת הדם במחזור, כולל אינסולין והורמון גדילה.
ה in vivo הדגמה של היעילות של הפחתת ייצור פרוגרין על ידי חסימת השחבור החריגה היא מועמדת חזקה לגישה חדשה ורב ערך לטיפול בפרוגריה.
(1) Osorio FG, Navarro CL, Cadiñanos J, López-Mejia IC, Quirós PM, et al, Science Translational Medicine, 3: גיליון 106, פרסום מקוון מראש, 26 באוקטובר (2011).
(2) Scaffidi, P. and Misteli, T. היפוך הפנוטיפ הסלולרי במחלת ההזדקנות המוקדמת של Hutchinson-Gilford progeria syndrome, Nature Medicine 11 (4): 440-445 (2005).
יוני 2011: מחקר במימון PRF מזהה Rapamycin כטיפול אפשרי לפרוגריה
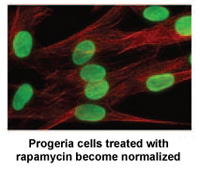
חוקרים מהמכונים הלאומיים לבריאות ובבית החולים הכללי של מסצ'וסטס בבוסטון, MA פרסמו מחקר חדש היום ב מדע, רפואה מתרגמת שעשוי להוביל לטיפול תרופתי חדש לילדים עם פרוגריה.*
רפמיצין היא תרופה שאושרה על ידי ה-FDA אשר הוכחה בעבר כמאריכה את חייהם של דגמי עכברים שאינם פרוגריה. מחקר חדש זה מדגים כי rapamycin מקטין את כמות החלבון פרוגרין הגורם למחלה ב-50%, משפר את הצורה הגרעינית החריגה ומאריך את תוחלת החיים של תאי פרוגריה. מחקר זה מספק את ההוכחה הראשונה לכך שרפמיצין עשוי להפחית את ההשפעות המזיקות של פרוגרין בילדים עם פרוגריה.
יש על זה סיקור תקשורתי אדיר! לחץ למטה לקישורים לכתבות במדיה:
בלוג הבריאות של וול סטריט ג'ורנל
קרן המחקר של פרוגריה שמחה לספק תאים לפרויקט זה מה- PRF Cell & Tissue Bank, ולעזור במימון המחקר דרך שלנו תוכנית מענקים.
מחקר חדש ומרגש זה מדגים את הקצב המדהים של מחקר הפרוגריה, תוך מתן תובנות נוספות לגבי תהליך ההזדקנות המשפיע על כולנו.
*"רפמיצין הופך את הפנוטיפים הסלולריים ומשפר את פינוי החלבון המוטנטי בתאי פרוגריה של האצ'ינסון-גילפורד"
קאן קאו, ג'ון ג'יי גרציוטו, ססיליה ד' בלייר, ג'וזף ר. מאצולי, מייקל אראדוס, דימיטרי קריינץ, פרנסיס ס. קולינס
Sci Transl Med. 2011 יוני 29;3(89):89ra58.
יוני 2011: מחקר פורץ דרך על קשר פרוגריה-הזדקנות
חדשות הערב של CBS, וול סטריט ג'ורנל ו אחרים דוח על מחקר חדש
חוקרי מכונים לאומיים לבריאות גילו קשר לא ידוע בעבר בין פרוגריה להזדקנות. הממצאים מספקים תובנות לגבי הקשר בין החלבון הרעיל, הגורם לפרוג'ריה, המכונה פרוגרין ו טלומרים, שמגנים על קצוות ה-DNA בתוך התאים עד שהם נשחקים עם הזמן והתאים מתים.
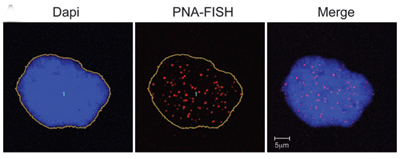
תאים המבטאים פרוגרין מאנשים נורמליים מראים סימנים של הזדקנות. DNA בגרעין נצבע בכחול. הטלומרים נתפסים כנקודות אדומות.
המחקר* מופיע במהדורה המקוונת המוקדמת של 13 ביוני 2011 של Journal of Clinical Investigation. היא מגיעה למסקנה שבהזדקנות רגילה, טלומרים קצרים או לא מתפקדים מעוררים תאים לייצר פרוגרין, הקשור לנזק לתאים הקשור לגיל.
"בפעם הראשונה, אנו יודעים שקיצור הטלומרים וחוסר תפקוד משפיעים על ייצור הפרוגרין", אומרת המנהלת הרפואית של קרן פרוגריה מחקר לסלי ב' גורדון, MD, PhD. "לכן שני התהליכים הללו, שניהם משפיעים על ההזדקנות הסלולרית, למעשה קשורים."
מחקרים קודמים הראו כי פרוגרין לא מיוצר רק בילדים עם פרוגריה, אלא שהוא מיוצר בכמויות קטנות יותר בכולנו, ורמות הפרוגרין עולות עם ההזדקנות. באופן עצמאי, מחקרים קודמים על קיצור טלומרים ותפקוד לקוי נקשרו להזדקנות נורמלית. מאז 2003, עם גילוי המוטציה בגן פרוגריה וחלבון הפרוג'רין הגורם למחלה, אחד מתחומי המחקר המרכזיים התמקד בהבנה האם וכיצד פרוגריה והזדקנות קשורים.
"החיבור של תופעת המחלה הנדירה הזו והזדקנות נורמלית מניב פרי בצורה חשובה", אמר מנהל NIH פרנסיס ס. קולינס, MD, PhD, מחבר בכיר של המאמר. "מחקר זה מדגיש שתובנות ביולוגיות יקרות ערך מתקבלות על ידי חקר הפרעות גנטיות נדירות כמו פרוגריה. התחושה שלנו מההתחלה הייתה שלפרוגריה יש הרבה מה ללמד אותנו על תהליך ההזדקנות הרגיל. "
מדענים חקרו באופן מסורתי טלומרים ופרוגרין בנפרד. למרות שעדיין יש הרבה מה ללמוד האם הקשר החדש הזה יכול להוביל לריפוי לילדים עם פרוגריה או להיות מיושם להארכת תוחלת החיים האנושית, מחקר זה מספק ראיות נוספות לכך שפרוגרין, החלבון הרעיל שהתגלה דרך מציאת המוטציה בגן בפרוגריה , ממלא תפקיד בתהליך ההזדקנות הרגיל.
*תפקוד לקוי של פרוגרין וטלומרים משתפים פעולה כדי לעורר הזדקנות תאית בפיברובלסטים אנושיים רגילים, Cao et al, J Clin Invest doi:10.1172/JCI43578.
לחץ כאן לטקסט המלא של ההודעה לעיתונות של NIH.
מאי 2011: התגלתה הגורם לתסמונת הפרוג'רואיד, מספקת תובנה נוספת לגבי הקשר של פרוגריה להזדקנות
צוות מחקר בראשות חוקר פרוגריה ד"ר קרלוס לופז-אוטין מאוניברסיטת אוביידו בספרד נתקלו בשתי משפחות שלילדיהן יש מחלת הזדקנות מואצת שלא הייתה ידועה בעבר בדומה לפרוג'ריה. הילדים לא הראו פגמים באף גנים שהיו קשורים בעבר למחלות פרוגרואיד, אך על ידי לימוד החלקים ה"מקודדים" של הגנום שלהם, הצוות מצא פגם בגן שנקרא BANF1. לבני משפחה עם מחלת הפרוג'רואיד היו כמויות נמוכות מאוד של החלבון שנוצר על ידי BANF1, ובדומה לאנשים עם פרוגריה, המעטפות הגרעיניות בתאים שלהם היו חריגות באופן ניכר. החריגות נעלמו בניסויים בתרבית תאים כאשר הגן הפגום הוחלף בגרסה הנכונה. הממצאים פורסמו ב- כתב העת האמריקאי לגנטיקה אנושית במאי 2011.
BANF1 מצטרף כעת לקבוצת הגנים הידועים שנראה כי משפיעים על צורות מסוימות של הזדקנות מוקדמת - וזה עשוי להשפיע גם על הזדקנות רגילה.
בשנים האחרונות, מדענים הצליחו להבין טוב יותר הזדקנות נורמלית ברמה מולקולרית, בין היתר הודות למחקרים על תסמונות הזדקנות מוקדמת כמו זו וכן פרוגריה, אשר "גורמות להתפתחות מוקדמת של מאפיינים הקשורים בדרך כלל לגיל מתקדם, "אמר לופז-אוטין. הוא הוסיף כי המחקר שלו "מדגיש את חשיבותה של הלמינה הגרעינית להזדקנות האדם ומדגים את התועלת של השיטות החדשות של רצף הגנום כדי לזהות את הגורם הגנטי למחלות נדירות והרסניות, שבאופן מסורתי קיבלו תשומת לב מוגבלת".
Xose S. Puente, Victor Quesada, Fernando G. Osorio, Rubén Cabanillas, Juan Cadiñanos, Julia M. Fraile, Gonzalo R. Ordónez, Diana A. Puente, Ana Gutiérrez-Fernández, Miriam Fanjul-Fernández et al. "רצף אקסומים וניתוח פונקציונלי מזהים מוטציית BANF1 כגורם לתסמונת פרוגרואיד תורשתית." American Journal of Human Genetics, 5 במאי 2011 DOI: 10.1016/j.ajhg.2011.04.010
אוגוסט 2010: גורם גדילה דמוי אינסולין 1 משפר את התסמינים, מאריך חיים בעכבר פרוגרואיד
ב-26 באוגוסט 2010, טרשת עורקים, פקקת וביולוגיה של כלי דם פורסמו אלקטרונית, לקראת ההדפסה, תוצאות מחקר המשווה בין פרוגריה לבין הזדקנות קרדיווסקולרית טיפוסית, שכותרתו "פתולוגיה קרדיווסקולרית בהאצ'ינסון-גילפורד פרוגריה: מתאם עם הפתולוגיה של כלי הדם של ההזדקנות". המחקר מצא כי פרוגרין, החלבון הלא תקין הגורם לפרוג'ריה, קיים גם בכלי הדם של האוכלוסייה הכללית ועולה עם הגיל, מה שמוסיף למקרה ההולך וגובר שיש הקבלות בין הזדקנות רגילה להזדקנות פרוגריה.
החוקרים בדקו נתיחות קרדיווסקולריות והתפלגות פרוגרין בחולים עם פרוגריה יחד עם קבוצה ללא פרוגריה בין הגילאים חודש עד 97 שנים, ומצאו כי פרוגרין אצל אנשים ללא פרוגריה עלה בממוצע ב-3.3 אחוזים בשנה בעורקים הכליליים.
"מצאנו קווי דמיון בין היבטים רבים של מחלות לב וכלי דם הן בפרוגריה והן בטרשת עורקים המשפיעה על מיליוני אנשים ברחבי העולם" אמרה ד"ר לסלי גורדון, מחברת הבכירה של המחקר והמנהלת הרפואית של קרן המחקר פרוגריה. "על ידי בחינת אחת המחלות הנדירות בעולם, אנו מקבלים תובנה מכרעת לגבי מחלה הפוגעת במיליוני אנשים ברחבי העולם. למחקר מתמשך יש פוטנציאל להשפיע משמעותית על ההבנה שלנו לגבי מחלות לב והזדקנות".
מחקר זה תומך באפשרות כי פרוגרין תורם לסיכון לטרשת עורקים באוכלוסייה הכללית, וראוי לבדיקה כתכונה חדשה פוטנציאלית כדי לסייע בניבוי סיכון למחלות לב.
אוליב M, Harten I, Mitchell R, Beers J, Djabali K, Cao K, Erdos MR, Blair C, Funke B, Smoot L, Gerhard-Herman M, Machan JT, Kutys R, Virmani R, Collins FS, Wight TN, Nabel EG, Gordon LB.
"פתולוגיה קרדיווסקולרית בהאצ'ינסון-גילפורד פרוגריה: מתאם עם הפתולוגיה של כלי הדם של ההזדקנות". Arterioscler Thromb Vasc Biol. 2010 Nov;30(11):2301-9; Epub 2010 26 באוגוסט.
מאי 2010: מחקרים באוקספורד מראים כיצד מחקר פרוגריה יכול לקדם את ההבנה שלנו לגבי הזדקנות נורמלית
המצב הזה דומה מאוד לזה שבפרוגריה. שם, פרלמין A (הנקרא פרוגרין) שומר על קבוצת הפרנסיל. ואכן, השלב הראשוני בגרימת המחלה הוא אי הסרת קבוצת הפרנסיל. כישלון זה קורה בגלל שמוטציית פרוג'ריה גורמת למחיקה של החלק של פרלמין A הדרוש ל-FACE 1 כדי לקשור ולהסיר את קבוצת הפרנסיל. לפיכך, הגורם לפגמים בהזדקנות ובפרוגריה זהים: FACE1 לא יכול לעשות את העבודה שלו.
זה ידוע מזה כמה שנים שמעכבי פרנסיל טרנספראז (FTIs) מעכבים (ויכולים להפוך) את נוכחותם של סמנים גרעיניים של מחלה בתאי פרוגריה. כעת, Shanahan וחב' מצאו ש-FTIs מעכבים הופעה של סמנים גרעיניים דומים בתאים מאנשים נורמליים מבוגרים. FTIs נמצאים כיום בשימוש בניסויים קליניים של Progeria ושנהאן וחב' מציינים כי ניסויים קליניים אלה "ישפכו אור נוסף על הפוטנציאל הטיפולי של תרופות אלו בטיפול בהזדקנות."
המחקרים המתוארים במאמר זה הם הדוגמה הטובה ביותר עד כה לאופן שבו מחקרים על פרוגריה מקדמים את ההבנה שלנו לגבי הזדקנות נורמלית.
Ragnauth CD, Warren DT, Liu Y, Shanahan CM וחב', "Prelamin A פועלת להאצת הזדקנות תאי שריר חלקים ומהווה סמן ביולוגי חדש של הזדקנות כלי דם אנושיים." תפוצה: 25 במאי 2010, עמ' 2200-2210.
אפריל 2010: עדות נוספת לכך שבפרוגריה, נוכחות קבוצת פרנסיל במולקולת הפרוגרין אחראית לתסמיני המחלה.
דייויס ועמיתים לעבודה הכינו עכבר דגם חדש שהפרלמין A שלו, בניגוד ל-RD פרלמין A, אינו פרנסילט, אבל כן שומר על רצף 15 חומצות האמינו שבדרך כלל מתפצל בנתיב לסנתז של lamin A. לעכבר זה אין תסמינים של פרוגרואיד, מה שמצביע על כך. שב-RD, כמו גם בפרוגריה, הנוכחות של קבוצת הפרנסיל, ולא שינוי ברצף חומצות האמינו, אחראית על תסמיני מחלה.
DaviesBS, Barnes RH 2nd, Tu Y, Ren S, Andres DA, Spielmann HP, Lammerding J, Wang Y, Young SG, Fong LG,
"הצטברות של פרלמין A לא פרנזילתי גורמת לקרדיומיופתיה אך לא לפרוגריה", הום מול ג'נט. 26 באפריל 2010. [Epub לפני ההדפסה]
פברואר 2010: עדויות נוספות FTI מספקות השפעות מועילות באמצעות פרנסילציה של פרוגרין
המחברים העריכו את האפשרות שההקלה של מחלת פרוגרואיד על ידי מעכב פרנסילטרנספראז (FTI) במודל עכבר של פרוגריה נובעת מהשפעת התרופה על פרנסילציה של חלבונים שאינם פרוגרין. הם בנו עכבר שיצר פרוגרין לא פרנסיל, אבל לא פרוגרין פרנסיל. עכבר זה פיתח גם פנוטיפים של מחלות דמויות פרוגריה, אך FTI לא שיפר אותם. תוצאה זו מצביעה על כך שהתרופה אינה פועלת על ידי עיכוב חלבונים מלבד פרוגרין; הוא חייב לפעול על הפרנסילציה של פרוגרין, הצעד הביוכימי שאינו קיים במודל הנבדק.
Yang SH, Chang SY, Andres DA, Spielmann HP, Young SG, Fong LG. "הערכת היעילות של מעכבי חלבון פרנסילטרנספראז במודלים של עכברים של פרוגריה."
J Lipid Res. 2010 פברואר;51(2):400-5. Epub 2009 26 באוקטובר.
אוקטובר 2009: האמנויות פוגשות את המדעים בסיפור בנג'מין כפתור
מלוני WJ, "תסמונת האצ'ינסון-גילפורד פרוגריה: הצגתה בסיפור הקצר של פ. סקוט פיצג'רלד 'המקרה המוזר של בנג'מין באטון' והביטויים שלו בעל פה."
ג'יי דנט. מילון 2009 אוקטובר 88 (10): 873-6
מאי 2009: מאמר פורץ דרך בנושא השפעת HGPS על תפקודים סלולריים.
HGPS הוכח בעבר כמשפיע על תפקודים תאיים בסיסיים רבים, כולל שכפול, ביטוי גנים ותיקון DNA. בוש ועמיתיו הוסיפו לרשימה זו את ההובלה של חלבונים מהציטופלזמה לגרעין. כל החלבונים מסונתזים בציטופלזמה, ואלו שבסופו של דבר נמצאים בגרעין צריכים לעבור את הממברנה הגרעינית. ההובלה מתבצעת דרך תעלות בממברנה הגרעינית הנקראות "נקבוביות גרעיניות". חלבונים רבים גדולים מכדי פשוט להתפזר דרך הנקבוביות הגרעיניות, אך "מודרכים" דרכם על ידי חלבונים מיוחדים שהתפתחו למטרה זו. במאמר זה, תאים המבטאים את הגן המוטנטי האחראי על HGPS נמצאו כבעלי הובלה מופחתת של חלבונים לתוך הגרעינים על ידי מדידה ישירה.
Busch A, Kiel T, Heupel WM, Wehnert M, Huebner S., "יבוא חלבון גרעיני מופחת בתאים המבטאים מוטציות למינ A הגורמות למעטפת גרעינית." Exp Cell Res. 11 במאי 2009.
אפריל 2009: קישור פרוגריה והזדקנות רגילה: תובנות חדשות
← מתן מבנה וארגון: ארכיטקטורה גרעינית ושלמות הגנום
→ נזק ל-DNA ותיקון השתבשו
→ ישנים ומעבר לתיקון מדכאי גידולים והזדקנות תאית, ו
← התחדשות והתחדשות: ביולוגיה של תאי גזע. התחדשות והתחדשות: ביולוגיה של תאי גזע.
המאמר מדגיש את הדרכים שבהן ההתקדמות האחרונה בחקר מחלות פרוגרואיד נותנת תובנות לגבי תפקודים תאיים בסיסיים כמו גם הזדקנות.
Capell BS, Tlougan BE, Orlow SJ, "מהנדיר ביותר לנפוץ ביותר: תובנות מתסמונות פרוגרואיד לסרטן העור והזדקנות." כתב עת לדרמטולוגיה חוקרת (23 באפריל 2009), 1-11
אפריל 2009: מענקי מחקר PRF בעבר מפתחים שיטה חדשה לחקר פרוגרין בתאים
ניסויים קודמים עם תאי פיברובלסט מחולי פרוגריה הראו שהנזק שנגרם על ידי המוטציה הוא תחילה תוצאה של פעולה של הצורה המשונה של למין A, הנקראת פרוגרין. אבל הפרשנות של ניסויים אלה יכולה להיות קשה בתרבות במשך מספר משתנה של דורות. פונג et. אל. הקימו מערכת ניסיונית שבה הכמות של פרוגרין ב מסוג פראי ניתן להגדיל או להקטין תאים. שיטה זו תאפשר לחוקרים למיין את ההשפעות הישירות של פרוגרין מאלה משניות, ובכך לקדם את חקר המנגנונים התאיים המובילים לפתופיזיולוגיה של תאי פרוגריה.
הפעלת הסינתזה של פרוגרין, הפרלמין A המוטנטי בתסמונת פרוגריה Hutchinson-Gilford, עם אוליגונוקלאוטידים אנטי-סנס. (מאמר ב-PubMed) פונג LG, Vickers TA, Farber EA, Choi C, Yun UJ, Hu Y, Yang SH, Coffinier C, Lee R, Yin L, Davies BS, Andres DA, Spielmann HP, Bennett CF, Young SG , "הפעלת הסינתזה של פרוגרין, הפרלמין A המוטנטי בתסמונת פרוגריה האצ'ינסון-גילפורד, עם אנטי-סנס אוליגונוקלאוטידים." הום מול ג'נט. 17 באפריל 2009.
דרס. פונג ויאנג מומנו בעבר באמצעות מענקים מ-The Progeria Research Foundation.
ינואר 2009: כימות של ביטוי גנים פרוגריה בתאים נורמליים ופרוגריה על ידי טכניקה חדשה וחזקה.
הצוות השבדי מוצא הצטברות של פרוגרין RNA בתאים נורמליים ככל שהם מתבגרים
פרוגרין הוא החלבון הלא תקין הגורם לפרוגריה. בשנים האחרונות, מספר קבוצות מחקר מצאו שתאים נורמליים מייצרים גם פרוגרין, אבל הרבה פחות מתאי ילד עם פרוגריה. יתרה מכך, כמות חלבון הפרוגרין בתאים נורמליים עולה ככל שהם מזדקנים במעבדה. תוצאות אלו יצרו קשר ישיר ברמה התאית בין פרוגריה להזדקנות נורמלית.
ד"ר מריה אריקסון, מחברת מציאת הגנים לפרוגריה ב-2003, המציאה כעת טכניקה חדשה וחזקה למדידה כמותית של הביטוי של הגן פרוגריה. המעבדה של ד"ר אריקסון במכון קרולינסקה בשבדיה השתמשה בטכניקה למדידת כמות הפרוגרין RNA הן בתאי נורמלי והן בתאי פרוגריה. RNA היא מולקולת השרטוט בתאים שלנו לייצור חלבון. הקבוצה השוודית מצאה שגם תאי פרוגריה ונורמליים מייצרים כמויות גדולות יותר ויותר של פרוגרין RNA ככל שהם מתבגרים. התוצאה של אריקסון מראה שאות ה-RNA לייצור פרוגרין נבנה במהירות בתאים של ילדים עם פרוגריה, ונבנה לאט במשך כל החיים בכולנו.
ממצאים חדשים אלו מחזקים את ההבנה שלנו לגבי הקשר בין הזדקנות נורמלית לפרוגריה. בנוסף, הטכניקה החדשה צפויה להיות בשימוש נרחב בניסויים העוסקים במנגנון הפעולה של פרוגרין.
Rodriguez S, Coppedè F, Sagelius H ו- Erikson M. "התבטאות מוגברת של תסמונת האצ'ינסון-גילפורד פרוגריה קטועה lamin A תמליל במהלך הזדקנות התא". כתב העת האירופי לגנטיקה אנושית (2009), 1-10.
אוגוסט ואוקטובר 2008: האם פרוגריה הפיכה? שני פרסומים אחרונים מראים ש-FTIs וריפוי גנטי עשויים לעשות בדיוק את זה!
שני מחקרים נפרדים מראים כי פרוגריה הפיכה במערכת הלב וכלי הדם ובעור של דגמי עכברים. הניסויים היו משמעותיים בכך שלא טיפלו בעכברים עד שהם הביעו תסמיני פרוגריה, בעוד שרוב המחקרים הקודמים החלו טיפול לפני שהפרוגריה הופיעה. ייצור פרוגרין (החלבון המזיק העשוי מהגן פרוגריה) עוכב או על ידי טיפול במעכב פרנסיל טרנספראז (FTI) או על ידי כיבוי הגן. בשני המקרים העכברים חזרו למצב נורמלי או כמעט נורמלי. תצפיות אלו מספקות ראיות מעודדות לניסוי הקליני הנוכחי של FTIs עבור פרוגריה.
בתצוגה מדהימה של התקדמות עם תרופת FTI - שנמצאת כעת בשימוש ב- ניסוי תרופות קליני פרוגריה הראשון אי פעם – צוות המחקר של ד"ר פרנסיס קולינס במכון הלאומי לבריאות * מצא ש-FTI מנעו ואף הפכו את ההשפעה ההרסנית ביותר של פרוגריה בעכברים: מחלות לב וכלי דם.* "נדהמנו ש[התרופה] עבדה כל כך טוב", אומר פרנסיס קולינס, גנטיקאי ומנהל לשעבר של המכון הלאומי לחקר הגנום האנושי, שהיה מחבר בכיר של צוות המחקר שזיהה את המוטציה בגן פרוגריה ב-2003. "לא רק התרופה הזו מונעת מהעכברים האלה לפתח מחלות לב וכלי דם, היא הפכה את הנזק בעכברים שכבר חלו במחלה".
עכברי הפרוגריה מפתחים מחלת לב המשקפת את זו של ילדים עם פרוגריה. המחברים מצאו שה-FTI הצליח גם למנוע התפתחות של מחלות לב במידה מסוימת כאשר עכברים טופלו מרגע הגמילה, וגם להפוך חלקית מחלה מבוססת כאשר עכברים טופלו החל מגיל 9 חודשים. "אחד הדברים הבולטים מנקודת המבט שלי הייתה היכולת להפוך את המחלה", אמר קולינס, וזה קריטי בהתחשב בכך שפרוגריה בדרך כלל לא מאובחנת בלידה, אלא רק כאשר ילדים מתחילים להראות תסמינים, כאשר חלק מהנזק כבר אובחן. נַעֲשָׂה.
"אם יתגלו לתרופות אלו השפעות דומות בילדים, הדבר עשוי לסמן פריצת דרך משמעותית לטיפול במחלה ההרסנית הזו", אמר ד"ר נאבל מ-NHLBI, שהיה שותף למחקר. "בנוסף, ממצאים אלה שופכים אור על התפקיד הפוטנציאלי של תרופות FTI לטיפול בצורות אחרות של מחלת עורקים כליליים."
צפו במאמר ב סיינטיפיק אמריקן, "תקווה חדשה לפרוגריה: תרופה למחלת הזדקנות נדירה", ב https://www.sciam.com/article.cfm?id=new-hope-for-progeria-drug-for-rare-aging-disease וההודעה לעיתונות של NIH ב https://www.nih.gov/news/health/oct2008/nhgri-06.htm
* קאפל, et. אל, "מעכב פרנסילטרנספראז מונע הן את הופעתה והן את ההתקדמות המאוחרת של מחלות לב וכלי דם במודל עכבר פרוג'ריה". הליכים של האקדמיה הלאומית למדעים, כרך יד. 105, לא. 41, 15902-15907 (14 באוקטובר, 2008)
במחקר שני שפורסם באינטרנט ב-Journal of Medical Genetics**, צוות המחקר של ד"ר מריה אריקסון במכון קרולינסקה בשוודיה יצר מודל עכבר נוסף של פרוגריה עם מומים בעור ובשיניים. העכברים מהונדסים גנטית כך שניתן לכבות את המוטציה של פרוגריה בכל עת. ברגע שהמחלה התגלתה, הגן לפרוגריה כובה. לאחר 13 שבועות כמעט לא ניתן היה להבחין בין העור לעור רגיל. מחקר זה מראה כי ברקמות אלו הביטוי של מוטציית פרוגריה אינו גורם לנזק בלתי הפיך וכי היפוך המחלה אפשרי, מה שנותן הבטחה לטיפול בפרוגריה.
**אריקסון, et. אל., "פנוטיפ הפיך במודל עכבר של תסמונת האצ'ינסון-גילפורד פרוגריה." J. Med. ג'נט. פורסם באינטרנט ב-15 באוגוסט 2008; doi:10.1136/jmg.2008.060772
לרכישת מאמר זה, עבור אל: https://jmg.bmj.com/cgi/rapidpdf/jmg.2008.060772v1
עדויות נוספות לקשר בין פרוגריה להזדקנות נורמלית ומחלות לב
מחקרים מרגשים אלה של קאפל ואריקסון מראים שמעבר לפרוגריה, לתוצאות אלו יש פוטנציאל להועיל לכל החולים עם מחלות לב וכלי דם. חוקרים גילו שהחלבון הרעיל שאחראי לפרוגריה מיוצר למעשה ברמות נמוכות בכל בני האדם, ואולי מצטבר ככל שאנו מתבגרים. לפיכך, על ידי לימוד הילדים הנדירים הללו, נוכל לקדם את ההבנה שלנו לגבי מנגנון עיקרי של הזדקנות אנושית - ואולי למצוא דרכים חדשות להאט את התהליך.
