Что нового в
Исследования прогерии
Мы добавили этот раздел, чтобы вы могли легко получить доступ к информации о последних и наиболее значимых научных публикациях по исследованию прогерии.
В дополнение к статьям, выделенным ниже, теперь есть сотни статей о прогерии и связанных с прогерией темах. Мы предлагаем вам поискать в PubMed, чтобы найти конкретную тему(ы), которую вы ищете.
Март 2023 г.: захватывающие вехи исследований в области оценки лечения и продления жизни!
Мы рады поделиться с вами двумя захватывающими результатами исследований, опубликованными сегодня в ведущем в мире журнале по сердечно-сосудистым заболеваниям. Тираж (1):
Биомаркер при прогерии
Новый способ измерения прогерина, токсичного белка, вызывающего прогерию, был разработан группой под руководством соучредителя PRF и медицинского директора доктора Лесли Гордона. С открытием этого биомаркера, который использует плазму крови для измерения уровня прогерина, Исследователи могут понять, как лечение влияет на участников клинических испытаний, спустя более короткий промежуток времени и на нескольких этапах каждого клинического испытания.
Этот тест может оптимизировать процесс клинических испытаний путем предоставление ранней информации об эффективности тестируемых методов лечения, как ввод к другим клиническим тестам, таким как набор веса, дерматологические изменения, контрактура и функция суставов и т. д., все из которых требуют гораздо больше времени для проявления. Эти клинические признаки прогерии являются важными долгосрочными мерами эффектов лечения, которые теперь дополняются уровнями прогерина, измеренными на ранних стадиях терапии. Теперь мы можем понять преимущества лечения уже через четыре месяца после начала лечения или прекратить лечение, которое может не принести пользы участнику испытания, чтобы избежать ненужных побочных эффектов.
Еще более долгая жизнь с лонафарнибом
Помимо ускорения будущих открытий в области лечения и излечения, этот новый и инновационный способ измерения прогерина указывает на то, что Долгосрочная польза лонафарниба для детей с прогерией больше, чем предполагалось ранее.
Данные исследования показывают, что более низкие уровни прогерина в крови отражают преимущества выживания: чем дольше человек с прогерией принимал лонафарниб, тем больше преимуществ выживания от терапии. Уровни прогерина снижались примерно на 30-60% в течение всего времени приема препарата, а ожидаемая продолжительность жизни пациентов, находящихся на лечении более 10 лет, по оценкам, увеличивалась почти на 5 лет. Это более чем 35% увеличение средней продолжительности жизни, с 14,5 лет до почти 20 лет!
Чтобы узнать больше, ознакомьтесь с нашим пресс-релизом здесь.
«Одна из самых замечательных историй, когда-либо рассказанных в этом подкасте»
– Доктор Кэролин Лэм, всемирно известный специалист по болезням сердца и ведущая подкаста Циркуляция на ходу, о путешествии, которое привело к этим захватывающим открытиям. Послушайте полное интервью о глубоком влиянии этого исследования непосредственно от доктора Гордона. Слушать здесь (начиная с 6:41).
Послушайте подкаст доктора Лесли Гордона о циркуляции на бегу
А в июне вышли две редакционные статьи (2) и (3) были опубликованы в Циркуляция подчеркивая решающее значение этого биомаркера для совершенствования методов лечения и излечения детей с прогерией, а также для лучшего понимания процессов старения.

(1) Гордон, Л.Б., Норрис, В., Хамрен, С., и др.. Плазменный прогерин у пациентов с синдромом прогерии Хатчинсона-Гилфорда: разработка иммуноферментного анализа и клиническая оценка. Циркуляция, 2023
(2) Прогрессирование сердечных аномалий при синдроме прогерии Хатчинсона-Гилфорда: проспективное лонгитюдное исследование.
Олсен Ф.Дж., Гордон Л.Б., Смут Л., Кляйнман М.Э., Герхард-Херман М., Хегде С.М., Мукундан С., Махони Т., Массаро Дж., Ха С., Пракаш А. Циркуляция. 2023 6 июня;147(23):1782-1784. doi: 10.1161/CIRCULATIONAHA.123.064370. Epub 2023 5 июня.
(3) Доступные инструменты для обнаружения прогерина и прогрессирования заболеваний сердца при синдроме прогерии Хатчинсона-Гилфорда.
Эрикссон М., Хаугаа К., Ревечон Г. Циркуляция. 2023 6 июня;147(23):1745-1747. doi: 10.1161/CIRCULATIONAHA.123.064765. Epub 2023 5 июня.
Март 2021 г.: захватывающие прорывы в РНК-терапии прогерии!
Мы рады поделиться результатами два очень интересных прорывных исследования по использованию РНК-терапии в исследовании прогерии. Оба исследования были совместно профинансированы Фондом исследований прогерии (PRF) и соавтором выступил медицинский директор PRF, доктор Лесли Гордон.
Прогерин — это болезнетворный белок при прогерии. Терапия РНК нарушает способность организма вырабатывать прогерин, блокируя его выработку на уровне РНК. Это означает, что лечение более специфично, чем большинство терапий которые воздействуют на прогерин на уровне белка.
Хотя каждое исследование использовало различную систему доставки лекарств, оба исследования были нацелены на одну и ту же базовую стратегию лечения, ингибируя производство РНК, кодирующей аномальный белок, прогерин. Оба исследования проводились исследователями из Национальных институтов здравоохранения (NIH) и были опубликованы сегодня в журнале Природная медицина.
Одно исследованиепод руководством Фрэнсиса Коллинза, доктора медицины, доктора философии, директора NIH, показали, что лечение мышей с прогерией препаратом под названием SRP2001 rвыявили вредную экспрессию мРНК и белка прогерина в аорте, главная артерия в организме, а также в других тканях. В конце исследования стенка аорты оставалась более прочной, и мыши продемонстрировали увеличение выживаемости более 60%.
«То, что таргетная РНК-терапия показала столь значительные результаты на животных моделях, дает мне надежду, что это может привести к значительному прогрессу в лечении прогерии», — сказал Коллинз.
The другое исследованиепод руководством Тома Мистели, доктора философии, директора Центра исследований рака Национального института рака (NIH), продемонстрировали 90 – 95% снижение токсичной прогерин-продуцирующей РНК в различных тканях после лечения препаратом LB143. Лаборатория Мистели обнаружила, что снижение белка прогерина было наиболее эффективным в печени, с дополнительными улучшениями в сердце и аорте.
Теперь мы знаем, что существует множество способов уменьшить производство вредного белка прогерина с помощью РНК-терапии. Каждое исследование обнаружило различные участки РНК в мышиных моделях, которые при воздействии на них обеспечивали эффективный путь лечения, что приводило к Мыши с прогерией, которые жили намного дольше, чем те, которых лечили Зокинви (лонафарниб) в предыдущих исследованиях., единственный одобренный FDA препарат для детей с прогерией. Кроме того, исследователи обнаружили, что комбинированное лечение с РНК-терапией и Зокинви (лонафарниб) снижает уровень белка прогерина в печени и сердце более эффективно, чем каждое из этих отдельных средств.
«Эти два чрезвычайно важных исследования демонстрируют основные достижения, которые сейчас нас ждут в области целенаправленной терапии прогерии», — сказал медицинский директор PRF, доктор Лесли Гордон. «Я был взволнован работой с этими блестящими исследовательскими группами по продвижению РНК-терапии для детей с прогерией. Оба исследования являются захватывающими исследованиями, подтверждающими принцип, и PRF с нетерпением ждет начала клинических испытаний которые применяют эти стратегии лечения.
—
Эрдос, MR, Кабрал, Вашингтон, Таварес, UL и др. Целенаправленный антисмысловой терапевтический подход при синдроме прогерии Хатчинсона–Гилфорда. Нат Мед (2021). https://doi.org/10.1038/s41591-021-01274-0
Путтараджу М., Джексон М., Кляйн С. и др. Систематический скрининг выявляет терапевтические антисмысловые олигонуклеотиды для синдрома прогерии Хатчинсона–Гилфорда. Нат Мед (2021). https://doi.org/10.1038/s41591-021-01262-4
Январь 2021 г.: Заметный прогресс в генетическом редактировании на моделях мышей с прогерией
Научный журнал Природа опубликованные прорывные результаты продемонстрировав, что генетическое редактирование в мышиной модели прогерии исправило мутацию, вызывающую прогерию во многих клетках, улучшило несколько ключевых симптомов заболевания и значительно увеличило продолжительность жизни мышей.
Исследование, софинансируемое PRF и соавтором которого является медицинский директор PRF доктор Лесли Гордон, показало, что при однократной инъекции редактора оснований, запрограммированного на исправление мутации, вызывающей заболевание, мыши жили в 2,5 раза дольше, чем контрольные мыши с прогерией, не проходившие лечение, до возраста, соответствующего началу старости у здоровых мышей. Важно, что пролеченные мыши также сохранили здоровую сосудистую ткань — важное открытие, поскольку потеря целостности сосудов является предиктором смертности у детей с прогерией.
Исследование проводилось под совместным руководством мирового эксперта в области генетического редактирования Дэвида Лю, доктора философии из Института Брода Массачусетского технологического института, Джонатана Брауна, доцента кафедры сердечно-сосудистой медицины Университета Вандербильта, и Фрэнсиса Коллинза, доктора медицины, доктора философии, директора Национальных институтов здравоохранения.
«Наблюдение столь впечатляющей реакции на нашей модели прогерии у мышей является одним из самых захватывающих терапевтических достижений, в которых я принимал участие за 40 лет работы врачом-ученым», — сказал доктор Коллинз.
«Пять лет назад мы все еще заканчивали разработку самого первого редактора оснований», — сказал доктор Лю. «Если бы вы сказали мне тогда, что в течение пяти лет одна доза редактора оснований может воздействовать на прогерию у животного на уровнях ДНК, РНК, белка, сосудистой патологии и продолжительности жизни, я бы сказал: «Нет никакого способа». Это настоящее свидетельство преданности команды, которая сделала эту работу возможной».
Для изучения этих результатов необходимы дополнительные доклинические исследования, которые, как мы надеемся, однажды приведут к клиническим испытаниям. Подробнее об этой захватывающей новости читайте в этом Уолл Стрит Джорнал статья.
Ноябрь 2020 г.: одобрение FDA препарата лонафарниб (Зокинви)
20 ноября 2020 года PRF выполнила важную часть своей миссии: лонафарниб, первое в истории средство лечения прогерии, получил одобрение FDA.
Прогерия теперь присоединилась к менее чем 5% редким заболеваниям, для лечения которых FDA одобрило лечение.* Дети и молодые люди с прогерией в США теперь могут получить доступ к лонафарнибу (теперь называемому «Зокинви») по рецепту, а не через клиническое исследование.
Эта знаменательная веха стала возможной благодаря 13 годам упорных исследований, включавших четыре клинических испытания, все из которых координировались PRF, стали возможными благодаря мужественным детям и их семьям и профинансированы вами, замечательным сообществом доноров PRF.
кликните сюда для получения более подробной информации.
*300 редких заболеваний, для которых существует одобренное FDA лечение (https://www.rarediseases.info.nih.gov/diseases/FDS-orphan-drugs)/7000 редких заболеваний, для которых известна молекулярная основа (www.OMIM.org) =4.2%
Апрель 2018 г.: Глобальное исследование, опубликованное в JAMA, показывает, что лечение лонафарнибом увеличивает выживаемость детей с прогерией
Кликните сюда для более подробной информации.
Связь лечения лонафарнибом по сравнению с отсутствием лечения с уровнем смертности у пациентов с синдромом прогерии Хатчинсона-Гилфорда, Лесли Б. Гордон, доктор медицины, доктор философии; Хизер Шеппелл, доктор философии; Джо Массаро, доктор философии; Ральф Б. Д'Агостино-старший, доктор философии; Джоан Брейзиер, магистр наук; Сьюзан Э. Кэмпбелл, магистр наук; Моника Э. Кляйнман, доктор медицины; Марк В. Киран, доктор медицины, доктор философии; ДЖАМА, 24 апреля 2018 г.
Июль 2016 г.: результаты тройного испытания
Октябрь 2014 г.: замечательное путешествие PRF опубликовано в журнале Expert Opinion
 В статье, опубликованной в Мнение эксперта Авторами статьи являются исполнительный директор Одри Гордон и медицинский директор Лесли Гордон. В ней два руководителя PRF обсуждают историю PRF, ее цели и достижения, а также то, как программы PRF сыграли решающую роль на пути от безвестности к лечению.
В статье, опубликованной в Мнение эксперта Авторами статьи являются исполнительный директор Одри Гордон и медицинский директор Лесли Гордон. В ней два руководителя PRF обсуждают историю PRF, ее цели и достижения, а также то, как программы PRF сыграли решающую роль на пути от безвестности к лечению.
*«Фонд исследований прогерии: его замечательный путь от безвестности к лечению» 30 октября 2014 г.
Авторы пишут: «Мы надеемся, что приведенное ниже описание программ и услуг PRF, а также рассказ о том, как они помогают PRF выполнять свою миссию по спасению детей с прогерией, помогут и вдохновят других предпринять аналогичные действия в отношении многих групп населения с редкими заболеваниями, которым требуется немедленное внимание».
Май 2014 г.: исследование показало, что пробные препараты увеличивают предполагаемую продолжительность жизни детей с прогерией
Это исследование демонстрирует, что есть доказательства того, что ингибитор фарнезилтрансферазы (FTI) может продлить жизнь детей с прогерией по крайней мере на полтора года. Исследование показало продление средней выживаемости на 1,6 года в течение шести лет после начала лечения. Два дополнительных препарата, добавленных позже в испытания, правастатин и золедронат, также могут способствовать этому открытию. Это первое доказательство того, что методы лечения влияют на выживаемость при этом смертельном заболевании.
кликните сюда для более подробной информации.
Влияние ингибиторов фарнезилирования на выживаемость при синдроме прогерии Хатчинсона-Гилфорда, Лесли Б. Гордон, доктор медицины, доктор философии, Джо Массаро, доктор философии, Ральф Б. Д'Агостино-старший, доктор философии, Сьюзан Э. Кэмпбелл, магистр наук, Джоан Брейзиер, магистр наук, У. Тед Браун, доктор медицины, доктор философии, Моника Э. Кляйнман, доктор медицины, Марк У. Киран, доктор медицины, доктор философии и совместные клинические испытания прогерии; Циркуляция, 2 мая 2014 г. (онлайн).
Сентябрь 2012 г.: Открыто первое в истории лечение прогерии
Результаты первое в истории клиническое исследование препарата для детей с прогерией показывают, что лонафарниб, тип ингибитора фарнезилтрансферазы (FTI), изначально разработанный для лечения рака, оказался эффективным при прогерии. Каждый ребенок показал улучшение в одном или нескольких из четырех способов: набор дополнительного веса, улучшение слуха, улучшение структуры костей и/или, что наиболее важно, повышение гибкости кровеносных сосудов. Исследование* финансировалось и координировалось The Progeria Research Foundation.
кликните сюда для более подробной информации.
*Гордон Л.Б., Kleinman ME, Miller DT, Neuberg D, Giobbie-Hurder A, Gerhard-Herman M, Smoot L, Gordon CM, Cleveland R, Snyder BD, Fligor B, Bishop WR, Statkevich P, Regen A, Sonis A, Riley S, Ploski C, Correia A, Quinn N, Ullrich NJ, Nazarian A, Liang MG, Huh SY, Schwartzman A, Kieran MW, Клиническое исследование ингибитора фарнезилтрансферазы у детей с синдромом прогерии Хатчинсона-Гилфорда, Труды Национальной академии наук, 9 октября 2012 г. т. 109 № 41 16666-16671
Октябрь 2011 г.: Новый подход к терапии прогерии
То, что аберрантный сплайсинг в культивируемых клетках кожи Progeria может быть предотвращен таким образом, было показано в 2005 году (2). Однако для лечения пациентов ингибирующий реагент должен быть доставлен в целости и сохранности во все ткани пациента. Потребовалось еще шесть лет и работа в нескольких лабораториях, чтобы разработать эти методы «доставки».
В новом исследовании (1) блокирование аберрантного сплайсинга у модельной мыши привело к впечатляющим результатам. Было отмечено явное снижение концентрации прогерина во всех проанализированных тканях, за исключением скелетных мышц, которые могут иметь сниженное поглощение блокирующего агента. Модельные мыши повторили многие фенотипы пациентов с прогерией, включая
- Значительно сокращенная продолжительность жизни (103 дня по сравнению с 2 годами у мышей дикого типа).
- Снижение темпов роста.
- Неправильная осанка с искривлением позвоночника.
- Глубокие ядерные аберрации в результате накопления прогерина.
- Общая потеря жирового слоя под кожей.
- Глубокие изменения костей.
- Изменения сердечно-сосудистой системы, включая значительную потерю гладкомышечных клеток сосудов.
- Изменения концентрации различных гормонов в циркулирующей плазме крови, включая инсулин и гормон роста.
The в естественных условиях Демонстрация эффективности снижения продукции прогерина путем блокирования аберрантного сплайсинга является весомым кандидатом на роль ценного нового подхода к терапии прогерии.
(1) Осорио Ф.Г., Наварро К.Л., Кадиньянос Дж., Лопес-Мехия И.С., Кирос П.М. и др., Научная трансляционная медицина, 3: Выпуск 106, предварительная онлайн-публикация, 26 октября (2011).
(2) Скаффиди, П. и Мистели, Т. Изменение клеточного фенотипа при преждевременном старении, синдроме прогерии Хатчинсона-Гилфорда, Nature Medicine 11 (4): 440-445 (2005).
Июнь 2011 г.: исследование, финансируемое PRF, определяет рапамицин как возможное средство лечения прогерии
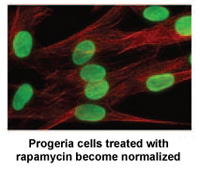
Исследователи из Национального института здравоохранения и Массачусетской больницы общего профиля в Бостоне, штат Массачусетс, опубликовали сегодня новое исследование в Наука, Трансляционная медицина что может привести к созданию нового лекарственного лечения для детей с прогерией.*
Рапамицин — одобренный FDA препарат, который ранее продлевал жизнь не прогерийным моделям мышей. Это новое исследование показывает, что рапамицин снижает количество болезнетворного белка прогерина на 50%, улучшает аномальную форму ядра и продлевает продолжительность жизни клеток прогерии. Это исследование предоставляет первые доказательства того, что рапамицин может быть способен уменьшить разрушительное воздействие прогерина у детей с прогерией.
По этому поводу есть огромное освещение в СМИ! Нажмите ниже, чтобы получить ссылки на статьи в СМИ:
Блог о здоровье Wall Street Journal
Фонд исследований прогерии был рад предоставить клетки для этого проекта из Банк клеток и тканей PRF, и помогите финансировать исследование через наш программа грантов.
Это новое захватывающее исследование демонстрирует поразительные темпы изучения прогерии, одновременно предоставляя более глубокое понимание процесса старения, который затрагивает всех нас.
*«Рапамицин изменяет клеточные фенотипы и усиливает выведение мутантных белков в клетках прогерии Хатчинсона-Гилфорда»
Кан Цао, Джон Дж. Грациотто, Сесилия Д. Блер, Джозеф Р. Маццулли, Майкл Р. Эрдос, Дмитрий Крайнц, Фрэнсис С. Коллинз
Sci Transl Med. 2011 29 июня;3(89):89ra58.
Июнь 2011 г.: новаторское исследование связи прогерии и старения
Вечерние новости CBS, Уолл Стрит Джорнал и Другие Отчет о новом исследовании
Исследователи Национального института здравоохранения обнаружили ранее неизвестную связь между прогерией и старением. Результаты дают представление о взаимосвязи между токсичным белком, вызывающим прогерию, известным как прогерин и теломеры, которые защищают концы ДНК внутри клеток до тех пор, пока они со временем не изнашиваются и клетки не умирают.
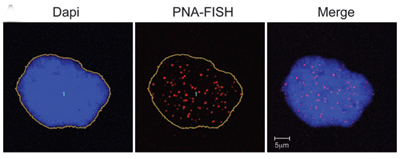
Клетки, экспрессирующие прогерин, у нормальных людей демонстрируют признаки старения. ДНК в ядре окрашена в синий цвет. Теломеры видны как красные точки.
Исследование* опубликовано в раннем онлайн-издании Journal of Clinical Investigation от 13 июня 2011 г. В нем делается вывод о том, что при нормальном старении короткие или дисфункциональные теломеры стимулируют клетки вырабатывать прогерин, который связан с возрастным повреждением клеток.
««Впервые мы знаем, что укорочение и дисфункция теломер влияют на выработку прогерина», — говорит медицинский директор Фонда исследований прогерии Лесли Б. Гордон, доктор медицины, доктор философии. «Таким образом, эти два процесса, оба из которых влияют на клеточное старение, на самом деле связаны».
Предыдущие исследования показали, что прогерин вырабатывается не только у детей с прогерией, но и в меньших количествах у всех нас, а уровень прогерина увеличивается с возрастом. Независимо от этого, предыдущие исследования укорочения и дисфункции теломер связывали с нормальным старением. С 2003 года, с открытием мутации гена прогерии и белка прогерина, вызывающего это заболевание, одно из ключевых направлений исследований было сосредоточено на понимании того, связаны ли прогерия и старение и как.
«Связь этого редкого заболевания и нормального старения приносит важные плоды», — сказал директор NIH Фрэнсис С. Коллинз, доктор медицины, доктор философии, старший автор статьи. «Это исследование подчеркивает, что ценные биологические знания получаются при изучении редких генетических заболеваний, таких как прогерия. С самого начала мы чувствовали, что прогерия может многому нас научить в отношении нормального процесса старения».
Ученые традиционно изучали теломеры и прогерин по отдельности. Хотя еще многое предстоит узнать о том, может ли эта новая связь привести к излечению детей с прогерией или потенциально применяться для продления человеческой жизни, это исследование предоставляет дополнительные доказательства того, что прогерин, токсичный белок, обнаруженный путем обнаружения мутации гена при прогерии, играет роль в нормальном процессе старения.
*Прогерин и дисфункция теломер совместно запускают клеточное старение в нормальных человеческих фибробластах, Цао и др., J Clin Invest doi:10.1172/JCI43578.
кликните сюда полный текст пресс-релиза NIH.
Май 2011 г.: обнаружена причина прогероидного синдрома, что дает дальнейшее представление о связи прогерии со старением
Исследовательская группа под руководством исследователя Progeria Доктор Карлос Лопес-Отин из Университета Овьедо в Испании столкнулись с двумя семьями, у детей которых ранее не было известное заболевание ускоренного старения, похожее на прогерию. У детей не было выявлено дефектов в каких-либо генах, которые ранее были связаны с прогероидными заболеваниями, но, изучая «кодирующие» части их геномов, команда обнаружила дефект в гене, называемом BANF1. У членов семьи с прогероидным заболеванием было очень низкое количество белка, вырабатываемого BANF1, и, как и у людей с прогерией, ядерные оболочки в их клетках были заметно ненормальными. Аномалии исчезали в экспериментах с культурой клеток, когда дефектный ген заменялся правильной версией. Результаты были опубликованы в Американский журнал генетики человека в мае 2011 года.
Теперь BANF1 присоединился к группе известных генов, которые, по-видимому, влияют на некоторые формы преждевременного старения, а также могут влиять на нормальное старение.
За последние несколько лет ученые смогли лучше понять нормальное старение на молекулярном уровне, отчасти благодаря исследованиям синдромов преждевременного старения, таких как этот, а также прогерии, которые «вызывают раннее развитие характеристик, обычно связанных с пожилым возрастом», сказал Лопес-Отин. Он добавил, что его исследование «подчеркивает важность ядерной пластинки для старения человека и демонстрирует полезность новых методов секвенирования генома для выявления генетической причины редких и разрушительных заболеваний, которым традиционно уделялось мало внимания».
Хосе С. Пуэнте, Виктор Кесада, Фернандо Г. Осорио, Рубен Кабанильяс, Хуан Кадиньянос, Джулия М. Фрайле, Гонсало Р. Ордоньес, Диана А. Пуэнте, Ана Гутьеррес-Фернандес, Мириам Фанжул-Фернандес и др. «Секвенирование экзома и функциональный анализ идентифицируют мутацию BANF1 как причину наследственного прогероидного синдрома». Американский журнал генетики человека, 5 мая 2011 г. DOI: 10.1016/j.ajhg.2011.04.010
Август 2010 г.: Инсулиноподобный фактор роста 1 улучшает симптомы и продлевает жизнь прогероидной мыши
26 августа 2010 г. Артериосклероз, тромбоз и сосудистая биология В электронном виде, до выхода в печать, опубликованы результаты исследования, сравнивающего прогерию и типичное сердечно-сосудистое старение, под названием «Сердечно-сосудистая патология при прогерии Хатчинсона-Гилфорда: корреляция с сосудистой патологией старения». Исследование показало, что прогерин, аномальный белок, вызывающий прогерию, также присутствует в сосудистой системе населения в целом и увеличивается с возрастом, что подтверждает растущую тенденцию к параллелям между нормальным старением и старением при прогерии.
Исследователи изучили результаты вскрытия сердечно-сосудистой системы и распределение прогерина у пациентов с прогерией, а также у группы без прогерии в возрасте от одного месяца до 97 лет и обнаружили, что у лиц без прогерии уровень прогерина в коронарных артериях увеличивался в среднем на 3,3 процента в год.
«Мы обнаружили сходство между многими аспектами сердечно-сосудистых заболеваний как при прогерии, так и при атеросклерозе, которым страдают миллионы людей по всему миру», — сказал доктор Лесли Гордон, старший автор исследования и медицинский директор Фонда исследований прогерии. «Изучая одно из самых редких заболеваний в мире, мы получаем важную информацию о заболевании, которым страдают миллионы людей по всему миру. Текущие исследования могут оказать значительное влияние на наше понимание болезней сердца и старения».
Это исследование подтверждает возможность того, что прогерин вносит вклад в риск атеросклероза среди населения в целом, и заслуживает изучения в качестве потенциального нового признака, помогающего прогнозировать риск сердечных заболеваний.
Олив М., Хартен И., Митчелл Р., Бирс Дж., Джабали К., Као К., Эрдос М.Р., Блэр К., Функе Б., Смут Л., Герхард-Херман М., Махан Дж.Т., Кутыс Р., Вирмани Р., Коллинз Ф.С., Уайт Т.Н., Набель Э.Г., Гордон Л.Б.
«Сердечно-сосудистая патология при прогерии Хатчинсона-Гилфорда: корреляция с сосудистой патологией старения». Артериосклеротический тромбососудистый биол. 2010 30(11) ноября:2301-9; Электронная публикация 2010 г., 26 августа.
Май 2010 г.: исследования Оксфорда показывают, как изучение прогерии может углубить наше понимание нормального старения.
Эта ситуация очень похожа на ситуацию при прогерии. Там преламин А (называемый прогерином) сохраняет фарнезильную группу. Действительно, начальным шагом в возникновении заболевания является неспособность удалить фарнезильную группу. Эта неспособность происходит из-за того, что мутация при прогерии приводит к удалению части преламина А, необходимой для того, чтобы FACE 1 связал и удалил фарнезильную группу. Таким образом, причина дефектов при старении и прогерии одна и та же: FACE1 не может выполнять свою работу.
В течение нескольких лет было известно, что ингибиторы фарнезилтрансферазы (FTI) подавляют (и могут обратить вспять) присутствие ядерных маркеров заболевания в клетках Progeria. Теперь Шанахан и др. обнаружили, что FTI подавляют появление подобных ядерных маркеров в клетках у пожилых нормальных людей. FTI в настоящее время используются в клинических испытаниях Progeria, и Шанахан и др. отмечают, что эти клинические испытания «прольют дополнительный свет на терапевтический потенциал этих препаратов в лечении старения».
Исследования, описанные в этой статье, являются лучшим на сегодняшний день примером того, как изучение прогерии способствует нашему пониманию нормального старения.
Рагнот К.Д., Уоррен Д.Т., Лю И., Шанахан К.М. и др., «Преламин А ускоряет старение гладкомышечных клеток и является новым биомаркером старения сосудов человека». Тираж: 25 мая 2010 г., стр. 2200-2210.
Апрель 2010 г.: Дополнительные доказательства того, что при прогерии наличие фарнезильной группы в молекуле прогерина является причиной симптомов заболевания.
Дэвис и его коллеги подготовили новую модель мыши, у которой преламин А, в отличие от преламина А RD, не фарнезилирован, но сохраняет последовательность из 15 аминокислот, которая обычно расщепляется на пути синтеза ламина А. У этой мыши нет прогероидных симптомов, что указывает на то, что при RD, как и при прогерии, за симптомы заболевания отвечает наличие фарнезильной группы, а не изменение аминокислотной последовательности.
DaviesBS, Barnes RH 2nd, Tu Y, Ren S, Andres DA, Spielmann HP, Lammerding J, Wang Y, Young SG, Fong LG,
«Накопление нефарнезилированного преламина А вызывает кардиомиопатию, но не прогерию», Хам Мол Генет. 2010 Апр 26. [Epub перед печатью]
Февраль 2010 г.: больше доказательств того, что ИИТ оказывают благотворное воздействие посредством фарнезилирования прогерина
Авторы оценили возможность того, что улучшение прогероидной болезни ингибитором фарнезилтрансферазы (FTI) в мышиной модели прогерии обусловлено влиянием препарата на фарнезилирование белка(ов), отличного от прогерина. Они сконструировали мышь, которая производила нефарнезилированный прогерин, но не фарнезилированный прогерин. У этой мыши также развились фенотипы заболевания, подобные прогерии, но FTI не улучшил их. Этот результат указывает на то, что препарат не действует путем ингибирования белков, отличных от прогерина; он должен действовать на фарнезилирование прогерина, биохимический этап, который отсутствует в тестируемой модели.
Ян Ш., Чан С.Й., Андрес ДА., Шпильманн Х.П., Янг С.Г., Фонг Л.Г. «Оценка эффективности ингибиторов фарнезилтрансферазы белка в мышиных моделях прогерии».
J Липидный Рес. 2010 февр.;51(2):400-5. Epub 2009 окт. 26.
Октябрь 2009: Искусство встречается с наукой в истории Бенджамина Баттона
Мэлони У. Дж., «Синдром прогерии Хатчинсона-Гилфорда: его описание в рассказе Ф. Скотта Фицджеральда «Загадочный случай Бенджамина Баттона» и его оральные проявления».
J. Dent. Res 2009 октябрь 88 (10): 873-6
Май 2009 г.: Статья открывает новые горизонты в изучении влияния HGPS на клеточные функции.
Ранее было показано, что HGPS влияет на многие фундаментальные клеточные функции, включая репликацию, экспрессию генов и репарацию ДНК. Буш и его коллеги добавили в этот список транспорт белков из цитоплазмы в ядро. Все белки синтезируются в цитоплазме, а те, которые в конечном итоге оказываются в ядре, должны пройти через ядерную мембрану. Транспорт осуществляется через каналы в ядерной мембране, называемые «ядерными порами». Многие белки слишком велики, чтобы просто диффундировать через ядерные поры, но «проводятся» через них специальными белками, которые эволюционировали для этой цели. В этой статье было обнаружено, что клетки, которые экспрессируют мутантный ген, ответственный за HGPS, имеют сниженный транспорт белков в ядра путем прямого измерения.
Буш А., Киль Т., Хойпель В.М., Венерт М., Хюбнер С., «Импорт ядерного белка снижен в клетках, экспрессирующих мутанты ламина А, вызывающие ядерную энвелопатию». Эксп. сопротивление ячейки. 2009 11 мая.
Апрель 2009 г.: Связь прогерии и нормального старения: новые идеи
→ Обеспечение структуры и организации: ядерная архитектура и целостность генома
→ Повреждение и восстановление ДНК пошли наперекосяк
→ Старые и не поддающиеся восстановлению супрессоры опухолей и клеточное старение, а также
→ Регенерация и обновление: биология стволовых клеток. Регенерация и обновление: биология стволовых клеток.
В статье освещаются способы, с помощью которых последние достижения в изучении прогероидных заболеваний дают представление об основных клеточных функциях, а также о старении.
Капелл Б.С., Тлоуган Б.Э., Орлов С.Дж., «От самых редких к самым распространенным: взгляд на рак кожи и старение с точки зрения прогероидных синдромов». Журнал исследовательской дерматологии (23 апреля 2009 г.), 1-11
Апрель 2009 г.: Прошлые получатели грантов PRF разработали новый метод изучения прогерина в клетках
Предыдущие эксперименты с клетками фибробластов от пациентов с прогерией показали, что повреждение, вызванное мутацией, изначально является результатом действия измененной формы ламина А, называемой прогерином. Но интерпретация этих экспериментов может быть затруднена в культуре для различного числа поколений. Фонг и др. создали экспериментальную систему, в которой количество прогерина в Дикий тип Клетки могут быть увеличены или уменьшены. Этот метод позволит исследователям отделить прямые эффекты прогерина от вторичных, тем самым продвигая изучение клеточных механизмов, которые приводят к патофизиологии клеток прогерии.
Активация синтеза прогерина, мутантного преламина А при синдроме прогерии Хатчинсона-Гилфорда, с помощью антисмысловых олигонуклеотидов. (Статья PubMed) Fong LG, Vickers TA, Farber EA, Choi C, Yun UJ, Hu Y, Yang SH, Coffinier C, Lee R, Yin L, Davies BS, Andres DA, Spielmann HP, Bennett CF, Young SG, «Активация синтеза прогерина, мутантного преламина А при синдроме прогерии Хатчинсона-Гилфорда, с помощью антисмысловых олигонуклеотидов». Хам Мол Генет. 2009 Апр 17.
Доктора Фонг и Янг ранее получали гранты от Фонда исследований прогерии.
Январь 2009 г.: Количественная оценка экспрессии гена прогерии в нормальных клетках и клетках прогерии с помощью нового мощного метода.
Шведская группа обнаружила накопление РНК прогерина в нормальных клетках по мере их старения
Прогерин — это аномальный белок, вызывающий прогерию. В последние годы несколько исследовательских групп обнаружили, что нормальные клетки также вырабатывают прогерин, но гораздо меньше, чем клетки ребенка с прогерией. Более того, количество белка прогерина в нормальных клетках увеличивается по мере их старения в лабораторных условиях. Эти результаты установили прямую связь на клеточном уровне между прогерией и нормальным старением.
Доктор Мария Эрикссон, автор открытия гена прогерии в 2003 году, теперь изобрела новый, мощный метод количественного измерения экспрессии гена прогерии. Лаборатория доктора Эрикссон в Каролинском институте в Швеции использовала этот метод для измерения количества РНК прогерина как в нормальных клетках, так и в клетках с прогерией. РНК — это молекула-схема в наших клетках для производства белка. Шведская группа обнаружила, что как нормальные клетки, так и клетки с прогерией производят все больше и больше РНК прогерина по мере старения. Результат Эрикссон показывает, что сигнал РНК для производства прогерина быстро формируется в клетках детей с прогерией и медленно формируется в течение жизни у всех нас.
Эти новые открытия укрепляют наше понимание связи между нормальным старением и прогерией. Кроме того, ожидается, что новая методика будет широко использоваться в экспериментах, посвященных механизму действия прогерина.
Родригес С., Коппеде Ф., Сагелиус Х. и Эриксон М. «Повышенная экспрессия укороченного транскрипта ламина А при синдроме прогерии Хатчинсона-Гилфорда во время старения клеток». Европейский журнал генетики человека (2009), 1-10.
Август и октябрь 2008 г.: обратима ли прогерия? Две недавние публикации показывают, что FTI и генная терапия могут сделать именно это!
Два отдельных исследования показывают, что прогерия обратима в сердечно-сосудистой системе и коже мышиных моделей. Эксперименты были значимы тем, что мышей не лечили до тех пор, пока у них не проявились симптомы прогерии, тогда как большинство предыдущих исследований начинали лечение до того, как прогерия была очевидна. Выработка прогерина (повреждающего белка, вырабатываемого геном прогерии) была подавлена либо обработкой ингибитором фарнезилтрансферазы (FTI), либо отключением гена. В обоих случаях мыши вернулись к нормальным или почти нормальным состояниям. Эти наблюдения дают обнадеживающие доказательства для текущего клинического испытания FTI для прогерии.
В ошеломляющей демонстрации прогресса с препаратом FTI, который теперь используется в Первое клиническое испытание препарата для лечения прогерии – Исследовательская группа доктора Фрэнсиса Коллинза в Национальном институте здравоохранения * обнаружила, что FTI предотвратили и даже обратили вспять наиболее разрушительный эффект прогерии у мышей: сердечно-сосудистые заболевания.* «Мы были поражены тем, что [препарат] сработал так хорошо», – говорит Фрэнсис Коллинз, генетик и бывший директор Национального института исследований генома человека, который был старшим автором исследовательской группы, идентифицировавшей мутацию гена прогерии в 2003 году. «Этот препарат не только предотвратил развитие сердечно-сосудистых заболеваний у этих мышей, но и обратил вспять повреждения у мышей, у которых уже было это заболевание».
У мышей с прогерией развивается болезнь сердца, которая отражает болезнь детей с прогерией. Авторы обнаружили, что FTI была способна как предотвратить развитие болезни сердца в некоторой степени, когда мышей лечили с момента отлучения от груди, так и частично обратить вспять уже существующую болезнь, когда мышей лечили, начиная с 9-месячного возраста. «Одной из поразительных вещей с моей точки зрения была способность обратить вспять болезнь», — сказал Коллинз, что имеет решающее значение, учитывая, что прогерия обычно не диагностируется при рождении, а только когда у детей начинают проявляться симптомы, когда часть ущерба уже нанесена.
«Если эти препараты окажут схожее действие на детей, это может стать крупным прорывом в лечении этой разрушительной болезни», — сказал доктор Набель из NHLBI, который был соавтором исследования. «Кроме того, эти результаты проливают свет на потенциальную роль препаратов FTI в лечении других форм ишемической болезни сердца».
Просмотреть статью в Научный американец, «Новая надежда для прогерии: лекарство от редкого заболевания старения», на https://www.sciam.com/article.cfm?id=new-hope-for-progeria-drug-for-rare-aging-disease и пресс-релиз NIH на https://www.nih.gov/news/health/oct2008/nhgri-06.htm
* Капелл и др., «Ингибитор фарнезилтрансферазы предотвращает как начало, так и позднее прогрессирование сердечно-сосудистого заболевания в модели мышей с прогерией». Труды Национальной академии наук, Том 105, № 41, 15902-15907 (14 октября 2008 г.)
Во втором исследовании, опубликованном в Интернете в Journal of Medical Genetics**, исследовательская группа доктора Марии Эрикссон из Каролинского института в Швеции создала еще одну модель прогерии на мышах с аномалиями кожи и зубов. Мыши были генетически модифицированы таким образом, что мутацию прогерии можно было отключить в любое время. Как только болезнь становилась очевидной, ген прогерии отключался. Через 13 недель кожа была почти неотличима от нормальной кожи. Это исследование показывает, что в этих тканях экспрессия мутации прогерии не вызывает необратимых повреждений и что обращение болезни вспять возможно, что дает надежду на лечение прогерии.
**Эрикссон и др., «Обратимый фенотип в мышиной модели синдрома прогерии Хатчинсона-Гилфорда». Журнал медицинской генетики. опубликовано онлайн 15 августа 2008 г.; doi:10.1136/jmg.2008.060772
Чтобы приобрести эту статью, перейдите по ссылке: https://jmg.bmj.com/cgi/rapidpdf/jmg.2008.060772v1
Еще больше доказательств связи между прогерией и нормальным старением и болезнями сердца
Эти захватывающие исследования Капелла и Эрикссона показывают, что помимо прогерии, эти результаты могут принести пользу всем пациентам с сердечно-сосудистыми заболеваниями. Исследователи обнаружили, что токсичный белок, ответственный за прогерию, на самом деле вырабатывается в небольших количествах у всех людей, возможно, накапливаясь по мере старения. Таким образом, изучая этих редких детей, мы можем углубить наше понимание основного механизма старения человека — и, возможно, найти новые способы замедлить этот процесс.
