ما الجديد في
بحث عن مرض الشيخوخة المبكرة
لقد أضفنا هذا القسم حتى تتمكن من الوصول بسهولة إلى المعلومات المتعلقة بأحدث وأهم المنشورات العلمية حول أبحاث مرض الشيخوخة المبكرة.
بالإضافة إلى المقالات الموضحة أدناه، هناك الآن مئات المقالات حول مرض الشيخوخة المبكرة والموضوعات المرتبطة به. نقترح عليك البحث في PubMed للعثور على الموضوع(المواضيع) المحددة التي تبحث عنها.
مارس 2023: إنجازات بحثية مثيرة في تقييم العلاج وإطالة العمر!
يسعدنا أن نشارك معكم تحديثين بحثيين مثيرين، تم نشرهما عبر الإنترنت اليوم في مجلة أمراض القلب والأوعية الدموية الرائدة في العالم، التوزيع (1):
العلامة الحيوية في مرض الشيخوخة المبكرة
تم تطوير طريقة جديدة لقياس البروجيرين، وهو البروتين السام الذي يسبب مرض الشيخوخة المبكرة، بواسطة فريق بقيادة الدكتورة ليزلي جوردون، المؤسس المشارك والمدير الطبي لمؤسسة PRF. ومع اكتشاف هذا المؤشر الحيوي، الذي يستخدم بلازما الدم لقياس مستويات البروجيرين، يمكن للباحثين فهم كيفية تأثير العلاجات على المشاركين في التجارب السريرية بعد فترة زمنية أقصر وفي نقاط متعددة على طول كل تجربة سريرية.
يمكن لهذا الاختبار تحسين عملية التجارب السريرية من خلال توفير معلومات مبكرة حول فعالية العلاجات التي يتم اختبارها، كمقدمة لاختبارات سريرية أخرى مثل زيادة الوزن، والتغيرات الجلدية، وتقلص المفاصل ووظيفتها، وما إلى ذلك، وكلها تتطلب وقتًا أطول بكثير لتظهر. هذه السمات السريرية لمرض الشيخوخة المبكرة هي مقاييس مهمة طويلة الأجل لتأثيرات العلاج والتي تكملها الآن مستويات البروجيرين المقاسة في وقت سابق من العلاج. قد نتمكن الآن من فهم فوائد العلاج في وقت مبكر يصل إلى أربعة أشهر بعد بدء العلاج، أو إيقاف العلاج الذي قد لا يفيد المشارك في التجربة، لتجنب الآثار الجانبية غير الضرورية.
حياة أطول مع لونافارنيب
بالإضافة إلى تسريع اكتشافات العلاج والشفاء في المستقبل، تشير هذه الطريقة الجديدة والمبتكرة لقياس البروجيرين إلى أن إن الفائدة طويلة المدى للونوفارنيب للأطفال المصابين بالشيخوخة المبكرة أكبر مما تم تحديده سابقًا.
تشير بيانات الدراسة إلى أن انخفاض مستويات البروجيرين في الدم يعكس فائدة البقاء على قيد الحياة: فكلما طالت مدة بقاء شخص مصاب بمرض الشيخوخة المبكرة على عقار لونافارنيب، زادت فائدة البقاء على قيد الحياة من العلاج. انخفضت مستويات البروجيرين بنحو 30-60% طوال فترة تناول الدواء، وقُدِّر متوسط العمر المتوقع للمرضى الذين يتلقون العلاج لأكثر من 10 سنوات بزيادة تقارب 5 سنوات. هذا يعني أن متوسط العمر المتوقع للمرضى الذين يتلقون العلاج لأكثر من 10 سنوات قد ارتفع بنحو 5 سنوات. زيادة في متوسط العمر المتوقع بمقدار 35%، من 14.5 سنة إلى ما يقرب من 20 سنة!
لمعرفة المزيد، راجع بياننا الصحفي هنا
"واحدة من أكثر القصص المذهلة التي تمت مشاركتها على الإطلاق في هذا البودكاست"
- الدكتورة كارولين لام، أخصائية القلب المشهورة عالميًا ومضيفة البودكاست الدورة الدموية أثناء الجري، في الرحلة التي أدت إلى هذه النتائج المثيرة. استمع إلى المقابلة كاملة حول التأثير العميق لهذه الدراسة مباشرة من الدكتور جوردون. استمع هنا (ابتداء من 6:41).
استمع إلى الدكتورة ليزلي جوردون في بودكاست Circulation on the Run
وفي شهر يونيو، نُشرت مقالتان افتتاحيتان (2) و (3) تم نشرها في التوزيع تسليط الضوء على الأهمية الحاسمة لهذا المؤشر الحيوي لتطوير العلاجات وعلاج الأطفال المصابين بالشيخوخة المبكرة وفهم الشيخوخة بشكل أفضل.

(1) جوردون، إل بي، نوريس، دبليو، هامرين، إس، وآخرون. بروجيرين البلازما في المرضى الذين يعانون من متلازمة هتشينسون جيلفورد بروجيريا: تطوير التحليل المناعي والتقييم السريري. التوزيع, 2023
(2) تطور التشوهات القلبية في متلازمة هتشينسون جيلفورد بروجيريا: دراسة طولية مستقبلية.
أولسن FJ، جوردون LB، سموت L، كلاينمان ME، جيرهارد هيرمان M، هيجدي SM، موكوندان S، ماهوني T، ماسارو J، ها S، براكاش A. التوزيع. 6 يونيو 2023؛147(23):1782-1784. doi: 10.1161/CIRCULATIONAHA.123.064370. Epub 5 يونيو 2023.
(3) أدوات متاحة بسهولة للكشف عن بروجيرين وتطور أمراض القلب في متلازمة هتشينسون جيلفورد بروجيريا.
إريكسون إم، هوجا ك، ريفيشون جي. التوزيع. 6 يونيو 2023؛147(23):1745-1747. doi: 10.1161/CIRCULATIONAHA.123.064765. Epub 5 يونيو 2023.
مارس 2021: اختراقات مثيرة في علاجات الحمض النووي الريبوزي لمرض الشيخوخة المبكرة!
نحن سعداء بمشاركة النتائج من دراستان مثيرتان للغاية حول استخدام العلاج بالحمض النووي الريبي في أبحاث مرض الشيخوخة المبكرة. تم تمويل الدراستين بشكل مشترك من قبل مؤسسة أبحاث الشيخوخة المبكرة (PRF) وشارك في تأليفهما المدير الطبي لمؤسسة أبحاث الشيخوخة المبكرة، الدكتور ليزلي جوردون.
البروجيرين هو البروتين المسبب للمرض في مرض الشيخوخة المبكرة. تتداخل علاجات الحمض النووي الريبي مع قدرة الجسم على إنتاج البروجيرين، عن طريق منع إنتاجه على مستوى الحمض النووي الريبي. وهذا يعني أن العلاج أكثر تحديدًا من معظم العلاجات التي تستهدف البروجيرين على مستوى البروتين.
على الرغم من أن كل دراسة استخدمت نظامًا مختلفًا لتوصيل الدواء، إلا أن كلتا الدراستين استهدفتا نفس استراتيجية العلاج الأساسية، حيث تثبيط إنتاج الحمض النووي الريبي الذي يشفر البروتين غير الطبيعي، بروجيرين. وقد قاد الدراستان باحثون في المعاهد الوطنية للصحة (NIH)، ونشرتا اليوم في مجلة الطب الطبيعي.
دراسة واحدةأظهرت دراسة أجراها الدكتور فرانسيس كولينز، مدير المعهد الوطني للصحة، أن علاج فئران بروجيريا بدواء يسمى SRP2001أدى ذلك إلى تثبيط التعبير الضار لبروتين mRNA والبروتين الموجود في الشريان الأورطيالشريان الأورطي، الشريان الرئيسي في الجسم، وكذلك في الأنسجة الأخرى. وفي نهاية الدراسة، ظل جدار الأبهر أقوى وأظهرت الفئران زيادة معدل البقاء على قيد الحياة لأكثر من 60%.
وقال كولينز: "إن الحصول على مثل هذه النتائج المهمة لعلاج الحمض النووي الريبي المستهدف في نموذج حيواني يمنحني الأمل في أن يؤدي هذا إلى تقدم كبير في علاج مرض الشيخوخة المبكرة".
ال دراسة اخرىأظهرت دراسة أجراها توم ميستلي، مدير مركز أبحاث السرطان في المعهد الوطني للسرطان، التابع للمعاهد الوطنية للصحة، 90 – 95% تقليل الحمض النووي الريبي المنتج للبروجيجين السام في أنسجة مختلفة بعد العلاج بدواء يسمى LB143. وجد مختبر ميستلي أن تقليل بروتين البروجيرين كان أكثر فعالية في الكبد، مع تحسنات إضافية في القلب والشريان الأورطي.
نحن نعلم الآن أن هناك طرقًا متعددة لتقليل إنتاج بروتين البروجيرين الضار باستخدام العلاج بالحمض النووي الريبي. وجدت كل دراسة امتدادات مختلفة من الحمض النووي الريبي في نماذج الفئران، والتي عند استهدافها، قدمت مسارًا فعالًا للعلاج، مما أدى إلى فئران بروجيريا التي عاشت لفترة أطول بكثير من تلك التي عولجت في دراسات سابقة باستخدام زوكينفي (لونوفارنيب)وهو الدواء الوحيد الذي وافقت عليه إدارة الغذاء والدواء الأمريكية لعلاج الأطفال المصابين بالشيخوخة المبكرة. وعلاوة على ذلك، وجد الباحثون أن العلاج المركب باستخدام العلاج بالحمض النووي الريبوزي وعقار زوكينفي (لونوفارنيب) أدى إلى خفض مستويات بروتين البروجيرين في الكبد والقلب بشكل أكثر فعالية من أي علاج منفرد.
"توضح هاتان الدراستان المهمتان للغاية التطورات الكبرى التي نمر بها الآن "في مجال علاجات بروجيريا المستهدفة،" قال الدكتور ليزلي جوردون، المدير الطبي لمؤسسة PRF. "لقد كنت سعيدًا بالعمل مع هذه المجموعات البحثية الرائعة لتطوير علاج الحمض النووي الريبي للأطفال المصابين بالبروجيريا. كلتا الدراستين مثيرتان لإثبات المبدأ، و تتطلع شركة PRF إلى المضي قدمًا نحو التجارب السريرية الذين يطبقون استراتيجيات العلاج هذه.
—
إردوس، مر، كابرال، واشنطن، تافاريز، UL وآخرون. نهج علاجي مضاد للاتجاه مستهدف لمتلازمة هتشينسون-جيلفورد بروجيريا. الطب الطبيعي (2021). https://doi.org/10.1038/s41591-021-01274-0
بوتاراجو، M.، جاكسون، M.، كلاين، S. وآخرون. يحدد الفحص المنهجي النوكليوتيدات العلاجية المضادة للاتجاه لمتلازمة هتشينسون جيلفورد. الطب الطبيعي (2021). https://doi.org/10.1038/s41591-021-01262-4
يناير 2021: تقدم ملحوظ في التحرير الجيني في نماذج فئران بروجيريا
المجلة العلمية طبيعة نتائج اختراقية منشورة أظهرت دراسة حديثة أن التحرير الجيني في نموذج الفأر المصاب بمرض الشيخوخة المبكرة أدى إلى تصحيح الطفرة التي تسبب مرض الشيخوخة المبكرة في العديد من الخلايا، وتحسين العديد من أعراض المرض الرئيسية، وزيادة العمر بشكل كبير في الفئران.
وقد وجدت الدراسة التي شارك في تمويلها PRF وشارك في تأليفها المدير الطبي لـ PRF الدكتور ليزلي جوردون، أنه باستخدام حقنة واحدة من محرر قاعدي مبرمج لتصحيح الطفرة المسببة للمرض، عاشت الفئران 2.5 مرة أطول من الفئران غير المعالجة المصابة بمرض بروجيريا، إلى سن يتوافق مع بداية الشيخوخة لدى الفئران السليمة. ومن المهم أن الفئران المعالجة احتفظت أيضًا بأنسجة وعائية صحية - وهو اكتشاف مهم، حيث أن فقدان سلامة الأوعية الدموية يعد مؤشرًا للوفاة لدى الأطفال المصابين بمرض بروجيريا.
أجرى الدراسة كل من الخبير العالمي في مجال التحرير الجيني، ديفيد ليو، من معهد برود التابع لمعهد ماساتشوستس للتكنولوجيا، وجوناثان براون، أستاذ مساعد في الطب في قسم طب القلب والأوعية الدموية في جامعة فاندربيلت، وفرانسيس كولينز، مدير المعاهد الوطنية للصحة.
قال الدكتور كولينز: "إن رؤية هذه الاستجابة الدرامية في نموذج الفأر المصاب بمرض بروجيريا هو أحد أكثر التطورات العلاجية المثيرة التي شاركت فيها على مدار 40 عامًا كطبيب وعالم".
"قبل خمس سنوات، كنا لا نزال ننهي تطوير أول محرر قاعدي على الإطلاق"، كما قال الدكتور ليو. "لو أخبرتني حينها أنه في غضون خمس سنوات، يمكن لجرعة واحدة من محرر القواعد أن تعالج مرض الشيخوخة المبكرة في الحيوانات على مستوى الحمض النووي، والحمض النووي الريبي، والبروتين، وعلم الأمراض الوعائية، ومتوسط العمر، لكنت قلت "لا توجد طريقة". إنها شهادة حقيقية على تفاني الفريق الذي جعل هذا العمل ممكنًا".
هناك حاجة إلى دراسات ما قبل السريرية إضافية للتحقيق في هذه النتائج، والتي نأمل أن تؤدي يومًا ما إلى تجربة سريرية. اقرأ المزيد عن هذه الأخبار المثيرة في هذا وول ستريت جورنال شرط.
نوفمبر 2020: موافقة إدارة الغذاء والدواء على عقار لونافارنيب (زوكينفي)
في 20 نوفمبر 2020، حققت PRF جزءًا مهمًا من مهمتنا: تم منح lonafarnib، أول علاج على الإطلاق لمرض الشيخوخة المبكرة، موافقة إدارة الغذاء والدواء.
انضم مرض الشيخوخة المبكرة الآن إلى أقل من 5% من الأمراض النادرة التي لها علاج معتمد من إدارة الغذاء والدواء الأمريكية.* يمكن للأطفال والشباب المصابين بمرض الشيخوخة المبكرة في الولايات المتحدة الآن الوصول إلى لونافارنيب (المسمى الآن "زوكينفي") عن طريق وصفة طبية، بدلاً من خلال تجربة سريرية.
لقد وصلنا إلى هذا الإنجاز التاريخي بفضل 13 عامًا من البحث الدؤوب الذي تضمن أربع تجارب سريرية، تم تنسيقها جميعًا بالتعاون مع PRF، وأصبحت ممكنة بفضل الأطفال الشجعان وأسرهم، وبتمويل منكم، أنتم مجتمع المانحين الرائع في PRF.
انقر هنا لمزيد من المعلومات.
*300 مرض نادر له علاج معتمد من إدارة الغذاء والدواء (https://www.rarediseases.info.nih.gov/diseases/FDS-orphan-drugs)/7000 مرض نادر معروف أساسه الجزيئي (www.OMIM.org) =4.2%
أبريل 2018: دراسة عالمية نُشرت في JAMA تتوصل إلى أن العلاج باستخدام لونافارنيب يطيل فترة البقاء على قيد الحياة لدى الأطفال المصابين بالشيخوخة المبكرة
العلاقة بين علاج لونافارنيب وعدم العلاج ومعدل الوفيات لدى المرضى المصابين بمتلازمة هتشينسون جيلفورد بروجيريا، ليزلي ب. جوردون، دكتوراه في الطب، دكتوراه؛ هيذر شابيل، دكتوراه؛ جو ماسارو، دكتوراه؛ رالف ب. داجوستينو الأب، دكتوراه؛ جوان برازيير، ماجستير؛ سوزان إي. كامبل، ماجستير؛ مونيكا إي. كلاينمان، دكتوراه في الطب؛ مارك دبليو كيران، دكتوراه في الطب، دكتوراه؛ جاما، 24 أبريل 2018.
يوليو 2016: نتائج التجربة الثلاثية
أكتوبر 2014: رحلة PRF الرائعة المنشورة في Expert Opinion
 في مقالة نشرت في رأي الخبراء وتم تأليف الكتاب من قبل المديرة التنفيذية أودري جوردون والمدير الطبي ليزلي جوردون، حيث يناقش زعيما PRF تاريخ PRF وأهدافها وإنجازاتها، وكيف كانت برامج PRF محورية في الرحلة من الغموض إلى العلاج.
في مقالة نشرت في رأي الخبراء وتم تأليف الكتاب من قبل المديرة التنفيذية أودري جوردون والمدير الطبي ليزلي جوردون، حيث يناقش زعيما PRF تاريخ PRF وأهدافها وإنجازاتها، وكيف كانت برامج PRF محورية في الرحلة من الغموض إلى العلاج.
*"مؤسسة أبحاث مرض الشيخوخة المبكرة: رحلتها المذهلة من الغموض إلى العلاج" 30 أكتوبر 2014
يكتب المؤلفون: "نأمل أن يساعد وصف برامج وخدمات PRF التالي، إلى جانب وصف لكيفية مساعدتهم لـ PRF في تحقيق مهمتها لإنقاذ الأطفال المصابين بالشيخوخة المبكرة، وإلهام الآخرين لاتخاذ إجراءات مماثلة للعديد من مجموعات الأمراض النادرة التي تحتاج إلى اهتمام فوري".
مايو 2014: دراسة تتوصل إلى أن الأدوية التجريبية تزيد من متوسط العمر المتوقع للأطفال المصابين بالشيخوخة المبكرة
وتوضح هذه الدراسة أن هناك أدلة تشير إلى أن مثبطات فارنيسيل ترانسفيراز (FTI) يمكنها إطالة عمر الأطفال المصابين بمرض الشيخوخة المبكرة بما لا يقل عن عام ونصف العام. وأظهرت الدراسة إطالة متوسط البقاء على قيد الحياة بمقدار 1.6 عام خلال الأعوام الستة التالية لبدء العلاج. وقد تساهم عقاران إضافيان أضيفا لاحقًا في التجارب، وهما برافاستاتين وزوليدرونات، في تحقيق هذه النتيجة. وهذا هو أول دليل على وجود علاجات تؤثر على معدلات البقاء على قيد الحياة لهذا المرض المميت.
انقر هنا لمزيد من التفاصيل.
تأثير مثبطات الفارنيسيل على البقاء على قيد الحياة في متلازمة هتشينسون جيلفورد بروجيريا، ليزلي ب. جوردون، دكتوراه في الطب، وجو ماسارو، دكتوراه، ورالف ب. داجوستينو الأب، دكتوراه، وسوزان إي. كامبل، ماجستير الآداب، وجوان برازيير، ماجستير العلوم، ودبليو تيد براون، دكتوراه في الطب، ودكتوراه، ومونيكا إي كلاينمان، دكتوراه في الطب، ومارك دبليو كيران، دكتوراه في الطب، وبرنامج التجارب السريرية لمتلازمة بروجيريا؛ التوزيع2 مايو 2014 (متاح على الانترنت).
سبتمبر 2012: اكتشاف أول علاج لمرض الشيخوخة المبكرة
نتائج أول تجربة سريرية على الإطلاق لعلاج الأطفال كشفت دراسة حديثة أن عقار لونافارنيب، وهو نوع من مثبطات فارنيسيل ترانسفيراز (FTI) الذي تم تطويره في الأصل لعلاج السرطان، أثبت فعاليته في علاج مرض الشيخوخة المبكرة. وقد أظهر كل طفل تحسنًا في واحدة أو أكثر من أربع طرق: اكتساب وزن إضافي، وتحسن السمع، وتحسن بنية العظام، و/أو الأهم من ذلك، زيادة مرونة الأوعية الدموية. وقد تم تمويل الدراسة* وتنسيقها من قبل مؤسسة أبحاث الشيخوخة المبكرة.
انقر هنا لمزيد من التفاصيل.
*جوردون إل بي، Kleinman ME، Miller DT، Neuberg D، Giobbie-Hurder A، Gerhard-Herman M، Smoot L، Gordon CM، Cleveland R، Snyder BD، Fligor B، Bishop WR، Statkevich P، Regen A، Sonis A، Riley S، Ploski C، Correia A، Quinn N، Ullrich NJ، Nazarian A، Liang MG، Huh SY، Schwartzman A، Kieran MW، تجربة سريرية لمثبط فارنيسيل ترانسفيراز في الأطفال المصابين بمتلازمة هتشينسون جيلفورد بروجيريا، وقائع الأكاديمية الوطنية للعلوم, 9 أكتوبر 2012 المجلد 109 العدد 41 16666-16671
أكتوبر 2011: نهج جديد لعلاج مرض الشيخوخة المبكرة
وقد تبين في عام 2005 أن عملية الربط الشاذة في خلايا الجلد المزروعة في مرض الشيخوخة المبكرة يمكن منعها بهذه الطريقة (2). ومع ذلك، لعلاج المرضى، يجب توصيل الكاشف المثبط سليمًا إلى جميع أنسجة المريض. وقد استغرق الأمر ست سنوات أخرى، وعملًا في العديد من المختبرات، لتطوير طرق "التوصيل" هذه.
في البحث الجديد (1)، أدى منع الوصل الشاذ في نموذج الفأر إلى نتائج مبهرة. كانت هناك انخفاضات واضحة في تركيزات البروجيرين في جميع الأنسجة التي تم تحليلها باستثناء العضلات الهيكلية، والتي قد يكون لديها امتصاص أقل للعامل المحظور. كررت الفئران النموذجية العديد من النمط الظاهري لمرضى بروجيريا، بما في ذلك
- انخفاض كبير في متوسط العمر المتوقع (103 أيام مقارنة بـ 2 سنة بالنسبة للفئران البرية).
- انخفاض معدل النمو.
- وضعية غير طبيعية مع انحناء العمود الفقري.
- انحرافات نووية عميقة نتيجة لتراكم البروجيرين.
- فقدان عام لطبقة الدهون الموجودة تحت الجلد.
- تغيرات عميقة في العظام.
- تغيرات في القلب والأوعية الدموية، بما في ذلك فقدان كبير في خلايا العضلات الملساء الوعائية.
- تغيرات في تركيزات الهرمونات المختلفة في بلازما الدم المتداولة، بما في ذلك الأنسولين وهرمون النمو.
ال في الجسم الحي إن إثبات فعالية تقليل إنتاج البروجيرين عن طريق منع الوصل الشاذ يعد مرشحًا قويًا لنهج جديد قيم لعلاج مرض الشيخوخة المبكرة.
(1) أوسوريو إف جي، نافارو سي إل، كاديانيانوس جيه، لوبيز-ميجيا آي سي، كيروس بي إم، وآخرون، علوم الطب الترجمي، 3: العدد 106، النشر الإلكتروني المسبق، 26 أكتوبر (تشرين الأول) 2011.
(2) Scaffidi, P. وMisteli, T. عكس النمط الظاهري الخلوي في مرض الشيخوخة المبكرة متلازمة هتشينسون جيلفورد بروجيريا، مجلة نيتشر ميديسين 11 (4): 440-445 (2005).
يونيو 2011: دراسة ممولة من PRF تحدد عقار راباميسين كعلاج محتمل لمرض الشيخوخة المبكرة
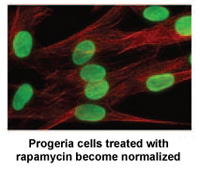
نشر باحثون في المعاهد الوطنية للصحة ومستشفى ماساتشوستس العام في بوسطن بولاية ماساتشوستس دراسة جديدة اليوم في العلوم والطب الانتقالي وهو ما قد يؤدي إلى إيجاد علاج جديد للأطفال المصابين بالشيخوخة المبكرة.*
راباميسين هو دواء معتمد من إدارة الغذاء والدواء الأمريكية وقد ثبت سابقًا أنه يطيل عمر نماذج الفئران غير المصابة بالشيخوخة المبكرة. وتوضح هذه الدراسة الجديدة أن الراباميسين يقلل من كمية بروتين البروجيرين المسبب للمرض بمقدار 50%، ويحسن الشكل النووي غير الطبيعي، ويطيل عمر خلايا الشيخوخة المبكرة. وتقدم هذه الدراسة أول دليل على أن الراباميسين قد يكون قادرًا على تقليل التأثيرات الضارة للبروجيرين لدى الأطفال المصابين بالشيخوخة المبكرة.
هناك تغطية إعلامية هائلة لهذا الموضوع! انقر أدناه للحصول على روابط للقصص الإعلامية:
أخبار الولايات المتحدة والتقرير العالمي
سعدت مؤسسة أبحاث مرض الشيخوخة المبكرة بتوفير الخلايا لهذا المشروع من بنك الخلايا والأنسجة PRF، والمساعدة في تمويل البحث من خلال برنامج المنح.
تظهر هذه الدراسة الجديدة المثيرة الوتيرة المذهلة لأبحاث مرض الشيخوخة المبكرة، مع توفير المزيد من الرؤى حول عملية الشيخوخة التي تؤثر علينا جميعًا.
*"يعكس الراباميسين النمط الظاهري الخلوي ويعزز إزالة البروتين المتحور في خلايا هتشينسون جيلفورد بروجيريا"
كان كاو، جون ج. جرازيوتو، سيسيليا د. بلير، جوزيف ر. مازولي، مايكل ر. إردوس، ديمتري كرينك، فرانسيس س. كولينز
Sci Transl Med. 2011 يونيو 29؛3(89):89ra58.
يونيو 2011: دراسة رائدة حول العلاقة بين مرض الشيخوخة المبكرة والشيخوخة
أخبار المساء على قناة سي بي إس, وول ستريت جورنال و آحرون تقرير عن دراسة جديدة
اكتشف باحثو المعاهد الوطنية للصحة ارتباطًا غير معروف سابقًا بين مرض الشيخوخة المبكرة والشيخوخة. توفر النتائج رؤى حول العلاقة بين البروتين السام المسبب لمرض الشيخوخة المبكرة والمعروف باسم بروجيرين و التيلوميرات، والتي تحمي أطراف الحمض النووي داخل الخلايا حتى تتآكل مع مرور الوقت وتموت الخلايا.
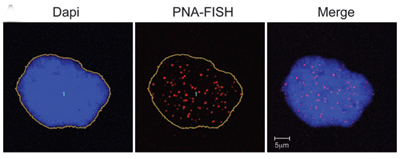
تظهر على الخلايا المعبرة عن البروجيرين من الأفراد الطبيعيين علامات الشيخوخة. ويظهر الحمض النووي في النواة باللون الأزرق. وتظهر التيلوميرات على شكل نقاط حمراء.
تظهر الدراسة* في الطبعة الإلكترونية المبكرة الصادرة في 13 يونيو 2011 من مجلة Journal of Clinical Investigation. وتستنتج الدراسة أنه في الشيخوخة الطبيعية، تعمل التيلوميرات القصيرة أو غير الوظيفية على تحفيز الخلايا لإنتاج البروجيرين، وهو الهرمون المرتبط بتلف الخلايا المرتبط بالعمر.
""لأول مرة، نعلم أن تقصير التيلومير واختلال وظيفته يؤثران على إنتاج البروجيرين"، كما يقول الدكتور ليزلي ب. جوردون، المدير الطبي لمؤسسة أبحاث الشيخوخة المبكرة. "وبالتالي فإن هاتين العمليتين، اللتين تؤثران على شيخوخة الخلايا، مرتبطتان بالفعل".
وقد أظهرت الأبحاث السابقة أن البروجيرين لا يتم إنتاجه فقط عند الأطفال المصابين بمرض الشيخوخة المبكرة، بل يتم إنتاجه بكميات أقل عند جميعنا، وتزداد مستويات البروجيرين مع التقدم في السن. وبشكل مستقل، ارتبطت الأبحاث السابقة حول تقصير التيلومير واختلال وظيفته بالشيخوخة الطبيعية. ومنذ عام 2003، مع اكتشاف طفرة جين مرض الشيخوخة المبكرة وبروتين البروجيرين الذي يسبب المرض، ركزت إحدى مجالات البحث الرئيسية على فهم ما إذا كان مرض الشيخوخة المبكرة والشيخوخة مرتبطين وكيف.
قال الدكتور فرانسيس إس كولينز، مدير المعهد الوطني للصحة، وأحد المؤلفين الرئيسيين للورقة البحثية: "إن ربط ظاهرة هذا المرض النادر بالشيخوخة الطبيعية يؤتي ثماره بطريقة مهمة. تسلط هذه الدراسة الضوء على أن دراسة الاضطرابات الوراثية النادرة مثل الشيخوخة المبكرة توفر رؤى بيولوجية قيمة. كان شعورنا منذ البداية أن الشيخوخة المبكرة لديها الكثير لتعلمنا إياه عن عملية الشيخوخة الطبيعية".
لقد درس العلماء تقليديا التيلوميرات والبروجيرين بشكل منفصل. وفي حين لا يزال هناك الكثير لنتعلمه حول ما إذا كان هذا الارتباط الجديد يمكن أن يؤدي إلى علاج للأطفال المصابين بالشيخوخة المبكرة أو يمكن تطبيقه على إطالة عمر الإنسان، فإن هذه الدراسة تقدم دليلا إضافيا على أن البروجيرين، البروتين السام الذي تم اكتشافه من خلال العثور على طفرة جينية في الشيخوخة المبكرة، يلعب دورا في عملية الشيخوخة الطبيعية.
*يتعاون بروجيرين وخلل التيلومير لتحفيز الشيخوخة الخلوية في الخلايا الليفية البشرية الطبيعية, كاو وآخرون، جيه كلين انفست doi:10.1172/JCI43578.
انقر هنا للحصول على النص الكامل للبيان الصحفي الصادر عن المعهد الوطني للصحة.
مايو 2011: اكتشاف سبب متلازمة الشيخوخة المبكرة، مما يوفر مزيدًا من الرؤى حول ارتباط الشيخوخة المبكرة بالشيخوخة
فريق بحثي بقيادة باحث في مرض بروجيريا الدكتور كارلوس لوبيز أوتين في دراسة أجراها باحثون بجامعة أوفييدو في إسبانيا، واجه فريق من الباحثين عائلتين يعاني أطفالهما من مرض الشيخوخة المتسارع غير المعروف سابقًا والذي يشبه مرض بروجيريا. لم يُظهِر الأطفال أي عيوب في أي جينات كانت مرتبطة سابقًا بأمراض الشيخوخة المبكرة، ولكن من خلال دراسة الأجزاء "المشفرة" من جينوماتهم، وجد الفريق عيبًا في جين يسمى BANF1. كان لدى أفراد الأسرة المصابين بمرض الشيخوخة المبكرة كميات منخفضة جدًا من البروتين الذي ينتجه BANF1، ومثل الأشخاص المصابين بمرض الشيخوخة المبكرة، كانت الأغلفة النووية في خلاياهم غير طبيعية بشكل ملحوظ. اختفت التشوهات في تجارب زراعة الخلايا عندما تم استبدال الجين المعيب بالنسخة الصحيحة. نُشرت النتائج في مجلة Neuropsychology. المجلة الأمريكية لعلم الوراثة البشرية في مايو 2011.
ينضم BANF1 الآن إلى مجموعة الجينات المعروفة التي يبدو أنها تؤثر على بعض أشكال الشيخوخة المبكرة - والتي قد تؤثر على الشيخوخة الطبيعية أيضًا.
وفي السنوات القليلة الماضية، تمكن العلماء من فهم الشيخوخة الطبيعية على المستوى الجزيئي بشكل أفضل بفضل دراسات متلازمات الشيخوخة المبكرة مثل هذا بالإضافة إلى متلازمة الشيخوخة المبكرة، والتي "تسبب التطور المبكر للخصائص المرتبطة عادة بالتقدم في السن"، كما قال لوبيز أوتين. وأضاف أن دراسته "تؤكد على أهمية الصفيحة النووية للشيخوخة البشرية وتوضح فائدة الأساليب الجديدة لتسلسل الجينوم لتحديد السبب الجيني للأمراض النادرة والمدمرة، والتي لم تحظ تقليديا إلا باهتمام محدود".
Xose S. Puente، Victor Quesada، Fernando G. Osorio، Rubén Cabanillas، Juan Cadiñanos، Julia M. Fraile، Gonzalo R. Ordóñez، Diana A. Puente، Ana Gutiérrez-Fernández، Miriam Fanjul-Fernández et al. "يحدد تسلسل إكسوم والتحليل الوظيفي طفرة BANF1 كسبب لمتلازمة البروجيرويد الوراثية." المجلة الأمريكية لعلم الوراثة البشرية، 5 مايو 2011 DOI: 10.1016/j.ajhg.2011.04.010
أغسطس 2010: عامل النمو الشبيه بالأنسولين 1 يحسن الأعراض ويطيل العمر في فأر بروجيرويد
في 26 أغسطس 2010، تصلب الشرايين، والجلطات، وعلم الأحياء الوعائي نُشرت إلكترونيًا، قبل الطباعة، نتائج دراسة قارنت بين الشيخوخة المبكرة والشيخوخة القلبية الوعائية النموذجية، بعنوان "أمراض القلب والأوعية الدموية في مرض هتشينسون جيلفورد: الارتباط بعلم الأمراض الوعائية للشيخوخة". وجدت الدراسة أن البروجيرين، وهو البروتين غير الطبيعي الذي يسبب مرض الشيخوخة المبكرة، موجود أيضًا في الأوعية الدموية لدى عامة السكان ويزداد مع تقدم العمر، مما يضيف إلى القضية المتزايدة التي تشير إلى وجود أوجه تشابه بين الشيخوخة الطبيعية والشيخوخة المبكرة.
قام الباحثون بفحص تشريح القلب والأوعية الدموية وتوزيع البروجيرين في المرضى الذين يعانون من مرض الشيخوخة المبكرة إلى جانب مجموعة غير مصابة بالشيخوخة المبكرة تتراوح أعمارهم بين شهر واحد و97 عامًا، ووجدوا أن البروجيرين في الأفراد غير المصابين بالشيخوخة المبكرة زاد بمعدل 3.3 في المائة سنويًا في الشرايين التاجية.
قال الدكتور ليزلي جوردون، المؤلف الرئيسي للدراسة والمدير الطبي لمؤسسة أبحاث الشيخوخة المبكرة: "لقد وجدنا أوجه تشابه بين العديد من جوانب أمراض القلب والأوعية الدموية في كل من مرض الشيخوخة المبكرة وتصلب الشرايين الذي يصيب ملايين الأشخاص في جميع أنحاء العالم". "من خلال فحص أحد أندر الأمراض في العالم، نكتسب رؤى حاسمة حول مرض يصيب ملايين الأشخاص في جميع أنحاء العالم. إن الأبحاث الجارية لديها القدرة على إحداث تأثير كبير على فهمنا لأمراض القلب والشيخوخة".
وتدعم هذه الدراسة إمكانية أن يكون البروجيرين مساهمًا في خطر الإصابة بتصلب الشرايين لدى عامة السكان، وتستحق الفحص باعتبارها سمة جديدة محتملة للمساعدة في التنبؤ بخطر الإصابة بأمراض القلب.
أوليف م، هارتن آي، ميتشل آر، بيرز جيه، جابالي كيه، كاو كيه، إردوس إم آر، بلير سي، فونكي بي، سموت إل، جيرهارد هيرمان إم، ماشان جيه تي، كوتيس آر، فيرماني آر، كولينز إف إس، وايت تي إن، نابل إي جي، جوردون إل بي.
"أمراض القلب والأوعية الدموية في مرض هتشينسون جيلفورد بروجيريا: الارتباط بعلم الأمراض الوعائية للشيخوخة". تصلب الشرايين الخثاري الوعائي البيولوجيا الوعائية. 2010 نوفمبر;30(11):2301-9; النشر الإلكتروني 2010، 26 أغسطس.
مايو 2010: أظهرت دراسات أكسفورد كيف يمكن لأبحاث مرض الشيخوخة المبكرة أن تعزز فهمنا للشيخوخة الطبيعية
إن هذا الوضع مشابه جدًا لما يحدث في مرض الشيخوخة المبكرة. ففي هذه الحالة يحتفظ بروتين البريلامين أ (المسمى بروجيرين) بمجموعة الفارنيسيل. والواقع أن الخطوة الأولى في التسبب في المرض هي الفشل في إزالة مجموعة الفارنيسيل. ويحدث هذا الفشل لأن طفرة البروجيريا تؤدي إلى حذف جزء من البريلامين أ اللازم لربط بروتين FACE 1 وإزالة مجموعة الفارنيسيل. وبالتالي فإن سبب العيوب في الشيخوخة ومرض الشيخوخة المبكرة هو نفسه: حيث لا يستطيع بروتين FACE1 القيام بوظيفته.
من المعروف منذ سنوات أن مثبطات فارنيسيل ترانسفيراز (FTIs) تمنع (ويمكنها عكس) وجود العلامات النووية للمرض في خلايا بروجيريا. الآن، وجد شاناهان وزملاؤه أن مثبطات فارنيسيل ترانسفيراز تمنع ظهور علامات نووية مماثلة في خلايا الأفراد العاديين المسنين. تُستخدم مثبطات فارنيسيل ترانسفيراز حاليًا في التجارب السريرية لمرض بروجيريا، ويشير شاناهان وزملاؤه إلى أن هذه التجارب السريرية "ستلقي مزيدًا من الضوء على الإمكانات العلاجية لهذه الأدوية في علاج الشيخوخة".
إن الدراسات الموصوفة في هذه المقالة هي أفضل مثال حتى الآن على كيفية مساهمة الدراسات التي أجريت على مرض الشيخوخة المبكرة في تعزيز فهمنا للشيخوخة الطبيعية.
Ragnauth CD, Warren DT, Liu Y, Shanahan CM et al, "Prelamin A يعمل على تسريع شيخوخة خلايا العضلات الملساء وهو علامة حيوية جديدة للشيخوخة الوعائية البشرية". الدورة: 25 مايو 2010، ص 2200-2210.
أبريل 2010: أدلة إضافية على أن وجود مجموعة فارنيسيل في جزيء البروجيرين في مرض الشيخوخة المبكرة هو المسؤول عن أعراض المرض.
قام ديفيز وزملاؤه بإعداد نموذج جديد للفأر، على عكس بريلامين أ في RD، لا يتم تحويله إلى فارنيسيلات، ولكنه يحتفظ بتسلسل الأحماض الأمينية الخمسة عشر الذي يتم قطعه عادة في المسار لتخليق لامين أ. لا يعاني هذا الفأر من أعراض الشيخوخة المبكرة، مما يشير إلى أنه في RD، وكذلك في Progeria، فإن وجود مجموعة الفارنيسيل، وليس التغيير في تسلسل الأحماض الأمينية، هو المسؤول عن أعراض المرض.
DaviesBS، Barnes RH 2nd، Tu Y، Ren S، Andres DA، Spielmann HP، Lammerding J، Wang Y، Young SG، Fong LG،
"تراكم بريلامين أ غير الفارنيسيل يسبب اعتلال عضلة القلب ولكن ليس الشيخوخة المبكرة", هم مول جينيت. 26 أبريل 2010. [نشر إلكتروني قبل الطباعة]
فبراير 2010: مزيد من الأدلة على أن مثبطات FTI توفر تأثيرات مفيدة من خلال فارنيسيلات بروجيرين
قام المؤلفون بتقييم احتمالية أن يكون تحسن مرض الشيخوخة المبكرة بواسطة مثبط فارنيسيل ترانسفيراز (FTI) في نموذج فأر لمرض الشيخوخة المبكرة ناتجًا عن تأثير الدواء على فارنيسيل بروتين (بروتينات) أخرى غير بروجيرين. قاموا ببناء فأر ينتج بروجيرين غير فارنيسيل، ولكن ليس بروجيرين فارنيسيل. طور هذا الفأر أيضًا أنماطًا مرضية شبيهة بمرض الشيخوخة المبكرة، لكن مثبط فارنيسيل ترانسفيراز (FTI) لم يخففها. تشير هذه النتيجة إلى أن الدواء لا يعمل عن طريق تثبيط البروتينات الأخرى غير بروجيرين؛ يجب أن يكون يعمل على فارنيسيل بروجيرين، وهي الخطوة الكيميائية الحيوية التي لا توجد في النموذج المختبر.
يانغ إس إتش، تشانج إس واي، أندريس دي إيه، سبيلمان إتش بي، يونج إس جي، فونج إل جي. "تقييم فعالية مثبطات بروتين فارنيسيل ترانسفيراز في نماذج الفئران المصابة بمرض الشيخوخة المبكرة".
مجلة بحوث الدهون 2010 فبراير؛51(2):400-5. نشر إلكتروني في 26 أكتوبر 2009.
أكتوبر 2009: الفنون تلتقي بالعلوم في قصة بنجامين باتون
مالوني دبليو جيه، "متلازمة هتشينسون-جيلفورد بروجيريا: عرضها في القصة القصيرة لف. سكوت فيتزجيرالد "الحالة الغريبة لبنجامين باتون" ومظاهرها الشفوية".
مجلة بحوث طب الأسنان 2009 أكتوبر 88 (10): 873-6
مايو 2009: مقال يفتح آفاقًا جديدة بشأن تأثير HGPS على الوظائف الخلوية.
وقد ثبت سابقًا أن HGPS يؤثر على العديد من الوظائف الخلوية الأساسية بما في ذلك التضاعف والتعبير الجيني وإصلاح الحمض النووي. وقد أضاف بوش وزملاؤه نقل البروتينات من السيتوبلازم إلى النواة إلى هذه القائمة. يتم تصنيع جميع البروتينات في السيتوبلازم، وتلك التي تنتهي في النواة يجب أن تعبر الغشاء النووي. يتم إنجاز النقل من خلال قنوات في الغشاء النووي تسمى "المسام النووية". العديد من البروتينات كبيرة جدًا بحيث لا تنتشر ببساطة عبر المسام النووية، ولكن "يتم" "دفعها" من خلالها بواسطة بروتينات خاصة تطورت لهذا الغرض. في هذه المقالة، وجد أن الخلايا التي تعبر عن الجين المتحور المسؤول عن HGPS لديها نقل منخفض للبروتينات إلى النوى عن طريق القياس المباشر.
بوش أ، كيل ت، هوبل دبليو إم، وينرت م، هوبنر س، "يتم تقليل استيراد البروتين النووي في الخلايا التي تعبر عن طفرات اللامين أ المسببة لاعتلال الغلاف النووي". خلية الدقة 11 مايو 2009.
أبريل 2009: ربط مرض الشيخوخة المبكرة بالشيخوخة الطبيعية: رؤى جديدة
→ توفير البنية والتنظيم: البنية النووية وسلامة الجينوم
→ تلف الحمض النووي وإصلاحه ذهبا في الاتجاه الخاطئ
→ مثبطات الأورام القديمة والتي لا يمكن إصلاحها وشيخوخة الخلايا، و
→ التجديد والتجدد: علم أحياء الخلايا الجذعية. التجديد والتجدد: علم أحياء الخلايا الجذعية.
تسلط المقالة الضوء على الطرق التي تساهم بها التطورات الحديثة في دراسة أمراض الشيخوخة في توفير نظرة ثاقبة للوظائف الخلوية الأساسية وكذلك الشيخوخة.
كابيل، بي إس، تلوغان، بي إي، أورلو، إس جيه، "من الأندر إلى الأكثر شيوعًا: رؤى من متلازمات الشيخوخة إلى سرطان الجلد والشيخوخة". مجلة الأمراض الجلدية الاستقصائية (2009 أبريل 23)، 1-11
أبريل 2009: ابتكر الحاصلون على منحة أبحاث PRF السابقة طريقة جديدة لدراسة بروجيرين في الخلايا
وقد أظهرت التجارب السابقة التي أجريت على الخلايا الليفية من مرضى بروجيريا أن الضرر الناجم عن الطفرة هو في البداية نتيجة لتأثير الشكل المتغير من لامين أ، المسمى بروجيرين. ولكن تفسير هذه التجارب قد يكون صعباً في المزرعة لعدد متفاوت من الأجيال. وقد أنشأ فونج وآخرون نظاماً تجريبياً يتم فيه قياس كمية بروجيرين في الخلايا الليفية. نوع بري يمكن زيادة أو تقليل الخلايا. ستسمح هذه الطريقة للباحثين بفرز التأثيرات المباشرة لـ Progerin من التأثيرات الثانوية، وبالتالي تقدم دراسة الآليات الخلوية التي تؤدي إلى الفسيولوجيا المرضية لخلايا Progeria.
تنشيط تخليق البروجيرين، وهو بروتين بريلامين أ الطافر في متلازمة هتشينسون جيلفورد، باستخدام الأوليجونوكليوتيدات المضادة للحس. (مقالة PubMed) فونغ إل جي، فيكرز تي إيه، فاربر إي إيه، تشوي سي، يون يو جيه، هو واي، يانغ إس إتش، كوفينير سي، لي آر، يين إل، ديفيز بي إس، أندريس دي إيه، سبيلمان إتش بي، بينيت سي إف، يونج إس جي، "تنشيط تخليق البروجيرين، البريلامين أ المتحور في متلازمة هتشينسون جيلفورد بروجيريا، باستخدام الأوليجونوكليوتيدات المضادة للحس". هم مول جينيت. 17 أبريل 2009.
وقد حصل الدكتور فونج والدكتور يونج في السابق على منح من مؤسسة أبحاث مرض الشيخوخة المبكرة.
يناير 2009: تحديد كمية التعبير الجيني لمرض الشيخوخة المبكرة في الخلايا الطبيعية وخلايا مرض الشيخوخة المبكرة باستخدام تقنية جديدة وقوية.
فريق سويدي يكتشف تراكم الحمض النووي الريبوزي منقوص الأكسجين في الخلايا الطبيعية مع تقدم العمر
البروجيرين هو البروتين غير الطبيعي المسبب لمرض الشيخوخة المبكرة. وفي السنوات الأخيرة، وجدت العديد من مجموعات البحث أن الخلايا الطبيعية تنتج أيضًا البروجيرين، ولكن بكميات أقل بكثير من خلايا الطفل المصاب بالشيخوخة المبكرة. وعلاوة على ذلك، تزداد كمية بروتين البروجيرين في الخلايا الطبيعية مع تقدم العمر في المختبر. وقد أثبتت هذه النتائج وجود ارتباط مباشر على المستوى الخلوي بين مرض الشيخوخة المبكرة والشيخوخة الطبيعية.
لقد ابتكرت الدكتورة ماريا إريكسون، مؤلفة البحث عن الجين المسؤول عن مرض بروجيريا في عام 2003، تقنية جديدة وقوية لقياس التعبير الكمي عن جين بروجيريا. وقد استخدم مختبر الدكتورة إريكسون في معهد كارولينسكا في السويد هذه التقنية لقياس كمية الحمض النووي الريبوزي للبروجيرين في كل من الخلايا الطبيعية وخلايا بروجيريا. والحمض النووي الريبوزي هو الجزيء النموذجي في خلايانا لإنتاج البروتين. وقد وجدت المجموعة السويدية أن كل من الخلايا الطبيعية وخلايا بروجيريا تنتج كميات أكبر وأكبر من الحمض النووي الريبوزي للبروجيرين مع تقدمها في العمر. وتُظهِر نتيجة إريكسون أن إشارة الحمض النووي الريبوزي لإنتاج البروجيرين تتراكم بسرعة في خلايا الأطفال المصابين بمرض بروجيريا، وتتراكم ببطء على مدار العمر فينا جميعًا.
تعزز هذه النتائج الجديدة فهمنا للعلاقة بين الشيخوخة الطبيعية ومرض الشيخوخة المبكرة. بالإضافة إلى ذلك، من المتوقع أن يتم استخدام التقنية الجديدة على نطاق واسع في التجارب التي تتناول آلية عمل البروجيرين.
رودريجيز س، كوبيدي ف، ساجيليوس هـ وإريكسون م. "زيادة التعبير عن نسخة لامين أ المقطوعة لمتلازمة هتشينسون جيلفورد بروجيريا أثناء شيخوخة الخلايا". المجلة الأوروبية لعلم الوراثة البشرية (2009), 1-10.
أغسطس وأكتوبر 2008: هل يمكن علاج مرض الشيخوخة المبكرة؟ أظهرت منشورتان حديثتان أن العلاج بالهرمونات البديلة والعلاج الجيني قد يكونان فعالين في هذا الأمر!
وقد أظهرت دراستان منفصلتان أن مرض بروجيريا قابل للعكس في الجهاز القلبي الوعائي وجلد نماذج الفئران. وكانت التجارب ذات أهمية كبيرة في عدم علاج الفئران حتى ظهرت عليها أعراض بروجيريا، في حين بدأت معظم الدراسات السابقة العلاج قبل ظهور أعراض بروجيريا. وقد تم تثبيط إنتاج البروجيرين (البروتين الضار المصنوع من جين بروجيريا) إما عن طريق العلاج بمثبطات فارنيسيل ترانسفيراز (FTI) أو عن طريق إيقاف تشغيل الجين. وفي كلتا الحالتين عادت الفئران إلى حالتها الطبيعية أو شبه الطبيعية. وتوفر هذه الملاحظات أدلة مشجعة للتجربة السريرية الحالية لمثبطات فارنيسيل ترانسفيراز لعلاج بروجيريا.
في عرض مذهل للتقدم الذي أحرزناه مع عقار FTI - والذي يتم استخدامه الآن في أول تجربة سريرية على الإطلاق لعلاج مرض بروجيريا – وجد فريق البحث التابع للدكتور فرانسيس كولينز في المعاهد الوطنية للصحة أن FTI منعت وحتى عكست التأثير الأكثر تدميراً لمرض بروجيريا في الفئران: أمراض القلب والأوعية الدموية.* يقول فرانسيس كولينز، عالم الوراثة والمدير السابق للمعهد الوطني لأبحاث الجينوم البشري، والذي كان المؤلف الرئيسي لفريق البحث الذي حدد طفرة جين بروجيريا في عام 2003: "لقد أذهلنا أن [الدواء] نجح بشكل جيد للغاية. لم يمنع هذا الدواء هذه الفئران من الإصابة بأمراض القلب والأوعية الدموية فحسب، بل عكس الضرر في الفئران التي كانت تعاني بالفعل من المرض".
وتصاب فئران بروجيريا بأمراض القلب التي تشبه تلك التي تصيب الأطفال المصابين بالبروجيريا. ووجد الباحثون أن العلاج بالهرمونات البديلة كان قادراً على منع تطور أمراض القلب إلى حد ما عندما عولجت الفئران منذ فطامها، وعكس المرض جزئياً عندما عولجت الفئران بدءاً من سن 9 أشهر. وقال كولينز: "من الأمور المذهلة من وجهة نظري هي القدرة على عكس المرض"، وهو أمر بالغ الأهمية نظراً لأن البروجيريا لا يتم تشخيصها عموماً عند الولادة، ولكن فقط عندما يبدأ الأطفال في إظهار الأعراض، عندما يكون جزء من الضرر قد حدث بالفعل.
وقال الدكتور نابيل من المعهد الوطني للقلب والرئة والدم، والذي شارك في تأليف الدراسة: "إذا ثبت أن هذه الأدوية لها تأثيرات مماثلة على الأطفال، فقد يمثل هذا تقدمًا كبيرًا في علاج هذا المرض المدمر. بالإضافة إلى ذلك، تسلط هذه النتائج الضوء على الدور المحتمل لأدوية FTI في علاج أشكال أخرى من مرض الشريان التاجي".
عرض المقال في مجلة ساينتفك امريكان"أمل جديد لمرض الشيخوخة المبكرة: دواء لمرض الشيخوخة النادر"، في https://www.sciam.com/article.cfm?id=new-hope-for-progeria-drug-for-rare-aging-disease والبيان الصحفي الصادر عن المعهد الوطني للصحة في https://www.nih.gov/news/health/oct2008/nhgri-06.htm
* كابيل، وآخرون، "يمنع مثبط فارنيسيل ترانسفيراز كل من ظهور أمراض القلب والأوعية الدموية والتقدم المتأخر لها في نموذج فأر بروجيريا." وقائع الأكاديمية الوطنية للعلوم، المجلد 105، العدد 41، 15902-15907 (14 أكتوبر 2008)
وفي دراسة ثانية نشرت على الإنترنت في مجلة علم الوراثة الطبية، ابتكر فريق البحث التابع للدكتورة ماريا إريكسون في معهد كارولينسكا في السويد نموذجًا آخر لفأر مصاب بمرض الشيخوخة المبكرة يعاني من تشوهات في الجلد والأسنان. وقد تم هندسة الفئران وراثيًا بحيث يمكن إيقاف طفرة الشيخوخة المبكرة في أي وقت. وبمجرد ظهور المرض، تم إيقاف جين الشيخوخة المبكرة. وبعد 13 أسبوعًا، أصبح الجلد غير قابل للتمييز تقريبًا عن الجلد الطبيعي. وتُظهر هذه الدراسة أن التعبير عن طفرة الشيخوخة المبكرة في هذه الأنسجة لا يسبب ضررًا لا رجعة فيه وأن عكس المرض ممكن، وهو ما يعطي وعدًا بعلاج الشيخوخة المبكرة.
**إريكسون وآخرون، "النمط الظاهري القابل للعكس في نموذج الفأر لمتلازمة هتشينسون جيلفورد بروجيريا". مجلة الطب الجيني. نُشرت على الإنترنت في 15 أغسطس 2008؛ doi:10.1136/jmg.2008.060772
لشراء هذا المقال، انتقل إلى: https://jmg.bmj.com/cgi/rapidpdf/jmg.2008.060772v1
مزيد من الأدلة على العلاقة بين مرض الشيخوخة المبكرة والشيخوخة الطبيعية وأمراض القلب
وتُظهِر دراسات كابيل وإريكسون المثيرة أن هذه النتائج، بخلاف مرض الشيخوخة المبكرة، قد تفيد جميع المرضى المصابين بأمراض القلب والأوعية الدموية. فقد اكتشف الباحثون أن البروتين السام المسؤول عن مرض الشيخوخة المبكرة يُنتَج في الواقع بمستويات منخفضة لدى جميع البشر، وربما يتراكم مع تقدمنا في السن. وعلى هذا، فمن خلال دراسة هؤلاء الأطفال النادرين، يمكننا تعزيز فهمنا لآلية رئيسية للشيخوخة البشرية ــ وربما نجد طرقاً جديدة لإبطاء هذه العملية.
