Klinische Studien &
Managed Access-Programm
Klinische Arzneimittelstudien zu Progerie: Hintergrund
 Klinische Arzneimittelstudien gegen Progerie sind die beste Hoffnung für Kinder mit Progerie. Sie testen mögliche Behandlungen, die ihnen ein längeres und gesünderes Leben ermöglichen könnten. Diese Studien sind der Höhepunkt jahrelanger Forschung, die sich darauf konzentrierte, mit welchem Medikament oder welcher Medikamentenkombination die Kinder behandelt und geheilt werden können.
Klinische Arzneimittelstudien gegen Progerie sind die beste Hoffnung für Kinder mit Progerie. Sie testen mögliche Behandlungen, die ihnen ein längeres und gesünderes Leben ermöglichen könnten. Diese Studien sind der Höhepunkt jahrelanger Forschung, die sich darauf konzentrierte, mit welchem Medikament oder welcher Medikamentenkombination die Kinder behandelt und geheilt werden können.
Seit wir 1999 PRF gründeten und es keine Ressourcen für diese Kinder gab, haben wir uns aus der völligen Unbekanntheit hochgearbeitet, über die Entdeckung von Genen, die ersten klinischen Studien zu Progerie und die erste von der FDA zugelassene Behandlung namens Lonafarnib – und das alles in einem Tempo, das in der wissenschaftlichen Gemeinschaft praktisch beispiellos ist. Und während wir dieser Handvoll Kinder helfen, hat die Verbindung von Progerie zu häufigen Herzkrankheiten und Alterung enorme Auswirkungen für uns alle.
Wie geht es weiter mit Behandlung und Heilung?
Startschuss für eine neue klinische Arzneimittelstudie: Die Anmeldung für die Progerininstudie hat begonnen!
PRF hat in Zusammenarbeit mit dem in Korea ansässigen Studiensponsor PRG Science & Technology (PRG S&T) mit der Anmeldung für eine brandneue klinische Studie mit einem Medikament namens Progerinin begonnen. Laborergebnisse zeigen, dass dieses Medikament in Kombination mit Lonafarnib wirksamer sein kann als Lonafarnib allein. PRF finanzierte die Laborarbeit, die zur Gründung von PRG S&T und der Entwicklung von Progerinin führte. Die Vorstudienarbeiten haben im Boston Children's Hospital begonnen, in der Erwartung, in den kommenden Monaten Kinder aus aller Welt zur Anmeldung für diese Studie zu gewinnen. Wir sind sehr aufgeregt, eine neue Studie mit einem so vielversprechenden Medikament zu beginnen, und freuen uns darauf, Ihnen weitere Einzelheiten mitzuteilen, sobald diese verfügbar sind.
Bitte wenden Sie sich an Shelby Phillips, um mehr über den Test zu erfahren.
E-Mail: sphillips@progeriaresearch.org
WhatsApp, Telegram, WeChat: 1-987-876-2407
Bürotelefon: 988-548-5308
PRF-Mitbegründerin und Geschäftsführerin Audrey Gordon besiegelt im Juni den Deal mit Dr. Bum-Joon Park von PRG S&T, um mit den vorgerichtlichen Arbeiten fortzufahren.
RNA-Therapie: Arzneimittelverabreichung Machbarkeitsstudie ist abgeschlossen!
PRF hat die ersten patientenbezogenen Schritte in Richtung einer klinischen Studie zur RNA-Therapie unternommen – SO aufregend!
Hintergrund: Im Januar 2021 berichteten wir bahnbrechende Erkenntnisse in der RNA-Therapeutik, wobei diese Therapie gehemmte Produktion von RNA, die für das Progeria-Krankheitsprotein Progerin kodiert. Die Studie* unter der Leitung von Dr. Francis Collins, Wissenschaftlicher Berater des Weißen Hauses und ehemaliger Direktor der National Institutes of Health (NIH), ergab, dass Progeria-Mäuse, die mit einem Medikament namens SRP-2001 behandelt wurden, reduzierte die schädliche Progerin-mRNA- und Proteinexpression in Blutgefäßensowie in anderen Geweben. Die Blutgefäße waren stärker und die Mäuse zeigten eine erhöhtes Überleben von über 60% im Vergleich zu unbehandelten Mäusen. Daher wurde die Arbeit an dieser vielversprechenden Therapie fortgesetzt und wir haben die Nächster Schritt mit einem Machbarkeitsstudie wie folgt:
Normalerweise sind RNA-Therapeutika Flüssigkeiten, die intravenös (direkt in die Vene) injiziert werden. Patienten mit Progerie würden jedoch die intravenöse Verabreichung der erforderlichen Tagesdosis nicht vertragen. Daher entwickelte PRF ein subkutanes Verabreichungssystem wobei die Flüssigkeit mit einer kleinen Nadel unter die Haut gespritzt werden kann. Eine 6-monatige Studie am BCH wurde durchgeführt, um die Durchführbarkeit dieses Verabreichungsansatzes für Patienten mit Progerie zu ermitteln.. Das Team testete, ob die Verabreichung einer Kochsalzlösung bequem subkutan injiziert werden kann und welches Injektionssystem und welche Injektionsstelle am bequemsten sind. Sobald die Daten aus dieser Studie analysiert sind, werden wir einen Schritt näher an einer klinischen Studie zur Gentherapie!
*Erdos, MR, Cabral, WA, Tavarez, UL et al. Ein gezielter Antisense-Therapieansatz für das Hutchinson-Gilford-Progerie-Syndrom. Nat Med (2021).
Was passiert HEUTE in den klinischen Studien zu Progerie?
Die jüngste Studie umfasste zwei Medikamente: lOnafarnib und ein neues Medikament, Everolimus. Phase 1 zur Bestimmung der sicheren und angemessenen Dosierung von Everolimus begann im April 2016 und wurde im Juni 2017 erfolgreich abgeschlossen. Phase 2, in der die Wirksamkeit der Kombination aus zwei Medikamenten getestet wurde, begann im Juli 2017 und wurde im April 2022 abgeschlossen. Sechzig Kinder aus 27 Ländern nahmen an dieser Phase mit zwei Medikamenten teil!
Everolimus ist eine Form des Medikaments Rapamycin; Everolimus könnte Kindern mit Progerie leichter verabreicht werden, da weniger Blutentnahmen zur Messung des Medikamentenspiegels erforderlich sind. Während Lonafarnib die Entwicklung des toxischen Progerins blockieren kann, scheint Rapamycin den Zellen zu ermöglichen, Progerin schneller abzubauen. Da Rapamycin auf einen anderen Weg als Lonafarnib abzielt, könnte sich die Kombination als „Doppelschlag“ gegen Progerie erweisen – hoffentlich eine bessere Behandlung als Lonafarnib allein.
Wir befinden uns nun in einer Phase der Datenanalyse und rechnen damit, die Ergebnisse schließlich in einer von Experten begutachteten wissenschaftlichen Zeitschrift zu veröffentlichen. In der Zwischenzeit sind die Studienteilnehmer entweder in die Monotherapie-Erweiterung der Studie oder in ein anderes Zugangsprogramm übergegangen. In beiden Fällen erhalten die Teilnehmer weiterhin Lonafarnib, die derzeitige Standardbehandlung.
Die Studienhistorie im Überblick
Bisher hat PRF vier klinische Studien finanziert und mitkoordiniert. PRF ist und war schon immer für alle Studienkosten verantwortlich, einschließlich Tests, Reisen, Verpflegung, Unterkunft, Übersetzer und Personal. Jede neue Studie ist teurer als die letzte, da sich mehr Kinder für eine Chance auf ein längeres, gesünderes Leben anmelden.
Einzelheiten zu den vorherigen Prozessen
#1 umfasste ein einzelnes Medikament, Lonafarnib, wurde 2007 begonnen und erwies sich als erfolgreich. Lesen Sie alles über die historische Behandlungsentdeckung Hier.
#2, der Machbarkeitsteil der „Triple Trial“, umfasste 3 Medikamente: Lonafarnib, Pravastatin und Zoledronat. Diese einmonatige „Ministudie“ der Phase 1 fand im März 2009 statt, um festzustellen, ob die Hinzufügung von 2 weiteren Medikamenten zur Lonafarnib-Behandlung bei einer größeren Population sicher war (was der Fall war).
#3, die „Triple Trial“, war eine Fortsetzung der Machbarkeitsstudie und war eine Phase-2-Studie, die im August 2009 begann. Ihr Protokoll wurde im Laufe von fünf Jahren geändert, indem man wieder auf nur Lonafarnib umstellte und die Aufnahme wieder öffnete, damit mehr Kinder teilnehmen konnten. Lesen Sie mehr Hier.
#4 ist die Studie mit den beiden Medikamenten Lonafarnib und Everolimus. Phase 1 zur Bestimmung der sicheren und angemessenen Dosierung von Everolimus begann im April 2016 und wurde im Juni 2017 erfolgreich abgeschlossen. Phase 2, in der die Wirksamkeit der Kombination der beiden Medikamente getestet wurde, begann im Juli 2017 und wurde im April 2022 abgeschlossen. Die Monotherapie-Erweiterung dieser Studie wird heute fortgesetzt.
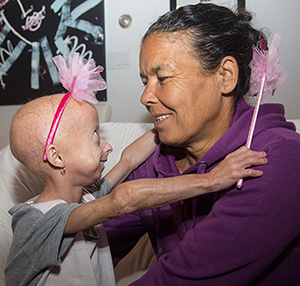
7. Mai 2007: Der Beginn der allerersten klinischen Arzneimittelstudie zu Progerie markiert einen historischen Moment in der Geschichte der Progerieforschung!
Im Jahr 2006 identifizierten Forscher eine mögliche medikamentöse Behandlung für Kinder mit Progerie, sogenannte FTI. Zum ersten Mal standen wir vor einer möglichen Behandlung für Kinder mit Progerie. Spannende Zeiten! Die klinische Studie zum Progeria-Medikament begann am 7. Mai 2007 mit der Ankunft von zwei Kindern – Meghan und Megan – im Boston Children's Hospital in Boston, MA, zu ihrem ersten von sieben Besuchen über einen Zeitraum von zwei Jahren. Bei diesem ersten Besuch wurden sie umfangreichen Tests unterzogen und erhielten ihre erste Dosis des Medikaments. Danach reisten bis Dezember 2009 durchschnittlich zwei Familien pro Woche nach Boston, gefolgt von einer Zeitspanne, in der das Studienteam die vielen tausend Datenelemente analysierte (jedes Kind wurde pro Besuch über 100 Tests unterzogen!) und die Veröffentlichung der Ergebnisse anstrebte.
„Mir ist keine andere seltene genetische Erkrankung bekannt, bei der es von der Genentdeckung bis zur klinischen Erprobung weniger als vier Jahre gedauert hat – ein phänomenaler Beweis für die harte Arbeit der Progeria Research Foundation.“
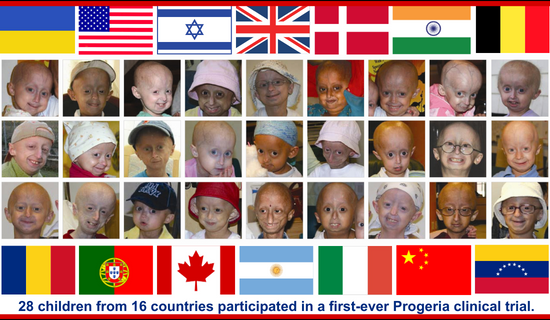
Es nahmen 28 Kinder aus 16 Ländern im Alter von 3 bis 15 Jahren teil. Die Kinder kehrten alle vier Monate zu Tests und zur Medikamentenversorgung ins Bostoner Kinderkrankenhaus zurück und blieben bei jedem Besuch 4-8 Tage in Boston. Während ihrer Zeit zu Hause beobachteten ihre Ärzte die Kinder genau und legten dem Bostoner Forschungsteam regelmäßig Gesundheitsberichte vor. Während der Dauer der Studie reisten durchschnittlich 2 Kinder pro Woche nach Boston, um teilzunehmen.
Wer, Wo, Wann, Wie und Wie viel…
Die ersten drei klinischen Studien wurden von Mark Kieran MD, PhD geleitet, Leiter der Abteilung für pädiatrische medizinische Neuroonkologie, Dana-Farber Cancer Institute und Children's Hospital Boston; Assistenzprofessor, Abteilungen für Pädiatrie und Hämatologie/Onkologie, Harvard Medical School. Dr. Kieran ist ein pädiatrischer Onkologe mit umfangreicher Erfahrung mit dem untersuchten Medikament (Farnesyltransferase oder FTI) bei Kindern. 2017 gab er seine Stelle bei Dana Farber auf, um in der Privatwirtschaft zu arbeiten. Co-Vorsitzende waren Monica Kleinman, MD, Leiterin der medizinisch-chirurgischen Intensivstation, leitende Mitarbeiterin für Intensivmedizin am BCH, Assistenzprofessorin an der Harvard Medical School; und Leslie Gordon, MD, PhD, Medizinische Leiterin der PRF, Dozentin am BCH und der Harvard Medical School, Professorin für Pädiatrie am Hasbro Children's Hospital und der Brown University in Providence, RI. Dr. Kleinman hat die Leitungsrolle des leitenden Prüfarztes übernommen.
Die klinischen Studien sind ein Gemeinschaftsprojekt von Ärzten des Boston Children's Hospital, des Dana-Farber Cancer Institute und des Brigham and Women's Hospital., alle Einrichtungen der Harvard University. Darüber hinaus trugen Ärzte und Wissenschaftler der Warren Alpert Medical School der Brown University und des NIH dazu bei, dass dieser erste und die anderen Versuche erfolgreich waren.
Wie sind wir an diesen Punkt gelangt?
Im Jahr 2003 hat das Forschungsteam der Progeria Research Foundation entdeckte das Progeria-Gen. Diese Entdeckung führte nicht nur zu einem besseren Verständnis von Progerie, sondern Wissenschaftler wissen jetzt auch, dass das Studium von Progerie uns helfen kann, mehr über Herzkrankheiten und den normalen Alterungsprozess zu erfahren, der uns alle betrifft. Seit der Genentdeckung hat uns die Unterstützung von Forschern, Klinikern, Familien von Kindern mit Progerie und Menschen wie IHNEN an einen weiteren Scheideweg bei der Suche nach einer Behandlung gebracht. Forscher begannen eine intensive Studie dieses feindlichen Proteins namens Progerin, und im Jahr 2006 identifizierten sie eine mögliche medikamentöse Behandlung für Kinder mit Progerie, die sogenannten Farnesyltransferase-Inhibitoren (FTIs), und führten im Labor Studien durch, die eine Studie am Menschen mit dem Medikament unterstützten. Der ausgewählte FTI wurde ursprünglich von Merck geliefert und hieß Lonafarnib. klicken Sie hier für weitere Einzelheiten zur Forschung.
Warum glaubten die Forscher, dass dieses Medikament bei Progerie wirken würde?
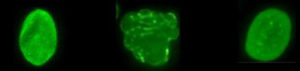
Normale Zelle, Progeriezelle, Progeriezelle nach der Behandlung mit FTI.
Das Protein, das unserer Meinung nach für Progerie verantwortlich ist, heißt Progerin. Um die normale Zellfunktion zu blockieren und Progerie zu verursachen, muss ein Molekül namens „Farnesylgruppe“ an das Progerinprotein angehängt werden. FTIs wirken, indem sie die Anheftung der Farnesylgruppe an Progerin blockieren (hemmen). Wenn also das FTI-Medikament diese Anheftung der Farnesylgruppe bei Kindern mit Progerie blockieren kann, kann Progerin „gelähmt“ und die Progerie gelindert werden. klicken Sie hier für weitere Informationen zu FTIs.
Wie hat PRF die Studie finanziert?
Dank der Unterstützung Tausender konnten wir alle notwendigen Mittel aufbringen, um die Kosten der Studie zu decken. Unser tiefempfundener Dank gilt allen, die ihre „Zeit, Talente und ihr Vermögen“ eingebracht haben, um diese unglaubliche Leistung zu ermöglichen, und natürlich allen mutigen Familien, die teilgenommen haben.
Der FTI Lonafarnib ist jetzt eine bewährte Behandlung für Progerie.
Im Jahr 2012 wurden die Studienergebnisse veröffentlicht, die zeigten, dass jedes Kind in einem oder mehreren Bereichen, einschließlich des lebenswichtigen Herz-Kreislauf-Systems, eine Verbesserung erfuhr. Im Mai 2014 zeigte eine Studie, dass eines oder mehrere von drei Medikamenten – darunter Lonafarnib –, die in PRF-finanzierten klinischen Studien getestet wurden, die Lebensdauer verlängerten; es war unklar, welches Medikament diese positive, lebensverändernde Wirkung hatte. Im April 2018 veröffentlichte jedoch eine Studie in Das Journal der American Medical Association (JAMA) berichteten, dass Lonafarnib allein das Überleben bei Kindern mit Progerie um mindestens 1,6 Jahre verlängerte. klicken Sie hier für Einzelheiten zur historischen Behandlungsentdeckungsstudie 2012, Hier für Einzelheiten zu den Ergebnissen von 2014 und Hier für Einzelheiten zur Studie von 2018.
„ALLE waren so wunderbar. Für uns seid ihr ALLE von Gott gesandt und wir SCHÄTZEN alles, was ihr für diese kleinen Engel tut. Unsere Familie ist so überwältigt von der Aufregung und allen möglichen Emotionen wegen Adalias Reise nach Boston an diesem Wochenende, dass ich gar nicht in Worte fassen kann, wie wir uns fühlen.“
„Dieses neue Medikament für Zach gibt uns neue Hoffnung, dass sein Herz stärker, sein Lächeln strahlender und sein Leben länger wird. Dieser neue Medikamententest ist eine Antwort auf unsere Gebete. Vielen Dank an alle, die bei PRF mitgearbeitet haben und dies möglich gemacht haben … die Ärzte, die Forscher und das Personal. Ihr seid unsere Helden!“
„Im Namen von Cam und unserer Familie danke ich Ihnen allen bei PRF für alles, was Sie getan haben! Ohne Sie wären wir in einer Welt voller Verwirrung und Trauer verloren gewesen. Stattdessen leben wir in einer Welt voller Hoffnung und Zielstrebigkeit. Nochmals vielen Dank! Mit viel Liebe und Respekt.“

Immer vorwärts: Die Dreifachstudie zu Progerie-Medikamenten beginnt im August 2009
Zusammenfassung:
Forscher haben zwei weitere Medikamente identifiziert, die in Kombination mit dem derzeit getesteten FTI-Medikament (Lonafarnib) eine noch wirksamere Behandlung für Kinder mit Progerie bieten könnten als FTI allein. Pravastatin und Zoledronat wurden zur aktuellen Behandlung mit Lonafarnib hinzugefügt. An dieser viel größeren Studie nahmen 45 Kinder aus 24 verschiedenen Ländern teil!
Strategie:
Alle drei Medikamente zielen auf verschiedene Punkte auf dem Weg ab, der zur Produktion des krankheitserregenden Progerins führt. In spannenden Laborstudien, die der Spanier Dr. Carlos Lopez-Otin auf dem wissenschaftlichen Workshop der Progeria Research Foundation 2007 vorstellte, verbesserten die beiden neuen Medikamente die Krankheit in Progeria-Zellen und verlängerten die Lebensdauer in Progeria-Mausmodellen.
Ziel:
Wenn die drei in dieser Studie verabreichten Medikamente diese Farnesylgruppenbindung wirksam blockieren können, könnte Progerin „gelähmt“ werden und die Progerie könnte sich sogar noch bessern als mit Lonafarnib allein. Die Hoffnung ist, dass die Medikamente als Partner wirken und sich gegenseitig ergänzen, sodass das Progerinprotein durch die Kombination der drei Medikamente stärker beeinflusst wird.
Der Machbarkeitsversuch:
Das Team führte eine Ministudie mit 5 Kindern mit Progerie durch. Die kurze, einmonatige „Machbarkeitsstudie“ untersuchte, ob die Kombination der drei Medikamente gut verträglich wäre, bevor eine größere internationale Studie gestartet wurde. Die Nebenwirkungen waren akzeptabel, und das Team ging zur größeren Wirksamkeitsstudie über.
Der Wirksamkeitstest:
An dieser Studie nahmen 45 Kinder aus 24 Ländern teil, die 17 Sprachen sprechen. Dazu gehören Kinder, die an der FTI-Studie teilgenommen haben, die Teilnehmer der Machbarkeitsstudie und andere Kinder, die entweder zu jung waren, um an der ersten Studie teilzunehmen, oder Kinder, die wir während der ersten klinischen Studie entdeckt haben (nachdem die Teilnehmerzahl beendet war). Kinder, die an der FTI-Studie teilgenommen hatten, hatten die Möglichkeit, sich bei ihrem letzten Besuch für die aktuelle Studie für die Dreifachstudie anzumelden. Dadurch konnten diese Kinder FTI weiter einnehmen, ohne Dosen zu vergessen.
Testmedikamente im Überblick
Pravastatin (vermarktet als Pravachol oder Selektine) gehört zur Arzneimittelklasse der Statine. Es wird normalerweise zur Senkung des Cholesterinspiegels und zur Vorbeugung von Herz-Kreislauf-Erkrankungen eingesetzt.
Zoledronsäure ist ein Bisphosphonat, wird üblicherweise als Knochenmedikament zur Linderung von Osteoporose und zur Vorbeugung von Skelettbrüchen bei Menschen mit bestimmten Krebsarten eingesetzt.
Lonafarnib ist ein FTI (Farnesyltransferase-Hemmer), ein Medikament, das im Labor eine Anomalie in Progeriezellen rückgängig machen kann und bei Progerie-Mäusen eine Besserung der Krankheit bewirkt hat.
Alle drei Medikamente blockieren die Produktion des Farnesylmoleküls, das Progerin zur Entstehung der Krankheit Progerie benötigt.
* „Kombinierte Behandlung mit Statinen und Aminobisphosphonaten verlängert die Lebensdauer in einem Mausmodell der vorzeitigen Alterung beim Menschen”, von Ignacio Varela, Sandrine Pereira, Alejandro P. Ugalde, Claire L. Navarro, María F. Suarez, Pierre Cau, Juan Cadinanos, Fernando G. Osorio, Nicolas Foray, Juan Cobo, Felix de Carlos, Nicolas Levy, Jose MP Freije und Carlos Lopez-Otán. Nature Medicine, 2008. 14(7): p. 767-72.
Im Juli Studie ** wurde veröffentlicht, aus dem hervorging, dass im Vergleich zur Monotherapie mit Lonafarnib keine signifikanten Verbesserungen festgestellt wurden. **Gordon et al., Klinische Studie mit den Protein-Farnesylierungsinhibitoren Lonafarnib, Pravastatin und Zoledronsäure bei Kindern mit Hutchinson-Gilford-Progerie-Syndrom, Verkehr, 10.1161/CIRCULATIONAHA.116.022188
Allerdings wurde der „Triple Trial“ über seinen ursprünglichen Zeitrahmen von 2–3 Jahren hinaus verlängert und auf bis zu 80 Kinder ausgeweitet, damit jedes Kind Zugang zu Lonafarnib allein hat, weil wir wissen, dass es den Kindern hilft. Normalerweise laufen klinische Studien ab und die Patienten werden bis zur Zulassung durch die FDA von allen Medikamenten entwöhnt; dies kann Jahre dauern. PRF hat sichergestellt, dass die Kinder weiterhin die einzige bekannte Behandlung erhalten, während sie und ihre Forschungspartner weiterhin zusätzliche Behandlungsmöglichkeiten erforschen (wie Everolimus, das derzeit getestet wird).
Die Hinzufügung eines neueren Medikament: Everolimus
Everolimus ist eine Form des Medikaments Rapamycin; Everolimus könnte Kindern mit Progerie leichter verabreicht werden, da weniger Blutentnahmen zur Messung des Medikamentenspiegels erforderlich sind. Während Lonafarnib die Entwicklung des toxischen Progerins blockieren kann, scheint Rapamycin den Zellen zu ermöglichen, Progerin schneller abzubauen. Da Rapamycin auf einen anderen Weg als Lonafarnib abzielt, könnte sich die Kombination als „Doppelschlag“ gegen Progerie erweisen – hoffentlich eine bessere Behandlung als Lonafarnib allein.
Die Wissenschaft hinter der Hinzufügung dieses zweiten Medikaments
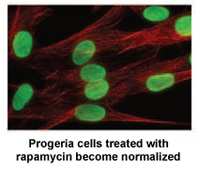
Rapamycin ist ein von der FDA zugelassenes Medikament, das nachweislich die Lebensdauer von Mausmodellen ohne Progerie verlängert. Eine Studie* von Forschern des NIH in Bethesda, MD und des Massachusetts General Hospital in Boston zeigt, dass Rapamycin die Menge des krankheitserregenden Proteins Progerin um 50% verringert, die abnormale Kernform verbessert und die Lebensdauer von Progeriezellen im Labor verlängert.
Rapamycin ist für seine Anti-Aging-Eigenschaften bei Mäusen bekannt. Diese Ergebnisse sind Teil einer wachsenden Liste von Studien, die dazu beitragen, die Theorie zu bestätigen, dass die Entdeckung eines Heilmittels für Progerie auch der gesamten alternden Bevölkerung zugute kommen könnte.
* K. Cao, J. J. Graziotto, C. D. Blair, J. R. Mazzulli, M. R. Erdos, D. Krainc, F. S. Collins, „Rapamycin kehrt zelluläre Phänotypen um und verbessert die Clearance mutierter Proteine in Hutchinson-Gilford-Progerie-Syndrom-Zellen.“ Sci. Transl. Med. 3, 89ra58 (2011).
Die Progeria Research Foundation stellte für dieses Projekt Zellen zur Verfügung aus der PRF Zell- und Gewebebank und half bei der Finanzierung der Forschung durch unsere Stipendienprogramm – ein weiterer Beweis dafür, dass die forschungsbezogenen Programme der PRF für Fortschritte auf dem Weg zur Heilung von wesentlicher Bedeutung sind.
Dieser Zwei-Medikamenten-Test war eine Gemeinschaftsanstrengung, die auf den Erkenntnissen aus früheren klinischen Studien von PRF aufbaute. Die Kinder wurden von praktisch demselben Ärzteteam des Boston Children's Hospital und des Brigham and Women's Hospital untersucht, die mittlerweile alle über weltweit anerkannte Expertise in Sachen Progerie und den eingesetzten Medikamenten verfügen.
An dieser Phase mit zwei Medikamenten nahmen 60 Kinder aus 27 Ländern teil. Die Daten aus dem Teil der Studie mit zwei Medikamenten werden derzeit analysiert und die Ergebnisse werden für die Veröffentlichung in einer von Experten begutachteten wissenschaftlichen Zeitschrift formuliert und niedergeschrieben.
Unsere Suche nach einem Heilmittel geht weiter …
Unsere Arbeit mit Gentherapien schreitet mit Volldampf voran! RNA-Therapie und DNA-Gen-Editing-Studien haben gezeigt, eine große Verbesserung der Lebensdauer von Progeria-Mäusen. PRF investiert weiterhin erhebliche Mittel in ihre Entwicklung, in der Hoffnung, dass diese Forschungsanstrengungen zu klinischen Studien und letztendlich zur Heilung führen.
Diese hochmodernen Therapien haben großes Potenzial! Mit Ihrer Hilfe kann PRF weiterhin so schnell wie möglich Fortschritte bei der Entwicklung der wirksamsten Behandlungen und Heilung erzielen.

